Тиреотропный гормон (ТТГ) в Москве недорого
Анализ ТТГ — это разновидность лабораторного исследования. Анализ крови на ТТГ заключается в исследовании показателя тиреотропного гормона, который производится гипофизом. Этот анализ позволяет выявить различного рода отклонения в работе щитовидки и определить заболевания, с ней связанные.
Анализ крови на гормоны ТТГ
Анализ ТТГ очень важен, так как может выявлять отклонения в виде:
- сбоя в регуляции обменных процессов;
- сбоя в теплообмене;
- сбоя в поддержании функций дыхательных органов;
- изменения в усвоении кислорода клетками;
- отклонения в перемещении глюкозы в ткани и ее переработки.
Биохимический анализ крови ТТГ
Анализы на гормоны ТТГ рекомендуется проводить, когда пациент замечает некоторые изменения в своем состоянии:
- анализ на кровь ТТГ помогает выяснить причину частых депрессивных состояний;
- ТТГ крови назначается при резком и значительном снижении температуры тела;
- исследование уровня ТТГ способно определить причину отставания ребенка в умственном и половом развитии;
- анализ крови на тиреотропный гормон назначается при ухудшении функций мышечного аппарата;
- тест ТТГ обязателен при подозрении на скрытое течение гипотиреоза;
- исследование ТТГ рекомендуется при аменорее;
- анализ на тиреотропный гормон является обязательным при импотенции, бесплодии и снижении полового влечения.

Гипотиреоз
Гипотиреоз — это заболевание, при котором диагностируется острая или хроническая недостаточность тиреоидных гормонов. При гипотиреозе уровень ТТГ определяется только при сдаче соответствующего анализа. Значения ТТГ при гипотиреозе помогает диагностировать заболевание на ранней стадии, соответственно, еще до возникновения характерной симптоматики. Гипотиреоз и высокий ТТГ является первичным показателем наличия патологии в организме.
Показатели Т3, Т4, ТТГ при гипотиреозе
Гипотиреоз возникает в случае, когда щитовидка не секретирует гормоны на необходимом уровне. Работой этого органа управляет гипофиз, за счет чего и продуцируется тиреотропный гормон, а показатели гормонов при гипотиреозе щитовидной железы резко «переступают» границы норм. При обращении в наши клиники, можно определить, достаточное ли количество гормонов вырабатывается, и уровень, на котором произошли изменения в работе щитовидки.
По ТТГ при гипотиреозе и разделяют три степени заболевания:
- Первая стадия гипотиреоза обуславливается наличием пелагических процессов в структуре железы, влияющих на ее работу.
 Уровень ТТГ при гипотиреозе является одним из главных показателей развития заболевания, так как чаще всего на этой стадии болезнь себя не выказывает.
Уровень ТТГ при гипотиреозе является одним из главных показателей развития заболевания, так как чаще всего на этой стадии болезнь себя не выказывает. - Вторая стадия заболевания развивается при поражении гипофиза вследствие опухоли, инсульта или травмы. При сбое работы гипофиза показатели Т3, Т4, ТТГ при гипотиреозе резко снижаются.
- Третья стадия — это показатель патологии гипоталамуса. Показатели гормонов щитовидной железы при гипотиреозе в данном случае являются аспектом для назначения нашим врачом правильного и эффективного лечения. Чтобы иметь представление о стоимости наших услуг, можно ознакомиться с информацией ниже. Важно запомнить, что при гипотиреозе ТТГ понижен или повышен в зависимости от сложности протекания болезни.
Гипертиреоз
Гипертиреоз — это заболевание, при котором отмечается чрезмерная активность щитовидки и выработки тиреоидных гормонов. Следствием увеличения количества выработки гормонов в крови является активизация обменных процессов, что негативным образом сказывается на общем состоянии человека. Показатели гормонов щитовидной железы при гипертиреозе способны показать наличие отклонений в работе органа и помочь нашему специалисту подобрать правильную методику лечения.
Показатели гормонов щитовидной железы при гипертиреозе способны показать наличие отклонений в работе органа и помочь нашему специалисту подобрать правильную методику лечения.
Показатели ТТГ при гипертиреозе
Показатель ТТГ при гипертиреозе щитовидной железы повышается, но при нормальном уровне Т3 и Т4 такое повышение свидетельствует о сублинической форме гипотиреоза. Показатели тиреотропного гормона при гипертиреозе показывают отклонения в работе щитовидки и являются главным аспектом при постановке диагноза гипертиреоз.
Когда уровень ТТГ при гипертиреозе повышается, а показатели Т3 и Т4 наоборот снижаются, это является следствием гипотиреоза. Когда ТТГ при гипертиреозе щитовидной повышается и выходит за допустимые пределы нормы, наш специалист настоятельно рекомендует дополнительные методики обследования. Повышение ТТГ при гипертиреозе может стать окончательным показателем для установки диагноза и назначения терапевтического лечения. Гормональные расстройства могут длительное время не проявлять себя и скрываться за характерной симптоматикой других заболеваний. Одной из причин ухудшения состояния здоровья может быть изменение уровня тиреотропного гормона ТТГ. Исследование ТТГ может рассказать специалисту о многом и помочь составить правильный план лечения.
Одной из причин ухудшения состояния здоровья может быть изменение уровня тиреотропного гормона ТТГ. Исследование ТТГ может рассказать специалисту о многом и помочь составить правильный план лечения.
Нормы анализа ТТГ
Любое незначительное отклонение тиреотропного гормона от нормы может привести к серьезным изменениям в организме человека. Именно поэтому так важен контроль состояния пациента квалифицированным специалистом для дальнейшего лечения.
В основании головного мозга в костном углублении расположена наиболее важная железа в теле человека — гипофиз. Она контролирует работу гормональной и эндокринной системы организма путем выработки различных гормонов, среди которых есть и гормон тиреотропин (ТТГ).
ТТГ в норме управляет деятельностью щитовидной железы, а именно:
- улучшает усвоение йода клетками организма;
- определяет окончательные размеры щитовидной железы;
- контролирует выработку щитовидкой гормонов Т3 и Т4;
- повышает активность работы клеток щитовидной железы.

Именно от соотношения уровня выработки тироксина и ТТГ зависит общее состояние организма. Повышение гормона Т4 приводит к снижению тиреотропина, а его понижение — к повышению выработки гормона ТТГ в организме.
Сбои в работе гормональной системы могут долгое время никак себя не проявлять, и скрываться под ярко выраженными симптомами других заболеваний. Окончательно выяснить причину ухудшения общего состояния здоровья и начать лечение можно лишь узнав, тиреотропный гормон в норме или нет.
Гормон ТТГ в норме:
- участвует в процессе синтеза фосфолипидов, белков, нуклеиновых кислот, обмене веществ;
- влияет на выработку гормонов щитовидной железы;
- регулирует работу нервной, сердечно-сосудистой, пищеварительной, репродуктивной систем, процесс терморегуляции и двигательной активности;
- способствует нормальному протеканию беременности и развитию плода;
- поддерживает оптимальный баланс женских половых гормонов.

Тиреотропный гормон: нормы и рекомендации при подготовке к анализу
Учитывая тот факт, что гормон ТТГ, функции которого мы ранее описывали, может спровоцировать нарушения деятельности многих органов и систем, любой врач может выписать направление на сдачу этого анализа.
Основными показаниями того, что норма анализа ТТГ снижена или превышена, являются:
- ухудшение работы мышечного аппарата;
- интенсивное выпадение волос;
- ощущения сильного сердцебиения;
- сбои менструального цикла;
- бессонница;
- отставание в умственном и половом развитии ребенка;
- бесплодие и импотенция у мужчин;
- снижение либидо;
- резкое увеличение массы тела;
- запоры и диарея;
- непереносимость холода.
Концентрация ТТГ в крови меняется на протяжении суток. Его максимальное количество отслеживается примерно в 2–4 часа ночи, а минимальное — в 17–19 часов. При постоянном бодрствовании секреция гормона нарушается. Также временное снижение тиреотропина характерно для периода беременности.
При постоянном бодрствовании секреция гормона нарушается. Также временное снижение тиреотропина характерно для периода беременности.
Контроль над уровнем тиреотропного гормона очень важен, поэтому для прохождения процедуры сдачи анализа вам стоит обратиться к специалистам нашего центра.
ПРАВИЛА ПОДГОТОВКИ К АНАЛИЗУ КРОВИ ТТГ
Данное исследование подвержено суточным колебаниям, поэтому кровь необходимо сдавать строго в определенное время суток – до 10 утра, если врач не назначил иного.
Кровь берется из вены. Необходимо соблюдать общие рекомендации:
- кровь сдается утром натощак или не ранее, чем через 2–4 часа после приема пищи;
- допускается употребление воды без газа;
- накануне анализа следует отказаться от алкоголя, исключить физическое и эмоциональное перенапряжение;
- отказаться от курения за 30 минут до исследования;
- не стоит сдавать кровь в период приема медикаментов, если врач не назначил иное.

недостаточноеобразование гормонов щитовидной железы: причины, симптомы, диагностика и методы лечения на сайте «Альфа-Центр Здоровья»
Заболевание, обусловленное недостаточным образованием гормонов щитовидной железы. Сопровождается потерей веса, сонливостью, зябкостью, нарушением менструального цикла, брадикардией.Гипотиреоз — самое распространенное нарушение функции щитовидной железы. В большинстве стран, в частности в России, гипотиреоз обусловлен дефицитом йода. Распространенность гипотиреоза в мире составляет 5%.
Неспособность щитовидной железы вырабатывать достаточные количества гормогов (T4 и T3) — самая частая причина гипотиреоза, называемая первичным гипотиреозом. Вторичный гипотиреоз встречается значительно реже. Значительная часть случаев гипотиреоза обусловлена так называемыми аутоиммунными заболеваниями щитовидной железы — хроническим лимфоцитарным тиреоидитом и первичным идиопатическим гипотиреозом. (В первом случае имеется зоб, во втором — атрофия щитовидной железы. ) Подобно другим аутоиммунным болезням, они поражают женщин намного чаще, чем мужчин (8:1).
) Подобно другим аутоиммунным болезням, они поражают женщин намного чаще, чем мужчин (8:1).
Лечение тиреотоксикоза — еще одна частая причина гипотиреоза. Нелеченный врожденный гипотиреоз приводит к множественным нарушениям развития, известным как кретинизм.
Преходящий гипотиреоз является по определению единственной обратимой формой гипотиреоза. Частота послеродового тиреоидита, который возникает через 1—6 месяцев после родов достигает 20%.
Жалобы
Проявления всех форм гипотиреоза сходны.
К частым жалобам относятся: грубая кожа, холодная кожа, бледность, редкие волосы (выпадение волос), отек вокруг глаз (периорбитальный отек), низкий голос, зоб, отеки ног (это так называемый слизистый отек — он не оставляет ямок при надавливании).
Более редкие жалобы: замедленная речь, апноэ (остановки дыхания) во сне, низкая температура тела (гипотермия), артериальная гипертония, увеличение языка (макроглоссия), боль в мышцах (миопатия).
Жалобы развиваются постепенно, поэтому гипотиреоз может тянуться годами без диагноза. Поскольку заболевание затрагивает многие системы органов, большинство жалоб неспецифичны. Кроме того, выраженность симптомов не всегда соответствует тяжести заболевания. Даже у больных с лабораторными признаками гипотиреоза жалобы могут отсутствовать. Слабость, сонливость, запоры, сухость кожи, выпадение волос — вот самые частые неспецифические симптомы гипотиреоза. Специфические же признаки гипотиреоза включают зябкость, одутловатость лица, огрубление и снижение тембра голоса.
Поскольку заболевание затрагивает многие системы органов, большинство жалоб неспецифичны. Кроме того, выраженность симптомов не всегда соответствует тяжести заболевания. Даже у больных с лабораторными признаками гипотиреоза жалобы могут отсутствовать. Слабость, сонливость, запоры, сухость кожи, выпадение волос — вот самые частые неспецифические симптомы гипотиреоза. Специфические же признаки гипотиреоза включают зябкость, одутловатость лица, огрубление и снижение тембра голоса.
Некоторые проявления гипотиреоза зависят от возраста. У детей это задержка роста, у женщин детородного возраста — нарушение менструального цикла, у пожилых — деменция. Наиболее характерная черта гипотиреоза — удлинение фазы расслабления сухожильных рефлексов, прежде всего ахиллова (нередко заподозрить гипотиреоз может невролог). Часто наблюдается плевральный или перикардиальный выпот, иногда значительный.
Диагностика
Поскольку у 95% больных гипотиреоз первичный, лучше всего начинать с определения тиреотропного гормона (ТТГ).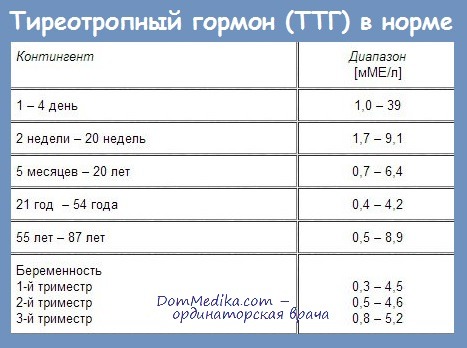 Повышенный уровень ТТГ в крови — самый чувствительный показатель гипотиреоза. Умеренное повышение ТТГ (обычно в пределах 15 мМЕ/л) часто наблюдается на фоне нормального уровня T4; в таких случаях говорят о скрытом гипотиреозе. Единой точки зрения по поводу лечения практически здоровых людей со скрытым гипотиреозом в настоящее время нет.
Повышенный уровень ТТГ в крови — самый чувствительный показатель гипотиреоза. Умеренное повышение ТТГ (обычно в пределах 15 мМЕ/л) часто наблюдается на фоне нормального уровня T4; в таких случаях говорят о скрытом гипотиреозе. Единой точки зрения по поводу лечения практически здоровых людей со скрытым гипотиреозом в настоящее время нет.
Поскольку главный признак гипотиреоза — снижение уровней тиреоидных гормонов, показано измерение уровня T4. Измерение общего T3 в диагностике гипотиреоза малочувствительно и почти никогда не применяется. В подавляющем большинстве случаев диагноз гипотиреоза может быть установлен по клинической картине, T4 и ТТГ. Определение антитиреоидных антител помогает установить причину гипотиреоза, а также выявить лиц, у которых повышен риск перехода скрытого гипотиреоза в клинически выраженный. Сцинтиграфия щитовидной железы почти никогда не нужна. Ее используют лишь для подтверждения аномалий развития щитовидной железы и исследования узлового зоба.
Лечение
Синтетический T4 — левотироксин (L-тироксин, Эутирокс) — основной препарат в лечении гипотиреоза. Содержание левотироксина в препаратах разных фирм стандартизовано, однако опыт говорит о том, что пациент должен пользоваться одним и тем же препаратом (в связи с небольшими различиями в содержании действующего вещества в препаратах разных изготовителей). Обычная замещающая доза составляет 75—150 мкг в день. Правильность подбора дозы контролируют по уровню ТТГ. После изменения дозы препарата новое стационарное состояние устанавливается не раньше чем через 4—6 недель. До этого времени измерять ТТГ не имеет смысла. Цель заместительной терапии левотироксином — достичь нормального уровня ТТГ, поскольку передозировка левотироксина и, следовательно, падение уровня ТТГ ниже нормы приводят к снижению плотности костей. Когда достигнут нормальный уровень ТТГ, для оценки правильности заместительной терапии левотироксином достаточно определять ТТГ каждые 6—12 месяцев.
№AN56TSH, ТТГ собак (тиреотропный гормон): показатели, норма
Секреция ТТГ (тиреотропина) регулируется гипоталамо-гипофизарно-тиреоидной системой. Тиреотропин-рилизинг-фактор (ТРФ) гипоталамуса стимулирует высвобождение ТТГ из гипофиза, который, в свою очередь, стимулирует синтез и выход Т4 из щитовидной железы. Синтез и высвобождение ТРФ гипоталамусом контролируются с помощью малоизученных импульсов, проходящих по нервным путям от высших мозговых центров.
Тиреотропин-рилизинг-фактор (ТРФ) гипоталамуса стимулирует высвобождение ТТГ из гипофиза, который, в свою очередь, стимулирует синтез и выход Т4 из щитовидной железы. Синтез и высвобождение ТРФ гипоталамусом контролируются с помощью малоизученных импульсов, проходящих по нервным путям от высших мозговых центров.Тиреотропный гормон повышает синтез и секрецию как Т4, так и Т3, и является основным регулятором концентрации гормонов щитовидной железы. Секреция ТТГ гипофизом модулируется гормонами щитовидной железы по механизму отрицательной обратной связи. В гипофизе, главным образом под действием T3, который образуется локально путем монодейодирования тироксина, происходит подавление секреции ТТГ. Только свободные или несвязанные (с белками плазмы) формы гормонов щитовидной железы проникают в клетки и реализуют свою биологическую функцию или регулируют секрецию ТТГ гипофизом.
Ауторегуляторные механизмы в щитовидной железе контролируют поглощение йода и синтез гормонов путем изменения чувствительности к стимуляции ТТГ, а также путем повышения секреции Т3 относительно синтеза Т4 в период дефицита йода.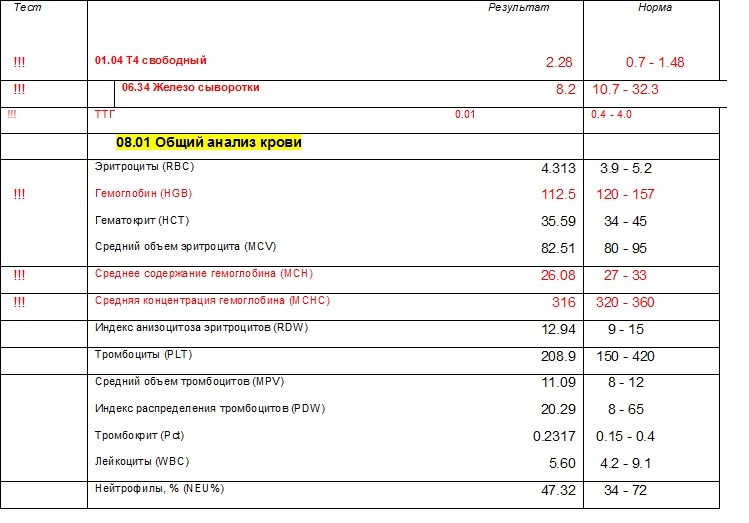 Находясь под влиянием мелатонина (гормона эпифиза), секреция ТТГ гипофизом имеет суточную периодичность, которая достигает наибольшей активности в середине ночи и наименьшей активности к началу вечера.
Находясь под влиянием мелатонина (гормона эпифиза), секреция ТТГ гипофизом имеет суточную периодичность, которая достигает наибольшей активности в середине ночи и наименьшей активности к началу вечера.
Первичный гипотиреоз собак вызван либо разрушением ткани щитовидной железы в результате развития аутоиммунного тиреоидита, либо идиопатической атрофией щитовидной железы. Эти расстройства характеризуются снижением выработки гормонов тканью щитовидной железы с дальнейшим снижением ингибирования механизма отрицательной обратной связи. В ответ на потребность организма в тиреоидных гормонах в гипофизе повышается секреция ТТГ, эффективность влияния которого снижена в связи с дисфункцией или атрофией ткани щитовидной железы. Таким образом, первичный гипотиреоз характеризуется повышенным уровнем ТТГ и снижением уровня Т4 в крови и/или уровня свободного Т4. К сожалению, не у всех собак с первичным гипотиреозом отмечается повышение уровня ТТГ, что объясняется пульсирующей секрецией ТТГ и эпизодическими повышениями значений в пределах референсного интервала.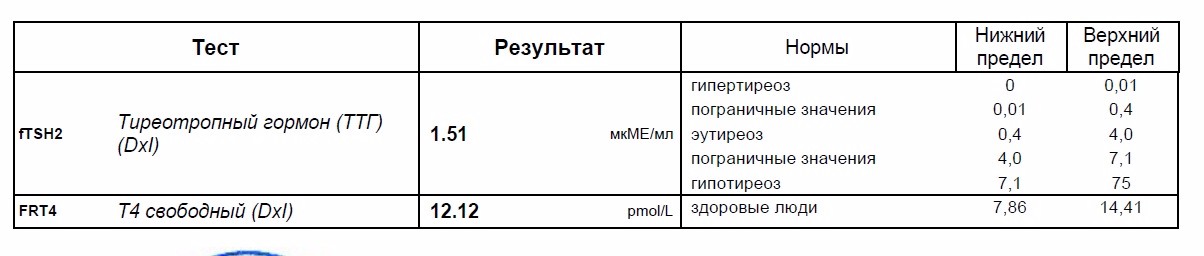 Возможно также, что существующий метод анализа может «пропустить» некоторые гликозилированные формы ТТГ, что приводит к ложноотрицательным результатам. И, наконец, хронический первичный гипотиреоз может привести к «истощению» продукции ТТГ гипофизом.
Возможно также, что существующий метод анализа может «пропустить» некоторые гликозилированные формы ТТГ, что приводит к ложноотрицательным результатам. И, наконец, хронический первичный гипотиреоз может привести к «истощению» продукции ТТГ гипофизом.
Вторичный гипотиреоз обусловлен снижением продукции ТТГ гипофизом. При этом прямого повреждения фолликулярных клеток щитовидной железы не происходит, а атрофия щитовидной железы может быть результатом отсутствия стимуляции со стороны ТТГ. Это расстройство характеризуется низким уровнем в крови T4, свободного T4, с сохранением ТТГ в пределах референсных значений. Дисфункции гипофиза постоянного характера (пороки развития гипофиза или травма) является редкой причиной развития вторичного гипотиреоза.
Определение ТТГ — видоспецифичный тест, который в настоящее время доступен для определения содержание этого гормона только у собак.
ПРЕАНАЛИТИКА
Перед проведением исследования животные должны находиться на голодной диете не менее 12 часов. Стабильность ТТГ в сыворотке крови составляет семь дней при температуре хранения +2С…+8С, два месяца при температуре хранения -17С…-23С (при условии соблюдения преаналитических требований по взятию биоматериала на гормональные исследования).
Стабильность ТТГ в сыворотке крови составляет семь дней при температуре хранения +2С…+8С, два месяца при температуре хранения -17С…-23С (при условии соблюдения преаналитических требований по взятию биоматериала на гормональные исследования).
ИНТЕРПРЕТАЦИЯ
Результаты исследования содержат информацию исключительно для врачей. Диагноз ставится на основании комплексной оценки различных показателей и дополнительных сведений.
Единицы измерения: нг/мл.
Референсные значения:
менее 0,45 нг/мл.
Сульфаниламидные препараты могут ингибировать продукцию гормонов щитовидной железы, что может имитировать первичный гипотиреоз как в проявлениях клинической картины, так и по результатам лабораторных показателей.
Глюкокортикоиды (эндогенные или экзогенные) и фенобарбитал могут подавлять продукцию ТТГ. Таким образом, некоторые заболевания, не связанные напрямую с болезнями щитовидной железы, подавляют высвобождение ТТГ гипофизом и, возможно, ингибируют высвобождение ТРГ из гипоталамуса, что приводит к схожести значений лабораторных показателей, подобно таковым при вторичном гипотиреозе.
Повышение уровня:
Первичный гипотиреоидизм.
Лечение сульфаниламидными препаратами.
Опухоль гипофиза.
Понижение уровня (в пределах РЗ):
Вторичный гипотиреоидизм.
Действие кортикостероидов (эндогенных, экзогенных) и фенобарбитала.
Гиперадренокортицизм.
Первичный гипотиреоз с ложноотрицательным результатом.
ТТГ — тиреотропный гормон — ОВУМ – медицинская лаборатория в Кемерοво
Описание
Тиреотропный гормон (ТТГ) вырабатывается в передней доле гипофиза.
ТТГ влияет на структуру и регулирует работу щитовидной железы (ЩЖ). ТТГ стимулирует увеличение числа и размеров клеток ЩЖ, образование гормонов щитовидной железы — тиреоидных гормонов: тироксина (Т4) и трийодтиронина (Т3).
Выделение ТТГ регулируется стимулирующими (с помощью тиреотропин-рилизинг гормона – ТРГ) или подавляющими влияниями гормонов гипоталамуса. Также секреция ТТГ регулируется тиреоидными гормонами по принципу отрицательной обратной связи: высокие концентрации гормонов Т4 и Т3 тормозят секрецию ТРГ гипоталамусом и ТТГ гипофизом, а низкие уровни – стимулируют.
Также секреция ТТГ регулируется тиреоидными гормонами по принципу отрицательной обратной связи: высокие концентрации гормонов Т4 и Т3 тормозят секрецию ТРГ гипоталамусом и ТТГ гипофизом, а низкие уровни – стимулируют.
ТТГ секретируется в импульсном режиме и имеет суточный ритм с максимум в 0-4 часа, минимальные значения регистрируются в 17-18 часов.
Содержание ТТГ и тиреоидных гормонов отличается в разные возрастные периоды, поэтому их уровень оценивают в соответствии с нормами для определенного возраста.
Для чего проводится анализ ТТГ
С помощью исследования ТТГ определяют, есть или нет нарушения в работе щитовидной железы.
Так как проявления заболеваний щитовидной железы очень индивидуальны, имеют разную степень выраженности, часто протекают без характерных проявлений или бессимптомно, очень важно своевременно провести лабораторное обследование.
Состояние, когда в организме существует недостаток гормонов щитовидной железы, называется гипотиреоз, если происходит избыточная продукция гормонов щитовидной железы – гипертиреоз, нормальная функция щитовидной железы обозначается – эутиреоз.
Одновременно проведенные исследования ТТГ и тиреоидных гормонов определяют уровень нарушений: поражение самой ЩЖ, нарушения в работе гипофиза или гипоталамуса.
Как оценивают функцию щитовидной железы
Существует 3 уровня лабораторного обследования для диагностики состояния ЩЖ:
- 1 уровень – скрининг. Проводится определение уровня ТТГ.
Исследование позволяет исключить гипо- или гипертиреоз, даже в случае, если у человека нет признаков заболеваний ЩЖ.
- 2 уровень – диагностика. Определяется ТТГ и свободный Т4.
Эти исследования проводятся, если есть подозрение на патологию ЩЖ (признаки заболевания, жалобы, отклонения в результатах биохимических анализов, изменения при проведении УЗИ ЩЖ).
Эти тесты определяют уровень нарушения функции ЩЖ и оценивают её тяжесть.
Схема обследования функции ЩЖ
- 3 уровень – выяснение причины заболевания ЩЖ.
Определяют свободный Т3, уровни антител к структурам ЩЖ (к тиреоидной пероксидазе, тиреоглобулину, рецепторам ТТГ), тиреоглобулин, кальцитонин.
Когда нужно сдать анализ на ТТГ
Анализ назначается лечащим врачом в случае самых разнообразных причин:
- профилактически, чтобы исключить нарушения в работе ЩЖ,
- скрининг при беременности,
- при бесплодии, чтобы исключить изменения функции ЩЖ,
- чтобы установить причину и выраженность заболевания, если есть признаки нарушения функции ЩЖ,
- для контроля за проводимым лечением по поводу заболеваний ЩЖ.
Почему может быть «несоответствие» между лабораторными показателями
Трактовку результата исследования гормонов проводит врач эндокринолог, с учетом всех данных о состоянии здоровья пациента, принимаемых им лекарственных веществах.
Так, при лечении заболеваний ЩЖ быстро приходят в норму Т4 и Т3, а нормализация уровня ТТГ запаздывает из-за инерции в работе системы гипоталамус — гипофиз — ЩЖ. Кратность лабораторных исследований на фоне лечения определяется лечащим врачом.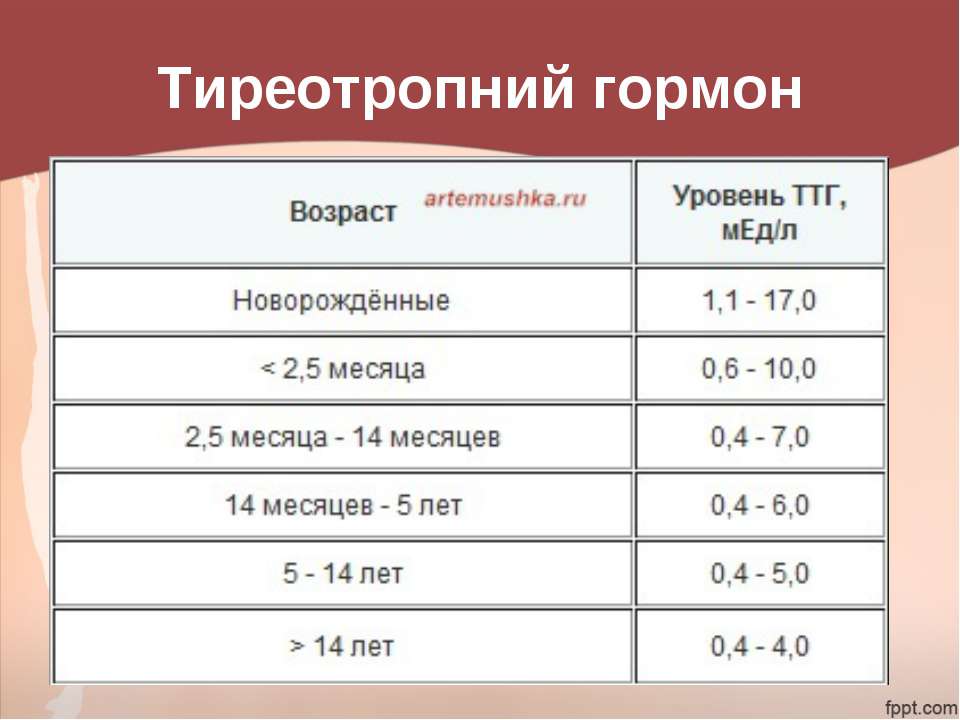
На изменения уровней гормонов ЩЖ может влиять ряд состояний, например голодание, стресс, холод, тяжелые физические нагрузки и другие.
Уровни гормонов изменяются во время беременности, так как весь обмен веществ в организме перестраивается для обеспечения возрастающих потребностей развивающегося плода. В зависимости от срока беременности нормы содержания в крови гормонов изменяются. Результаты обследования беременной женщины обязательно должен трактовать врач эндокринолог.
При острых и хронических заболеваниях, приеме ряда лекарств или биодобавок нарушается периферическое превращение Т4 в Т3, связывание гормонов с белками, выведение гормонов, подавляется секреция ТТГ. В этих случаях следует повторить исследования в динамике, чтобы исключить патологию ЩЖ.
Правила подготовки
Сдать анализ крови ТТГ (тиреотропный гормон) в лаборатории Медицинские анализы, цены в лаборатории KDL
ТТГ- тиреотропный гормон. Гормон гипофиза, регулирующий функцию щитовидной железы. Используется для скрининга и диагностики различных нарушений функции щитовидной железы: гипотиреоза (сниженной функции) и гипертиреоза (повышенной функции).
Гормон гипофиза, регулирующий функцию щитовидной железы. Используется для скрининга и диагностики различных нарушений функции щитовидной железы: гипотиреоза (сниженной функции) и гипертиреоза (повышенной функции).
Синтез и секреция ТТГ стимулируются тиролиберином, пептидом гипоталамуса, который вырабатывается при низком уровне гормонов щитовидной железы в кровотоке. Повышенные уровни T3 и T4 подавляют секрецию ТТГ по классическому механизму с отрицательной обратной связью.
В каких случаях обычно назначают исследование уровня ТТГ?
Чаще всего это исследование назначается при наличии симптомом измененной функции щитовидной железы (гипер- или гипотиреозе), при выявлении изменений щитовидной железы на УЗИ, для контроля лечения при приеме гормональных препаратов.
Анализ на ТТГ у женщин обязательно назначают во время беременности.
Что именно определяется в процессе анализа?
Тиреотропный гормон состоит из двух субъединиц: альфа и бета. Альфа единица гормона сходна с аналогичными субъединицами ЛГ, ФСГ и ХГЧ. Бета- единица ТТГ существенно отличается. Используемая тест- система выявляет наличие гормона ТТГ в крови методом хемилюминесцентного иммуноанализа на микрочастицах.
Бета- единица ТТГ существенно отличается. Используемая тест- система выявляет наличие гормона ТТГ в крови методом хемилюминесцентного иммуноанализа на микрочастицах.
Что означают результаты теста?
Сниженный уровень ТТГ чаще всего наблюдается при гипертиреозе. Болезнь Грейвса (диффузный токсический зоб) является наиболее распространенной причиной гипертиреоза. Это хроническое аутоиммунное расстройство, в результате которого происходит избыточная выработка гормонов щитовидной железы. В результате чего у пациентов могут отмечаться симптомы, связанные с гипертиреозом, такие как сердцебиение, потеря веса, нервозность, дрожание рук, покраснение и раздражение глаз, трудности с засыпанием. В ответ на высокий уровень Т3 и Т4 гипофиз вырабатывает меньше ТТГ, что приводит к его низкому уровню в крови.
Если наблюдается снижение уровня тиреоидных гормонов щитовидной железы (гипотиреоз), у человека могут наблюдаться такие симптомы, как увеличение веса, сухость кожи, регулярные запоры, усталость, плохая переносимость холода. Тиреоидит Хашимото чаще всего становится причиной гипотиреоза. Это хроническое аутоиммунное состояние, при котором иммунная система атакует клетки щитовидной железы, вызывая воспаление, в результате чего щитовидная железа вырабатывает недостаточно гормонов. По принципу обратной связи гипофиз начинает производить больше ТТГ, что проявляется его повышенным уровнем в крови.
Тиреоидит Хашимото чаще всего становится причиной гипотиреоза. Это хроническое аутоиммунное состояние, при котором иммунная система атакует клетки щитовидной железы, вызывая воспаление, в результате чего щитовидная железа вырабатывает недостаточно гормонов. По принципу обратной связи гипофиз начинает производить больше ТТГ, что проявляется его повышенным уровнем в крови.
В редких случаях изменение уровня ТТГ в крови связано с дисфункцией гипофиза или гипоталамуса.
Обычный срок выполнения теста
Обычно результат анализа на ТТГ можно получить в течение 1-2 дней
Нужна ли специальная подготовка к анализу?
Специальная подготовка не требуется. Подробнее про условия сдачи можно прочитать в разделе «Подготовка». При мониторинге лечения анализ на ТТГ нужно сдавать в сходных условиях: в одно и то же время суток.
Анализ на тиреотропный гормон (ТТГ)
Диагностическое направление
Оценка состояния щитовидной железы
Общая характеристика
Тиреотропный гормон (ТТГ) — гликопротеид, вырабатывается передней долей гипофиза. Является основным регулятором функции щитовидной железы. Контролируется тиреотропин–рилизинг гормоном гипоталамуса и тиреоидными гормонами.Тиреотропный гормон оказывает стимулирующее влияние на щитовидную железу, приводящее к увеличению синтеза трийодтиронина и тироксина.
Является основным регулятором функции щитовидной железы. Контролируется тиреотропин–рилизинг гормоном гипоталамуса и тиреоидными гормонами.Тиреотропный гормон оказывает стимулирующее влияние на щитовидную железу, приводящее к увеличению синтеза трийодтиронина и тироксина.Показания для назначения
1. Оценка функции щитовидной железы (скрининговое исследование). 2. Контроль эффективности тиреостатической терапии при тиреотоксикозе.3. Контроль эффективности супрессивной терапии при узловом зобе, раке щитовидной железы. 4. Контроль эффективности заместительной терапии первичного и послеоперационного гипотиреоза. 5. Оценка реакции при введении тиреотропин-рилизинг гормона.6. Дифференциальная диагностика причин нарушений менструального цикла, бесплодия, невынашивания, гирсутизма.7. Галакторея и повышение уровня пролактина (как следствие гипотиреоза).8. Дифференциальная диагностика нарушений полового развития.9. Задержка физического и психического развития у детей. 10. Диагностика причин нарушений ритма, гипертензии.11. Мониторинг назначения фармакологических доз йода (амиодарон, рентгеноконтрастные средства, содержащие йод).12. Алопеция.
10. Диагностика причин нарушений ритма, гипертензии.11. Мониторинг назначения фармакологических доз йода (амиодарон, рентгеноконтрастные средства, содержащие йод).12. Алопеция.
Маркер
Маркер функционального состояния гипофиза и щитовидной железы.
Клиническая значимость
1. Диагностика гипо- и гипертиреоза.2. Мониторинг терапии у пациентов с патологией щитовидной железы.
Состав показателей:
Тиреотропный гормон
Метод: Хемилюминесцентный иммуноанализДиапазон измерений: 0,008-3000,0
Единица измерения: Микроединиц на миллилитр
Референтные значения:
Возраст
Комментарии
Выполнение возможно на биоматериалах:
Биологический материал
Условия доставки
Контейнер
Объем
Сыворотка
Условия доставки:
24 Час. при температуре от 2 до 25 градусов Цельсия
при температуре от 2 до 25 градусов Цельсия
Контейнер:
Вакутейнер с разделительным гелем
Объем:
8.5 Миллилитров
Капиллярная кровь
Условия доставки:
24 Час. при температуре от 2 до 25 градусов Цельсия
при температуре от 2 до 25 градусов Цельсия
Контейнер:
Микровет с активатором свертывания крови
Объем:
500 Микролитр
Правила подготовки пациента
Стандартные условия: Утром до 11-00, натощак, через 8-12 часов периода голодания. Важно: Если накануне исследования проводилась процедура ангиографии, время забора крови на исследование согласовать с лечащим врачом (при применении контраста «Флуоресцеин» кровь для исследования ТТГ сдавать спустя 72 часа после введения контраста (интерференция между применением контраста и уровнем ТТГ — ложно-заниженные результаты (менее 0,01 мл МЕ/л).Возможно: В течение рабочего дня отделений МЛ «ДІЛА». Перерыв не менее 6 часов после приема пищи (должна быть исключена жирная пища).
Важно: Если накануне исследования проводилась процедура ангиографии, время забора крови на исследование согласовать с лечащим врачом (при применении контраста «Флуоресцеин» кровь для исследования ТТГ сдавать спустя 72 часа после введения контраста (интерференция между применением контраста и уровнем ТТГ — ложно-заниженные результаты (менее 0,01 мл МЕ/л).Возможно: В течение рабочего дня отделений МЛ «ДІЛА». Перерыв не менее 6 часов после приема пищи (должна быть исключена жирная пища).
Вы можете добавить данное исследование в корзину на этой странице
Интерференция:
- Амиодарон, бензеразид, галоперидол, литий, анальгин, бета-адреноблокаторы (атенолол, метопролол, пропранолол), кальцитонин, метоклопрамид, ловастатин, метимазол, морфин, фенотиазины, рифампицин, 131I (йод), физическая нагрузка.

- Бромкриптин, карбамазепин, кортикостероиды, допамин, гепарин (в/в введение), леводопа, фентоламин, соматостатин, октреотид, тироксин, трийодтиронин, йодиды, бета-адреномиметики, наличие аутоантител к ТТГ. Интерференция между применением контраста для ангиографии флуоресцеина и величинами определяемых в образцах крови тиреотропного гормона в случае, если забор этих образцов произошел в период времени до 72 часов после введения контраста. В образцах крови, содержащих остаточные количества флуоресцеина, могут наблюдаться ложно-заниженные результаты ТТГ (менее 0,01 мл МЕ/л), что актуально в процессе мониторинга за пациентами, прооперированными по поводу рака щитовидной железы и получающими супрессивные дозы тироксина.
Интерпретация:
- Первичный гипотиреоз, ТТГ-секретирующая опухоль гипофиза, эктопическая секреция ТТГ (опухоли легкого, молочной железы), резистентность к гормонам щитовидной железы, тяжелые соматические и психические заболевания, гестоз, гемодиализ, физические нагрузки.

- Первичный гипертиреоз, вторичный гипотиреоз, субклинический гипертиреоз, автономная секреция гормонов щитовидной железы, экзогенная терапия гормонами щитовидной железы, тяжелые общие заболевания в пожилом возрасте, голодание, психологический стресс.
признаки, разбор анализов и лечения
Гипотиреоз вызывается снижением уровня гормонов щитовидной железы: Т (тироксина) 3, Т4, ТТГ (тиреотропина). Обычно его развитие провоцируется аутоиммунным тиреоидитом – воспалительным процессом тканей железы, при котором собственная иммунная система разрушает ткани щитовидки. Чаще всего гипотиреоз выявляется у женщин.
Какие симптомы указывают на развитие гипотиреоза?
Функции гормонов щитовидной железы крайне важны для организма. На их недостаток указывают следующие признаки:
-
Повышенная утомляемость, снижение толерантности к нагрузкам, сонливость.
 Обычно пациенты с гипотиреозом говорят так: «Сразу после пробуждения мне хочется снова лечь спать».
Обычно пациенты с гипотиреозом говорят так: «Сразу после пробуждения мне хочется снова лечь спать».
-
Сухость кожных покровов и волос.
-
Ухудшение памяти, заторможенность, депрессия.
-
Одышка.
-
Выпадение и ломкость волос, значительное прорежение бровей.
-
Сниженное потоотделение.
-
Зябкость и понижение температуры тела.
-
Склонность к запорам и нарушениям работы желчного пузыря.
-
Повышенный уровень холестерина в крови.
-
Отечность лица и языка (на нем видны следы от зубов).
-
Снижение либидо.
-
Нарушения менструального цикла (ановуляторные циклы) и бесплодие у женщин.

-
Нарушения эрекции у мужчин.
Степень выраженности симптомов гипотиреоза зависит от степени снижения уровня Т3 и Т4.
Иногда женщины могут впервые столкнуться с гипотиреозом именно во время беременности. Эта патология негативно отражается на самочувствии матери и может привести к аномальному развитию плода, отслойке плаценты, внутриутробной гибели плода, выкидышу, послеродовому кровотечению, умственной отсталости будущего ребенка.
Диагностика
Для подтверждения диагноза «гипотиреоз» пациенту могут назначаться следующие виды исследований:
В норме показатели ТТГ составляют 0, 4 – 4, 0 мЕД/л. Женщинам, планирующим зачатие и беременным, рекомендуется чтобы показатель ТТГ приближался к верхнему референсному значению – 2, 5 м ЕД/л. Уровень Т4 св у женщин в первом триместре должен приближаться к значениям 11, 5 – 28, 8 пмоль/л.
Лечение
Заниматься самолечение гипотиреоза нельзя! Только врач-эндокринолог может составить правильную тактику терапии. В случае недостатка йода в организме пациенту могут назначаться препараты йода. При невозможности выработки достаточного уровня тиреоидных гормонов рекомендуется заместительная гормонотерапия. Выбор лекарств и их дозирование должен осуществлять только врач!
Обращение к врачам-эндокринологам сети медицинских центров 100med поможет вам выявить существующую проблему в работе щитовидной железы и пройти адекватный курс лечения. В наших клиниках созданы все условия для проведения качественной диагностики и лечения данной патологии.
Повышенный уровень потери при беременности у женщин с отрицательными антителами к щитовидной железе с уровнем ТТГ от 2,5 до 5,0 в первом триместре беременности | Журнал клинической эндокринологии и метаболизма
Контекст: Определение нормального ТТГ во время беременности постоянно меняется. Недавние исследования показали, что верхний предел нормы ТТГ в первом триместре должен составлять 2,5 мМЕ / литр.
Недавние исследования показали, что верхний предел нормы ТТГ в первом триместре должен составлять 2,5 мМЕ / литр.
Цель: Целью исследования было оценить потерю беременности и частоту преждевременных родов у женщин с отрицательными антителами к тироидной пероксидазе в первом триместре со значениями ТТГ между 2.5 и 5,0 мМЕ / л.
Дизайн: Настоящее исследование является составной частью недавно опубликованного крупномасштабного проспективного исследования, в котором оценивалось влияние лечения левотироксином на материнские и неонатальные осложнения у женщин с положительной реакцией на тироидную пероксидазу с уровнем ТТГ выше 2,5 мМЕ / литр. В настоящем исследовании оценивали 4123 женщин с отрицательными антителами к тироидной пероксидазе с уровнем ТТГ не более 5,0 мМЕ / л. Женщины были разделены на две группы в зависимости от их исходного ТТГ: группа А, уровень ТТГ ниже 2.5 мМЕ / литр, за исключением женщин с гипертиреозом, определяемых как неопределяемый ТТГ с повышенным свободным Т 4 , и группа B, уровень ТТГ между 2,5 и 5,0 мМЕ / литр.
Окружение: Исследование проводилось в двух амбулаторных клиниках общественных больниц на юге Италии.
Пациенты: Всего обследовано 4123 женщины.
Вмешательство: Вмешательства не было.
Основные показатели результатов: Измерялась частота невынашивания беременности и преждевременных родов в группе А по сравнению с группой В.
Результаты: Частота невынашивания беременности была значительно выше в группе B по сравнению с группой A (6,1 против 3,6% соответственно, P = 0,006). Не было разницы в частоте преждевременных родов между двумя группами.
Выводы: Увеличение частоты прерывания беременности у беременных с уровнем ТТГ от 2,5 до 5,0 мМЕ / литр дает убедительные физиологические доказательства в поддержку пересмотра верхнего предела нормы ТТГ в первом триместре до 2.5 мМЕ / литр.
Определение нормального ТТГ во время беременности меняется. В то время как значения ТТГ 4,0–5,0 мМЕ / литр когда-то считались нормальными, сейчас все больше сходится во мнении, что значения в первом триместре выше 2,5 мМЕ / литр и значения во втором и третьем триместре, превышающие 3,0 мМЕ / литр, находятся за пределами нормального диапазона. Это изменение отражено в рекомендациях Общества эндокринологов по щитовидной железе и беременности 2007 года, в которых рекомендуется, чтобы значения ТТГ у беременных, получающих терапию левотироксином, были менее 2.5 в первом триместре и менее 3,0 мМЕ / л в последующих триместрах (1). Снижение верхнего диапазона ТТГ во время беременности, и особенно в первом триместре, вызвано повышением уровня хорионического гонадотропина человека, который перекрестно реагирует на рецептор ТТГ и вызывает сопутствующее снижение уровней ТТГ в первом триместре (2). .
В то время как значения ТТГ 4,0–5,0 мМЕ / литр когда-то считались нормальными, сейчас все больше сходится во мнении, что значения в первом триместре выше 2,5 мМЕ / литр и значения во втором и третьем триместре, превышающие 3,0 мМЕ / литр, находятся за пределами нормального диапазона. Это изменение отражено в рекомендациях Общества эндокринологов по щитовидной железе и беременности 2007 года, в которых рекомендуется, чтобы значения ТТГ у беременных, получающих терапию левотироксином, были менее 2.5 в первом триместре и менее 3,0 мМЕ / л в последующих триместрах (1). Снижение верхнего диапазона ТТГ во время беременности, и особенно в первом триместре, вызвано повышением уровня хорионического гонадотропина человека, который перекрестно реагирует на рецептор ТТГ и вызывает сопутствующее снижение уровней ТТГ в первом триместре (2). .
Надежные нормативные данные подтверждают пересмотренный диапазон норм ТТГ во время беременности, хотя точный верхний предел нормы незначительно варьируется между исследованиями. Чрезвычайно важно определить клинические последствия, начиная с потери беременности и преждевременных родов, нелеченного ТТГ в первом триместре в диапазоне, который ранее считался нормальным. Для целей настоящего исследования, основанного на Руководстве эндокринного общества (1) и недавно опубликованных нормативных данных (3–6), мы решили оценить влияние уровней ТТГ от 2,5 до 5,0 мМЕ / л.
Чрезвычайно важно определить клинические последствия, начиная с потери беременности и преждевременных родов, нелеченного ТТГ в первом триместре в диапазоне, который ранее считался нормальным. Для целей настоящего исследования, основанного на Руководстве эндокринного общества (1) и недавно опубликованных нормативных данных (3–6), мы решили оценить влияние уровней ТТГ от 2,5 до 5,0 мМЕ / л.
Предыдущее исследование продемонстрировало повышенную частоту самопроизвольного прерывания беременности у женщин с явным материнским гипотиреозом (7).Однако данные о субклиническом гипотиреозе (определяемом как ТТГ ≥ 5,0 мМЕ / литр) и выкидышах противоречат некоторым, но не всем исследованиям, показывающим повышенную частоту невынашивания беременности (8, 9). С преждевременными родами связаны как явный, так и субклинический гипотиреоз (10). Кейси и др. (11) в проспективном исследовании 17 298 техасских женщин сообщили, что у женщин с уровнем ТТГ до 20 недель беременности, превышающим перцентиль 97,5, частота преждевременных родов выше, чем у контрольной эутиреоидной (4. 0 против 2,5%, P <0,05). Антитела к щитовидной железе не были обнаружены в исследовании Casey et al . Стагнаро-Грин и др. (12) обнаружил повышенную частоту очень преждевременных родов (до 32 недель беременности), но не преждевременных родов, у женщин с уровнем ТТГ выше 3,0. Ни в одном исследовании не был указан максимальный уровень ТТГ.
0 против 2,5%, P <0,05). Антитела к щитовидной железе не были обнаружены в исследовании Casey et al . Стагнаро-Грин и др. (12) обнаружил повышенную частоту очень преждевременных родов (до 32 недель беременности), но не преждевременных родов, у женщин с уровнем ТТГ выше 3,0. Ни в одном исследовании не был указан максимальный уровень ТТГ.
Насколько нам известно, настоящее исследование является первым, в котором оценивается взаимосвязь между спонтанной потерей беременности, преждевременными родами и значениями ТТГ в первом триместре между 2.5 и 5,0 мМЕ / л. Было продемонстрировано, что у эутиреоидных женщин с положительной реакцией на тиреоидные антитела в первом триместре повышается как частота выкидышей (13, 14), так и частота преждевременных родов (15). Следовательно, чтобы удалить этот смешивающий фактор, женщины с положительным результатом на антитела были исключены из настоящего исследования.
Объекты и методы
Настоящее исследование является составной частью проспективного исследования 4657 женщин, прошедших скрининг на ТТГ и антитела к тироидной пероксидазе в течение первых 11 недель беременности в южной Италии (16). Критерии отбора включали отсутствие в анамнезе заболеваний щитовидной железы и спонтанной одноплодной беременности. Женщин случайным образом распределили в группу универсального скрининга или группу по выявлению случаев заболевания и разделили на группы высокого или низкого риска заболевания щитовидной железы. Всем женщинам в группе универсального скрининга (как с высоким, так и с низким риском) и женщинам с высоким риском в группе выявления случаев незамедлительно проводились исследования антител к ТТГ и тироидной пероксидазе. У женщин из группы выявления случаев после родов анализировали сыворотку крови.Во время беременности антителопозитивные женщины с ТТГ выше 2,5 мМЕ / л получали левотироксин. Женщины с пониженным уровнем ТТГ и повышенным свободным T 4 были классифицированы как гипертиреоидные и направлены к эндокринологу. Оценивались материнские и неонатальные исходы.
Критерии отбора включали отсутствие в анамнезе заболеваний щитовидной железы и спонтанной одноплодной беременности. Женщин случайным образом распределили в группу универсального скрининга или группу по выявлению случаев заболевания и разделили на группы высокого или низкого риска заболевания щитовидной железы. Всем женщинам в группе универсального скрининга (как с высоким, так и с низким риском) и женщинам с высоким риском в группе выявления случаев незамедлительно проводились исследования антител к ТТГ и тироидной пероксидазе. У женщин из группы выявления случаев после родов анализировали сыворотку крови.Во время беременности антителопозитивные женщины с ТТГ выше 2,5 мМЕ / л получали левотироксин. Женщины с пониженным уровнем ТТГ и повышенным свободным T 4 были классифицированы как гипертиреоидные и направлены к эндокринологу. Оценивались материнские и неонатальные исходы.
В настоящем исследовании оценивались все женщины, участвовавшие в исследовании, у которых были отрицательные антитела к щитовидной железе, не классифицированные как гипертиреоид, и у которых ТТГ составлял 5,0 мМЕ / литр или ниже. Ни одна из этих женщин не получала лечения во время беременности.Были сформированы две группы женщин: группа А имела ТТГ менее 2,5 мМЕ / л и была классифицирована как эутиреоидная; группа B имела ТТГ от 2,5 до 5,0 мМЕ / л и была классифицирована как субклинический гипотиреоз. Переменной результата исследования был процент невынашивания беременности (включая выкидыш до 20 недель и мертворождение после 20 недель), преждевременных родов (34–37 недель) и очень преждевременных родов (<34 недель) в каждой группе. Статистический анализ проводился с использованием точного критерия Фишера.
Ни одна из этих женщин не получала лечения во время беременности.Были сформированы две группы женщин: группа А имела ТТГ менее 2,5 мМЕ / л и была классифицирована как эутиреоидная; группа B имела ТТГ от 2,5 до 5,0 мМЕ / л и была классифицирована как субклинический гипотиреоз. Переменной результата исследования был процент невынашивания беременности (включая выкидыш до 20 недель и мертворождение после 20 недель), преждевременных родов (34–37 недель) и очень преждевременных родов (<34 недель) в каждой группе. Статистический анализ проводился с использованием точного критерия Фишера.
Результаты
Четыре тысячи сто двадцать три женщины не имели антител к щитовидной железе, имели ТТГ 5.0 мМЕ / литр или ниже, и не было гипертиреоза. В общей сложности 84,4% женщин были в группе А (n = 3481) и 15,6% женщин были в группе B (n = 642). В таблице 1 представлены возраст, предыдущий акушерский анамнез, клинические данные и тесты функции щитовидной железы в группах A и B. В соответствии с планом исследования средний уровень ТТГ в группе A значительно ниже, чем в группе B (0,82 против 3,14 мМЕ / литр, Манна-Уитни U = 0, P <0,001). Средние уровни свободного T 4 были выше в группе A по сравнению с группа B (12,2 против 10,6, P <0,01). У женщин из группы А вероятность наличия в семейном анамнезе заболеваний щитовидной железы несколько выше. Разницы в средней гестационной неделе первого визита между группами не было.
В соответствии с планом исследования средний уровень ТТГ в группе A значительно ниже, чем в группе B (0,82 против 3,14 мМЕ / литр, Манна-Уитни U = 0, P <0,001). Средние уровни свободного T 4 были выше в группе A по сравнению с группа B (12,2 против 10,6, P <0,01). У женщин из группы А вероятность наличия в семейном анамнезе заболеваний щитовидной железы несколько выше. Разницы в средней гестационной неделе первого визита между группами не было.
Клиническая характеристика пациентов по группам
| . | Группа A ТТГ <2,5 (n = 3481) . | Группа B 2,5 ≤ ТТГ ≤ 5,0 (n = 642) . |
|---|---|---|
| Возраст (лет) | 28,7 ± 5 | 29,2 ± 5 |
| Раньше младенцы (%) | 2447 (70,3%) | 458 (71,3%) |
| Курение (%) ) | 185 (5,3%) | 38 (5,9%) |
Первое гинекологическое посещение (нед. ) ) | 8,8 ± 1,6 | 8,9 ± 1,5 |
| ТТГ в первом триместре (мМЕ / л), медиана ( межквартильный размах) a | 0.82 (0,36–1,40) | 3,14 (2,79–3,44) |
| Бесплатно T 4 первый триместр (пмоль / литр) a | 12,2 ± 2,1 | 10,6 ± 2,2 |
| Семейный анамнез заболевание щитовидной железы (%) b | 443 (12,7%) | 64 (10%) |
| Зоб (%) | 29 (0,8%) | 4 (0,6%) |
| Симптомы гипо- / гипертиреоз (%) | 267 (7,7%) | 45 (7%) |
| Сахарный диабет 1 типа / аутоиммунное заболевание (%) | 34 (1%) | 6 (0.9%) |
| Облучение (%) | 1 (0,03%) | 1 (0,1%) |
| Предыдущий выкидыш / преждевременные роды (%) | 50 (1,4%) | 9 (1,4%) ) |
. | Группа A ТТГ <2,5 (n = 3481) . | Группа B 2,5 ≤ ТТГ ≤ 5,0 (n = 642) . |
|---|---|---|
| Возраст (лет) | 28,7 ± 5 | 29.2 ± 5 |
| Раньше младенцы (%) | 2447 (70,3%) | 458 (71,3%) |
| Курение (%) | 185 (5,3%) | 38 (5,9%) |
| Первый гинекологический визит (нед.) | 8,8 ± 1,6 | 8,9 ± 1,5 |
| ТТГ в первом триместре (мМЕ / литр), медиана (межквартильный размах) a | 0,82 (0,36–1,40) | (2,79–3,44) |
| Бесплатно T 4 первый триместр (пмоль / литр) a | 12.2 ± 2,1 | 10,6 ± 2,2 |
| Семейный анамнез заболевания щитовидной железы (%) b | 443 (12,7%) | 64 (10%) |
| Зоб (%) | 29 (0,8 %) | 4 (0,6%) |
| Симптомы гипо- / гипертиреоза (%) | 267 (7,7%) | 45 (7%) |
| Диабет 1 типа / аутоиммунное заболевание (%) | 34 (1%) | 6 (0,9%) |
| Облучение (%) | 1 (0. 03%) 03%) | 1 (0,1%) |
| Предыдущий выкидыш / преждевременные роды (%) | 50 (1,4%) | 9 (1,4%) |
Клинические характеристики пациентов по группам
| . | Группа A ТТГ <2,5 (n = 3481) . | Группа B 2,5 ≤ ТТГ ≤ 5,0 (n = 642) . |
|---|---|---|
| Возраст (лет) | 28,7 ± 5 | 29.2 ± 5 |
| Раньше младенцы (%) | 2447 (70,3%) | 458 (71,3%) |
| Курение (%) | 185 (5,3%) | 38 (5,9%) |
| Первый гинекологический визит (нед.) | 8,8 ± 1,6 | 8,9 ± 1,5 |
| ТТГ в первом триместре (мМЕ / литр), медиана (межквартильный размах) a | 0,82 (0,36–1,40) | (2,79–3,44) |
| Бесплатно T 4 первый триместр (пмоль / литр) a | 12. 2 ± 2,1 2 ± 2,1 | 10,6 ± 2,2 |
| Семейный анамнез заболевания щитовидной железы (%) b | 443 (12,7%) | 64 (10%) |
| Зоб (%) | 29 (0,8 %) | 4 (0,6%) |
| Симптомы гипо- / гипертиреоза (%) | 267 (7,7%) | 45 (7%) |
| Диабет 1 типа / аутоиммунное заболевание (%) | 34 (1%) | 6 (0,9%) |
| Облучение (%) | 1 (0.03%) | 1 (0,1%) |
| Предыдущий выкидыш / преждевременные роды (%) | 50 (1,4%) | 9 (1,4%) |
| . | Группа A ТТГ <2,5 (n = 3481) . | Группа B 2,5 ≤ ТТГ ≤ 5,0 (n = 642) . |
|---|---|---|
| Возраст (лет) | 28,7 ± 5 | 29,2 ± 5 |
| Раньше дети (%) | 2447 (70.3%) | 458 (71,3%) |
| Курение (%) | 185 (5,3%) | 38 (5,9%) |
Первое посещение гинеколога (нед. ) ) | 8,8 ± 1,6 | 8,9 ± 1,5 |
| ТТГ в первом триместре (мМЕ / литр), медиана (межквартильный размах) a | 0,82 (0,36–1,40) | 3,14 (2,79–3,44) |
| Свободный T 4 первый триместр (пмоль / литр) a | 12.2 ± 2,1 | 10,6 ± 2,2 |
| Семейный анамнез заболевания щитовидной железы (%) b | 443 (12,7%) | 64 (10%) |
| Зоб (%) | 29 (0,8 %) | 4 (0,6%) |
| Симптомы гипо- / гипертиреоза (%) | 267 (7,7%) | 45 (7%) |
| Диабет 1 типа / аутоиммунное заболевание (%) | 34 (1%) | 6 (0,9%) |
| Облучение (%) | 1 (0.03%) | 1 (0,1%) |
| Предыдущий выкидыш / преждевременные роды (%) | 50 (1,4%) | 9 (1,4%) |
Частота самопроизвольной потери беременности в группе А (3,6%, n = 127 из 3481) был значительно ниже, чем частота самопроизвольного прерывания беременности в группе B (6,1%, n = 39 из 642) ( P = 0,006). В группе A было пять мертворождений (пять из 127 = 3,9%) и два мертворождения в группе B (два из 39 = 5,1%). Не было различий между группами в частоте преждевременных родов (группа A, 4.7% vs. группа B, 5,1%, P = нс) или очень преждевременные роды (группа A, 1.85% vs. группа B, 0,93%, P = нс). Свободный T 4 был значительно выше в группе A по сравнению с группой B. Однако частота спонтанного прерывания беременности, преждевременных родов или очень преждевременных родов не была связана с уровнями свободного T 4 . В таблице 2 представлены возраст, предыдущий акушерский анамнез, клинические данные, тесты функции щитовидной железы и средний гестационный возраст потери беременности в группах A и B с разбивкой по наличию или отсутствию потери беременности.Не было различий в возрасте матери, истории беременности или тестах функции щитовидной железы у женщин, у которых произошел выкидыш, в каждой группе: и женщин, у которых выкидыш не был.
В группе A было пять мертворождений (пять из 127 = 3,9%) и два мертворождения в группе B (два из 39 = 5,1%). Не было различий между группами в частоте преждевременных родов (группа A, 4.7% vs. группа B, 5,1%, P = нс) или очень преждевременные роды (группа A, 1.85% vs. группа B, 0,93%, P = нс). Свободный T 4 был значительно выше в группе A по сравнению с группой B. Однако частота спонтанного прерывания беременности, преждевременных родов или очень преждевременных родов не была связана с уровнями свободного T 4 . В таблице 2 представлены возраст, предыдущий акушерский анамнез, клинические данные, тесты функции щитовидной железы и средний гестационный возраст потери беременности в группах A и B с разбивкой по наличию или отсутствию потери беременности.Не было различий в возрасте матери, истории беременности или тестах функции щитовидной железы у женщин, у которых произошел выкидыш, в каждой группе: и женщин, у которых выкидыш не был. Наблюдалось небольшое, но статистически значимое увеличение показателей курения среди женщин, у которых не было выкидыша в группе А. Средний гестационный возраст на момент первого акушерского визита и средний гестационный возраст на момент выкидыша были практически идентичными во всех четырех случаях. группы.
Наблюдалось небольшое, но статистически значимое увеличение показателей курения среди женщин, у которых не было выкидыша в группе А. Средний гестационный возраст на момент первого акушерского визита и средний гестационный возраст на момент выкидыша были практически идентичными во всех четырех случаях. группы.
Клиническая характеристика пациентов по группам и истории выкидышей
| . | Группа А (n = 3481) . | Группа Б (n = 642) . | ||
|---|---|---|---|---|
| Потеря беременности (n = 127) (3,6%) . | Без потери беременности (n = 3354) (96,4%) . | Потеря беременности (n = 39) (6,1%) . | Отсутствие потери беременности (n = 603) (93,9%) . | |
| Возраст (лет) | 31,7 ± 3,1 | 28,5 ± 5,0 | 31.3 ± 2,4 | 29,0 ± 5,2 |
| Предыдущие дети (n) | 88 (69,3%) | 2359 (70,3%) | 28 (71,8%) | 430 (71,3%) |
| Курение (%) | 1 (0,8%) | 184 (5,5%) a | 0 (0,0%) | 38 (6,3%) |
Первый гинекологический визит (нед. ) ) | 8,9 ± 1,5 | 8,8 ± 1,6 | 8,8 ± 1,5 | 8,9 ± 1,5 |
| Неделя потери беременности | 11.7 ± 3,7 | 11,8 ± 3,6 | ||
| ТТГ в первом триместре (мМЕ / л), медиана (межквартильный размах) | 0,72 (0,30–1,33) | 0,82 (0,36–1,40) | 3,2 2,79–3,61) | 3,14 (2,79–3,43) |
| Бесплатно T 4 первый триместр (пмоль / литр) | 12,4 ± 2,2 | 12,2 ± 2,1 | 9,9 ± 2,4 | 10,6 ± 2,1 |
| Семейный анамнез заболевания щитовидной железы (%) | 13 (10.2%) | 430 (12,8%) | 7 (17,9%) | 57 (9,4%) |
| Зоб (%) | 0 (0%) | 29 (0,9%) | 0 ( 0%) | 4 (0,7%) |
| Симптомы гипо- / гипертиреоза (%) | 7 (5,5%) | 260 (7,7%) | 3 (7,7%) | 42 (7%) ) |
| Диабет 1 типа / аутоиммунное заболевание (%) | 0 (0%) | 34 (1%) | 0 (0%) | 6 (1%) |
| Облучение (%) | 0 (0%) | 1 (0. 03%) 03%) | 0 (0%) | 1 (0,2%) |
| Предыдущий выкидыш / преждевременные роды (%) | 3 (2,4%) | 47 (1,4%) | 0 (0%) | 9 (1,5%) |
| . | Группа А (n = 3481) . | Группа Б (n = 642) . | ||
|---|---|---|---|---|
| Потеря беременности (n = 127) (3,6%) . | Отсутствие потери беременности (n = 3354) (96.4%) . | Потеря беременности (n = 39) (6,1%) . | Отсутствие потери беременности (n = 603) (93,9%) . | |
| Возраст (лет) | 31,7 ± 3,1 | 28,5 ± 5,0 | 31,3 ± 2,4 | 29,0 ± 5,2 |
| Предыдущие дети (n) | 88 (69,3%) | 2359 ( 70,3%) | 28 (71,8%) | 430 (71,3%) |
| Курение (%) | 1 (0.8%) | 184 (5,5%) a | 0 (0,0%) | 38 (6,3%) |
Первое гинекологическое посещение (нед.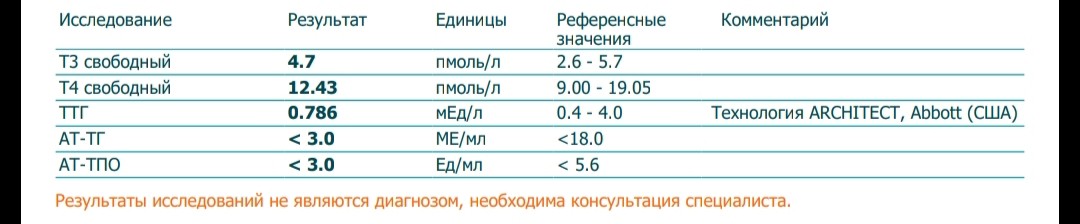 ) ) | 8,9 ± 1,5 | 8,8 ± 1,6 | 8,8 ± 1,5 | 8,9 ± 1,5 |
| Неделя потери беременности | 11,7 ± 3,7 | 11,8 ± 3,6 | ||
| ТТГ в первом триместре (мМЕ / литр), медиана (межквартильный размах) | (0,30–1,33) | 0.82 (0,36–1,40) | 3,29 (2,79–3,61) | 3,14 (2,79–3,43) |
| Свободный T 4 первый триместр (пмоль / литр) | 12,4 ± 2,2 | 12,2 ± 2,1 | 9,9 ± 2,4 | 10,6 ± 2,1 |
| Семейный анамнез заболевания щитовидной железы (%) | 13 (10,2%) | 430 (12,8%) | 7 (17,9%) | 57 (9,4%) |
| Зоб (%) | 0 (0%) | 29 (0,9%) | 0 (0%) | 4 (0.7%) |
| Симптомы гипо- / гипертиреоза (%) | 7 (5,5%) | 260 (7,7%) | 3 (7,7%) | 42 (7%) |
| Тип 1 диабет / аутоиммунное заболевание (%) | 0 (0%) | 34 (1%) | 0 (0%) | 6 (1%) |
| Облучение (%) | 0 (0%) | 1 (0,03%) | 0 (0%) | 1 (0,2%) |
| Предыдущий выкидыш / преждевременные роды (%) | 3 (2.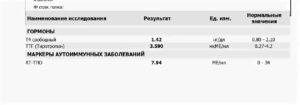 4%) 4%) | 47 (1,4%) | 0 (0%) | 9 (1,5%) |
Клиническая характеристика пациентов по группам и история невынашивания беременности
| . | Группа А (n = 3481) . | Группа Б (n = 642) . | ||
|---|---|---|---|---|
| Потеря беременности (n = 127) (3,6%) . | Без потери беременности (n = 3354) (96,4%) . | Потеря беременности (n = 39) (6.1%) . | Отсутствие потери беременности (n = 603) (93,9%) . | |
| Возраст (лет) | 31,7 ± 3,1 | 28,5 ± 5,0 | 31,3 ± 2,4 | 29,0 ± 5,2 |
| Предыдущие дети (n) | 88 (69,3%) | 2359 ( 70,3%) | 28 (71,8%) | 430 (71,3%) |
| Курение (%) | 1 (0,8%) | 184 (5,5%) a | 0 (0. 0%) 0%) | 38 (6,3%) |
| Первое гинекологическое посещение (нед.) | 8,9 ± 1,5 | 8,8 ± 1,6 | 8,8 ± 1,5 | 8,9 ± 1,5 |
| Неделя потери беременности | 11,7 ± 3,7 | 11,8 ± 3,6 | ||
| ТТГ в первом триместре (мМЕ / л), медиана (межквартильный размах) | 0,72 (0,30–1,33) | 0,82 (0,36–1,40) | 2.79–3.61) | 3.14 (2,79–3,43) |
| Свободный T 4 первый триместр (пмоль / литр) | 12,4 ± 2,2 | 12,2 ± 2,1 | 9,9 ± 2,4 | 10,6 ± 2,1 |
| Семейный анамнез щитовидной железы болезнь (%) | 13 (10,2%) | 430 (12,8%) | 7 (17,9%) | 57 (9,4%) |
| Зоб (%) | 0 (0%) | 29 (0,9%) | 0 (0%) | 4 (0,7%) |
| Симптомы гипо- / гипертиреоза (%) | 7 (5.5%) | 260 (7,7%) | 3 (7,7%) | 42 (7%) |
| Диабет / аутоиммунное заболевание 1 типа (%) | 0 (0%) | 34 (1%) ) | 0 (0%) | 6 (1%) |
| Облучение (%) | 0 (0%) | 1 (0,03%) | 0 (0%) | 1 (0,2%) ) |
| Предыдущий выкидыш / преждевременные роды (%) | 3 (2,4%) | 47 (1,4%) | 0 (0%) | 9 (1. 5%) 5%) |
| . | Группа А (n = 3481) . | Группа Б (n = 642) . | ||
|---|---|---|---|---|
| Потеря беременности (n = 127) (3,6%) . | Без потери беременности (n = 3354) (96,4%) . | Потеря беременности (n = 39) (6,1%) . | Отсутствие потери беременности (n = 603) (93,9%) . | |
| Возраст (лет) | 31.7 ± 3,1 | 28,5 ± 5,0 | 31,3 ± 2,4 | 29,0 ± 5,2 |
| Предыдущие дети (n) | 88 (69,3%) | 2359 (70,3%) | 28 (71,8%) | 430 (71,3%) |
| Курение (%) | 1 (0,8%) | 184 (5,5%) a | 0 (0,0%) | 38 (6,3%) |
| Первый гинекологический посещение (нед.) | 8,9 ± 1,5 | 8,8 ± 1,6 | 8. 8 ± 1,5 8 ± 1,5 | 8,9 ± 1,5 |
| Неделя потери беременности | 11,7 ± 3,7 | 11,8 ± 3,6 | ||
| ТТГ в первом триместре (мМЕ / л), медиана (межквартильный размах) | 0,72 (0,30–1,33) | 0,82 (0,36–1,40) | 3,29 (2,79–3,61) | 3,14 (2,79–3,43) |
| Свободный T 4 первый триместр (пмоль / литр) | 12,4 ± 2,2 | 12,2 ± 2.1 | 9,9 ± 2,4 | 10,6 ± 2,1 |
| Семейный анамнез заболевания щитовидной железы (%) | 13 (10,2%) | 430 (12,8%) | 7 (17,9%) | 57 (9,4%) ) |
| Зоб (%) | 0 (0%) | 29 (0,9%) | 0 (0%) | 4 (0,7%) |
| Симптомы гипо- / гипертиреоза (%) | 7 (5,5%) | 260 (7,7%) | 3 (7,7%) | 42 (7%) |
| Диабет / аутоиммунное заболевание 1 типа (%) | 0 (0%) | 34 (1%) | 0 (0%) | 6 (1%) |
| Облучение (%) | 0 (0%) | 1 (0.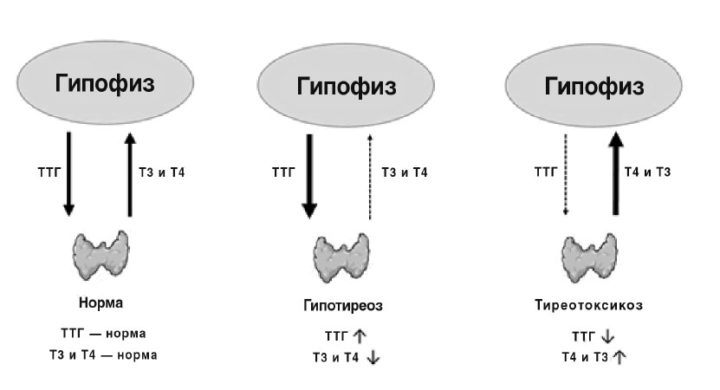 03%) 03%) | 0 (0%) | 1 (0,2%) |
| Предыдущий выкидыш / преждевременные роды (%) | 3 (2,4%) | 47 (1,4%) | 0 (0%) | 9 (1,5%) |
Для дальнейшего изучения влияния уровней ТТГ мы использовали простую логистическую регрессию для прогнозирования выкидыша на основе уровня ТТГ (рассматриваемого как непреобразованная непрерывная переменная) и статуса курения. Среди женщин в нашей выборке отношение шансов для каждой точки ТТГ было 1.157 (95% доверительный интервал 1,002, 1,336, P = 0,047), предполагая постоянную связь между ТТГ и выкидышем с учетом курения. Как и в одномерном анализе, вероятность выкидыша у курильщиков была ниже, чем у некурящих (отношение шансов 0,102, 95% доверительный интервал 0,014, 0,732, P = 0,023), с учетом уровня ТТГ.
Обсуждение
Настоящее исследование впервые продемонстрировало, что уровень ТТГ составляет от 2,5 до 5.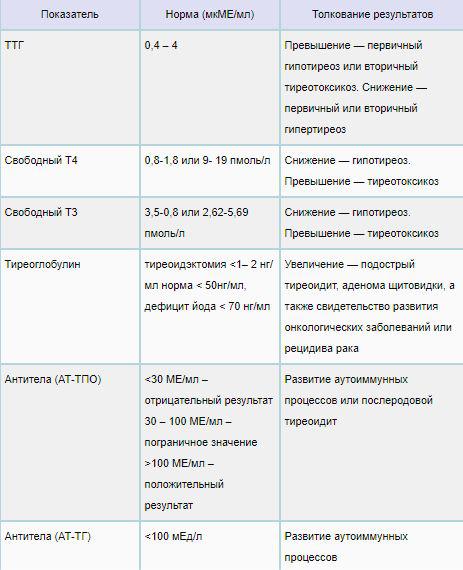 0 у женщин с отрицательными антителами к щитовидной железе в первом триместре ассоциируется со значительным увеличением частоты спонтанного прерывания беременности по сравнению с женщинами с отрицательными антителами к щитовидной железе в первом триместре с уровнем ТТГ менее 2,5 мМЕ / л (за исключением женщин с гипертиреозом). Не было обнаружено различий в частоте преждевременных или очень преждевременных родов. Повышенная частота выкидышей у женщин с уровнем ТТГ от 2,5 до 5,0 мМЕ / литр является убедительной поддержкой для пересмотра нормального диапазона ТТГ во время беременности, особенно в первом триместре.
0 у женщин с отрицательными антителами к щитовидной железе в первом триместре ассоциируется со значительным увеличением частоты спонтанного прерывания беременности по сравнению с женщинами с отрицательными антителами к щитовидной железе в первом триместре с уровнем ТТГ менее 2,5 мМЕ / л (за исключением женщин с гипертиреозом). Не было обнаружено различий в частоте преждевременных или очень преждевременных родов. Повышенная частота выкидышей у женщин с уровнем ТТГ от 2,5 до 5,0 мМЕ / литр является убедительной поддержкой для пересмотра нормального диапазона ТТГ во время беременности, особенно в первом триместре.
За последнее десятилетие нормативный диапазон уровней ТТГ во время беременности стал предметом все более пристальных исследований. Panesar et al. (3) сообщил в проспективном исследовании 343 китайских женщин, что нормативный диапазон уровней ТТГ в первом триместре беременности составляет 0,03–2,3 мМЕ / л. Pearce et al. (4) исследовал 585 женщин с отрицательными антителами к щитовидной железе (в Бостоне, Массачусетс) до 14 недель беременности и обнаружил, что 95% уровней ТТГ упали между 0,04 и 3,6 мМЕ / л. Гилберт и др. (5) изучали 1817 австралийских женщин с отрицательными антителами к щитовидной железе между 9 и 13 неделями беременности и сообщили о контрольном диапазоне 0.02–2,15 мМЕ / литр. Stricker et al. (6) провел скрининг 783 женщин с отрицательными антителами к щитовидной железе из Женевы, Швейцария, и сообщил о процентильном диапазоне 2,5–97 как 0,08–2,83 мМЕ / л. В целом, наблюдалась замечательная согласованность в диапазонах ТТГ, сообщаемых для женщин с отрицательными антителами в первом триместре, с консенсусом, сосредоточенным вокруг нижнего предела нормы 0,04 и верхнего диапазона нормы 2,5.
Гилберт и др. (5) изучали 1817 австралийских женщин с отрицательными антителами к щитовидной железе между 9 и 13 неделями беременности и сообщили о контрольном диапазоне 0.02–2,15 мМЕ / литр. Stricker et al. (6) провел скрининг 783 женщин с отрицательными антителами к щитовидной железе из Женевы, Швейцария, и сообщил о процентильном диапазоне 2,5–97 как 0,08–2,83 мМЕ / л. В целом, наблюдалась замечательная согласованность в диапазонах ТТГ, сообщаемых для женщин с отрицательными антителами в первом триместре, с консенсусом, сосредоточенным вокруг нижнего предела нормы 0,04 и верхнего диапазона нормы 2,5.
Benhadi et al. (17) недавно сообщили о взаимосвязи между уровнями ТТГ (после исключения явного гипотиреоза, классифицированного как ТТГ> 5.6 мМЕ / литр с бесплатным T 4 <7,7 пмоль / литр), и потеря ребенка, определяемая как сочетание выкидыша, внутриутробной или неонатальной смерти у 2497 голландских женщин. Средний срок гестации на момент включения в исследование составлял 13 недель, и женщины, включенные в исследование после 27 недель, были исключены из анализа. Исследование показало 60% увеличение потери детей при каждом удвоении концентрации ТТГ. Большая часть потери ребенка произошла в результате внутриутробной или неонатальной смерти (16 из 27) по сравнению с выкидышем (11 из 27), что отражает поздний гестационный возраст при первоначальном скрининге.Авторы делают вывод, что «… исход беременности можно улучшить, если лечить женщин с умеренно повышенным ТТГ (как при субклиническом гипотиреозе) или даже с нормальным ТТГ (если присутствуют ТПО-Ab)».
Исследование показало 60% увеличение потери детей при каждом удвоении концентрации ТТГ. Большая часть потери ребенка произошла в результате внутриутробной или неонатальной смерти (16 из 27) по сравнению с выкидышем (11 из 27), что отражает поздний гестационный возраст при первоначальном скрининге.Авторы делают вывод, что «… исход беременности можно улучшить, если лечить женщин с умеренно повышенным ТТГ (как при субклиническом гипотиреозе) или даже с нормальным ТТГ (если присутствуют ТПО-Ab)».
Сильными сторонами настоящего исследования являются большой размер когорты, исключение женщин, у которых были антитела к тироидной пероксидазе, и его перспективный характер. Ограничения исследования включают тот факт, что население состоит из женщин из одной географической области (южная Италия), которая имеет в анамнезе умеренный дефицит йода.Как продемонстрировало недавнее исследование Moleti et al. (18), также проведенного в южной Италии, дефицит йода играет ключевую роль в развитии нарушений щитовидной железы во время беременности. Другой потенциальный недостаток исследования заключается в том, что антитела к тиреоглобулину не измерялись, и поэтому следует предположить, что небольшой процент женщин был бы положительным по антителам к тиреоглобулину. Поскольку у женщин с положительными антителами к тиреоглобулину (отрицательными к тироидной пероксидазе) в первом триместре может развиться нарушение функции щитовидной железы по мере продолжения беременности, это могло повлиять на результаты исследования.Наконец, следует отметить небольшое увеличение числа курящих среди женщин группы А, у которых не было выкидыша, по сравнению с женщинами из группы А, у которых была потеря беременности. Причина этого неясна.
Другой потенциальный недостаток исследования заключается в том, что антитела к тиреоглобулину не измерялись, и поэтому следует предположить, что небольшой процент женщин был бы положительным по антителам к тиреоглобулину. Поскольку у женщин с положительными антителами к тиреоглобулину (отрицательными к тироидной пероксидазе) в первом триместре может развиться нарушение функции щитовидной железы по мере продолжения беременности, это могло повлиять на результаты исследования.Наконец, следует отметить небольшое увеличение числа курящих среди женщин группы А, у которых не было выкидыша, по сравнению с женщинами из группы А, у которых была потеря беременности. Причина этого неясна.
В 2004 году по завершении конференции по щитовидной железе и беременности, организованной Центрами по контролю и профилактике заболеваний, было задано несколько вопросов для дальнейших исследований, в том числе «… какой должна быть концентрация ТТГ для постановки диагноза субклинического гипотиреоза…» ( 19). Данные для ответа на этот вопрос теперь существуют. Недавние нормативные исследования подтверждают, что требуется новое определение, в результате чего диапазон составляет приблизительно 0,03–2,5 мМЕ / л. Настоящее исследование показывает, что уровни ТТГ, несколько превышающие этот диапазон (2,5–5,0 мМЕ / л), связаны с повышенным уровнем потери беременности. Таким образом, можно сделать вывод, что уровень ТТГ выше 2,5 мМЕ / литр не только превышает процентиль 97,5 для первого триместра беременности, но также связан с серьезными физиологическими последствиями.Negro et al. (16) в проспективном рандомизированном исследовании недавно сообщил, что лечение женщин с положительными антителами к щитовидной железе с уровнем ТТГ 2,5 мМЕ / литр или выше приводит к значительному снижению материнских и неонатальных осложнений. В настоящее время необходимо аналогичное исследование для женщин с отрицательными антителами к щитовидной железе с ТТГ выше 2,5 мМЕ / л.
Данные для ответа на этот вопрос теперь существуют. Недавние нормативные исследования подтверждают, что требуется новое определение, в результате чего диапазон составляет приблизительно 0,03–2,5 мМЕ / л. Настоящее исследование показывает, что уровни ТТГ, несколько превышающие этот диапазон (2,5–5,0 мМЕ / л), связаны с повышенным уровнем потери беременности. Таким образом, можно сделать вывод, что уровень ТТГ выше 2,5 мМЕ / литр не только превышает процентиль 97,5 для первого триместра беременности, но также связан с серьезными физиологическими последствиями.Negro et al. (16) в проспективном рандомизированном исследовании недавно сообщил, что лечение женщин с положительными антителами к щитовидной железе с уровнем ТТГ 2,5 мМЕ / литр или выше приводит к значительному снижению материнских и неонатальных осложнений. В настоящее время необходимо аналогичное исследование для женщин с отрицательными антителами к щитовидной железе с ТТГ выше 2,5 мМЕ / л.
Благодарности
Краткое раскрытие информации: R. N., A.S., R.G., A.T., T.M., and A.S.-G. нечего заявлять.
N., A.S., R.G., A.T., T.M., and A.S.-G. нечего заявлять.
Список литературы
1Абалович
М
,Амино
N
,Barbour
LA
,Cobin
RH
,Де Гроот
LJ
,Глинер
D
,Мандель
SJ
,Стагнаро-Зеленый
А
2007
Лечение дисфункции щитовидной железы во время беременности и в послеродовом периоде: руководство по клинической практике эндокринного общества
.J Clin Endocrinol Metab
92
(Suppl
):S1
—S47
2Hershman
JM
2004
Физиологические и патологические аспекты действия хорионического гонадотропина человека на щитовидную железу.
Best Practices Clin Endocrinol Metab
18
:249
—265
3Панесар
NS
,Li
CY
,Роджерс
MS
2001
Референсные интервалы гормонов щитовидной железы у беременных китаянок./124/124.jpg)
Ann Clin Biochem
38
:329
—332
4Пирс
EN
,Окен
E
,Gillman
МВт
,Ли
SL
,Magnani
B
,Платек
D
,Браверман
LE
2008
Связь значений теста функции щитовидной железы в первом триместре со статусом антител к тироидной пероксидазе, курением и употреблением поливитаминов.
Endocr Pract
14
:33
—39
5Гилберт
RM
,Хадлоу
NC
,Уолш
JP
,Флетчер
SJ
,Коричневый
SJ
,Stuckey
BG
,Li
EM
2008
Оценка функции щитовидной железы во время беременности: референсные интервалы в первом триместре (9–13 недели) получены от женщин Западной Австралии.
Med J Aust
189
:250
—253
6Стрикер
R
,Echenard
M
,Эберхарт
R
,Chevailler
MC
,Перес
В
,Куинн
FA
,Стрикер
R
2007
Оценка функции щитовидной железы матери во время беременности: важность использования референсных интервалов для гестационного возраста.
Eur J Эндокринол
157
:509
—514
7Абалович
М
,Гутьеррес
S
,Алькарез
G
,Maccallini
G
,Гарсия
А
,Levalle
O
2002
Явный и субклинический гипотиреоз, осложняющий исход беременности.
Щитовидная железа
12
:63
—68
8Аллан
WC
,Haddow
JE
,Палимаки
GE
,Уильямс
JR
,Митчелл
ML
,Hermos
RJ
,Faix
JD
,Кляйн
RZ
2007
Дефицит щитовидной железы у матери и осложнения беременности: значение для скрининга населения.
J Средний экран
7
:127
—130
9Клири-Голдман
Дж
,Мэлоун
FD
,Ламберт-Мессерлиан
G
,Салливан
L
,Каник
Дж
,Портер
TF
,Люти
D
,Брутто
S
,Бьянки
DW
, D’Alton ME для FASTER Consortium2008
Гипофункция щитовидной железы матери и исход беременности.
Акушер-гинеколь
112
:85
—92
10Стагнаро-Зеленый
А
2009
Заболевания щитовидной железы матери и преждевременные роды.
J Clin Endocrinol Metab
94
:21
—25
11Кейси
BM
,Даше
JS
,скважин
CE
,McIntire
DD
,Левено
кДж
,Каннингем
FG
2006
Субклинический гипотиреоз и исходы беременности.
Акушер-гинеколь
107
:337
—341
12Стагнаро-Зеленый
А
,Чен
X
,Богден
JD
,Дэвис
TF
,Scholl
TO
2005
Щитовидная железа и беременность: новый фактор риска преждевременных родов.
Щитовидная железа
15
:351
—357
13Prummel
MF
,Wiersinga
WM
2004
Аутоиммунитет щитовидной железы и выкидыш.
Eur J Эндокринол
150
:751
—755
14Глинер
D
2006
Выкидыш у женщин с антителами против ТПО: тироксин — ответ.
J Clin Endocrinol Metab
91
:2500
—2502
15негр
р
,Formoso
G
,Mangieri
T
,Pezzarossa
A
,Dazzi
D
,Хасан
H
2006
Лечение левотироксином у эутиреоидных беременных женщин с аутоиммунным заболеванием щитовидной железы: влияние на акушерские осложнения.
J Clin Endocrinol Metab
91
:2587
—2591
16негр
р
,Шварц
A
,Gismondi
R
,Тинелли
А
,Mangieri
T
,Стагнаро-Зеленый
А
2010
Универсальный скрининг в сравнении с выявлением случаев для выявления и лечения гормональной дисфункции щитовидной железы во время беременности.
J Clin Endocrinol Metab
95
:1699
—1707
17Бенхади
N
,Wiersinga
WM
,Рейцма
ДБ
,Врийкотте
TG
,Bonsel
GJ
2009
Более высокие уровни ТТГ у матери во время беременности связаны с повышенным риском выкидыша, внутриутробной или неонатальной смерти.
Eur J Эндокринол
160
:985
—991
18Moleti
M
,Lo Presti
VP
,Маттина
Ф
,Манкузо
A
,De Vivo
A
,Джорджанни
G
,Ди Белла
B
,Trimarchi
F
,Vermiglio
F
2009
Нарушения гестационной функции щитовидной железы в условиях легкого дефицита йода: ранний скрининг по сравнению с постоянным мониторингом гестационного статуса.
Eur J Эндокринол
160
:611
—617
19Холлоуэлл
JG
,LaFranchi
S
,Малый мост
RC
,Губка
CY
,Haddow
JE
,Бойл
CA
2005
2004 Куда мы пойдем дальше? Резюме обсуждения в рабочей группе функции щитовидной железы и исходов беременности.
Щитовидная железа
15
:72
—76
Авторские права © 2010 Общество эндокринологов
Высокий нормальный уровень ТТГ связан с более низким содержанием маннан-связывающего лектина у женщин детородного возраста | BMC Endocrine Disorders
В нашем настоящем анализе мы нашли еще один аргумент, не связанный напрямую с беременностью или фертильностью, в пользу поддержания ТТГ ниже 2,5 мМЕ / л или, по крайней мере, в более низких нормальных диапазонах у женщин детородного возраста.
Мы наблюдали, что уровень MBL, являющийся компонентом врожденного иммунного ответа, ниже у пациенток репродуктивного возраста с высоким нормальным ТТГ. Кроме того, более низкие уровни MBL были связаны с худшим липидным профилем, что подтверждалось более низким уровнем MBL у пациентов с аномально низким соотношением HDLC / холестерин и положительной корреляцией между уровнем MBL и соотношением HDLC / холестерин.
Генетически определенные диапазоны референсных значений MBL чрезвычайно широки. Однако в случае идентичных генотипов синтез MBL может изменяться в ответ на различные патологические состояния, как упоминалось во введении.Что касается взаимосвязи между уровнем MBL и функцией щитовидной железы, более низкие значения MBL были связаны с гипотиреозом [3,4,5]. Таким образом, наше настоящее наблюдение, показывающее более низкие концентрации MBL у женщин с ТТГ ≥ 2,5 мМЕ / л, предполагает, что высокий нормальный ТТГ у женщин детородного возраста менее благоприятен и, следовательно, должен рассматриваться как отклонение от нормы.
Другой аргумент, вытекающий из настоящего исследования в пользу поддержания ТТГ в более низких нормальных диапазонах, связан с выявлением менее благоприятных липидных профилей у пациентов с более низким уровнем MBL.Это согласуется с нашими предыдущими результатами [14], показывающими, что женщины с ТТГ ≥ 2,5 мМЕ / л имеют менее благоприятные липидные профили, что, в свою очередь, связано с более высоким окислительным повреждением липидов мембран. Это также согласуется с предложением существенно снизить пороговое значение ТТГ для диагностики тиреоидита Хашимото [15].
Это также согласуется с предложением существенно снизить пороговое значение ТТГ для диагностики тиреоидита Хашимото [15].
Поскольку мы задокументировали, что более высокий уровень перекисного окисления липидов [14] и более низкий уровень MBL (настоящее исследование) были связаны с ТТГ ≥ 2,5 мМЕ / л, мы решили статистически оценить, какой из них является более важным фактором высокого нормального ТТГ. .При оценке с помощью одномерного логистического регрессионного анализа среди множества линейных переменных уровень перекисного окисления липидов и уровень MBL были единственными двумя детерминантами, связанными с более высокой нормальной концентрацией ТТГ. Однако многомерный логистический регрессионный анализ показал, что уровень перекисного окисления липидов является единственным независимым фактором, связанным с ТТГ ≥ 2,5 мМЕ / л. Таким образом, на основании наших результатов можно предположить, что окислительное повреждение более тесно связано с аномальным уровнем ТТГ по сравнению с иммунным ответом, в частности с лектиновым путем системы комплемента.
Тем не менее, наши результаты по-прежнему имеют большое значение, поскольку они показывают аномальные иммунные ответы, возникающие в результате более высокого, но нормального уровня ТТГ. Таким образом, наши результаты открывают новую область иммунных механизмов, ответственных за различные аномалии органов в ответ на легкую дисфункцию щитовидной железы. Можно предположить, что определенные нарушения лектинового пути системы комплемента уже присутствуют в условиях умеренного гипотиреоза и могут способствовать таким явлениям, как бесплодие или неблагоприятный исход беременности.
В настоящем исследовании мы подтвердили, что уровень MBL не зависит от наличия антител к щитовидной железе. Это открытие имеет большое значение, поскольку оба, то есть MBL и антитела к щитовидной железе, являются компонентами иммунной системы. Таким образом, наши результаты подтверждают, что на уровень MBL влияет дисфункция щитовидной железы независимо от аутоиммунного процесса, который является основным этиологическим фактором гипотиреоза.
Аналогичным образом, мы наблюдали в настоящем исследовании, что уровень MBL не был статистически связан с лечением L-тироксином, что еще раз подчеркивает сильную связь между уровнем MBL и функцией щитовидной железы.
В нашем исследовании мы обнаружили, что уровень MBL отрицательно коррелирует с возрастом. Это наблюдение было ожидаемым, поскольку эффективность иммунной системы естественным образом снижается с возрастом, и согласуется с более ранними наблюдениями, показывающими, что лектиновый путь, активируемый маннаном, ниже у пожилых людей [16].
Здоровье селена и щитовидной железы в Новой Зеландии Европейские женщины
Аннотация
Основная цель исследования заключалась в том, чтобы определить различия в гормональном статусе (ТТГ, Т3 и Т4) между здоровыми участниками и участниками с тиреоидитом Хашимото.Вторичной целью исследования была оценка статуса питания селена в плазме и его взаимосвязи с уровнями гормонов щитовидной железы в сыворотке в обеих группах.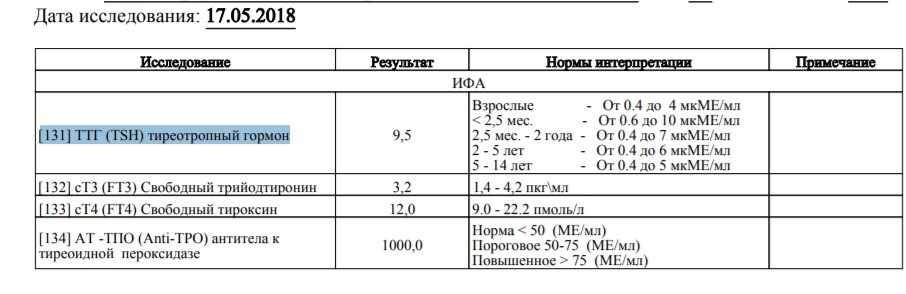 Это экспериментальное и перекрестное исследование. Участницы исследования были разделены на две группы: контрольную группу со здоровыми участниками (n = 13) и группу женщин с тиреоидитом Хашимото (n = 8). Никаких изменений в распорядке дня участников не требовалось. Для измерения уровня селена, тиреотропного гормона, тетрайодтиронина и трийодтиронина, креатинина и скорости клубочковой фильтрации в плазме крови у участников были взяты пробы крови, взятой не натощак.Две женщины с субклиническим гипотиреозом были исключены из анализа статистических данных. Женщины с тиреоидитом Хашимото были старше, имели более высокий уровень тетрайодтиронина, низкое соотношение трийодтиронин / тетрайодтиронин, более высокие уровни селена в плазме и аналогичные уровни трийодтиронина в плазме с женщинами из контрольной группы. Значимые связи между трийодтиронином и селеном, трийодтиронином были выявлены в группе женщин с тиреоидитом Хашимото. В обеих группах наблюдался умеренный дефицит селена, от которого страдали женщины с гипотиреозом.
Это экспериментальное и перекрестное исследование. Участницы исследования были разделены на две группы: контрольную группу со здоровыми участниками (n = 13) и группу женщин с тиреоидитом Хашимото (n = 8). Никаких изменений в распорядке дня участников не требовалось. Для измерения уровня селена, тиреотропного гормона, тетрайодтиронина и трийодтиронина, креатинина и скорости клубочковой фильтрации в плазме крови у участников были взяты пробы крови, взятой не натощак.Две женщины с субклиническим гипотиреозом были исключены из анализа статистических данных. Женщины с тиреоидитом Хашимото были старше, имели более высокий уровень тетрайодтиронина, низкое соотношение трийодтиронин / тетрайодтиронин, более высокие уровни селена в плазме и аналогичные уровни трийодтиронина в плазме с женщинами из контрольной группы. Значимые связи между трийодтиронином и селеном, трийодтиронином были выявлены в группе женщин с тиреоидитом Хашимото. В обеих группах наблюдался умеренный дефицит селена, от которого страдали женщины с гипотиреозом.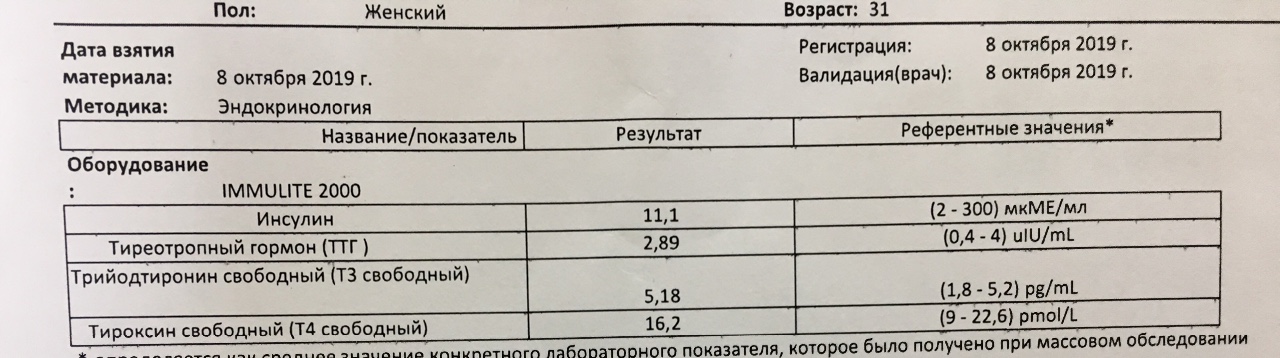 Нарушение периферического дейодирования у женщин с гипотиреозом потребовало увеличения дозировки L-тироксина, что, в свою очередь, увеличило уровень тетрайодтиронина и снизило уровень тиреотропного гормона гипофиза, чтобы достичь желаемого уровня трийодтиронина. Недавнее исследование показало, что для повышения уровня селена в плазме добавление селена с селенометионином или селенитом селена также может замедлить процесс разрушения щитовидной железы аутоантителами при тиреоидите Хашимото.В прошлом процесс добавления селена имел переменные показатели успеха. Следовательно, необходимы дальнейшие исследования.
Нарушение периферического дейодирования у женщин с гипотиреозом потребовало увеличения дозировки L-тироксина, что, в свою очередь, увеличило уровень тетрайодтиронина и снизило уровень тиреотропного гормона гипофиза, чтобы достичь желаемого уровня трийодтиронина. Недавнее исследование показало, что для повышения уровня селена в плазме добавление селена с селенометионином или селенитом селена также может замедлить процесс разрушения щитовидной железы аутоантителами при тиреоидите Хашимото.В прошлом процесс добавления селена имел переменные показатели успеха. Следовательно, необходимы дальнейшие исследования.
Ключевые слова
Новая Зеландия, селен, аутоиммунный тиреоидит Хашимото, L-тироксин
Сокращения
ТТГ: тиреотропный гормон; Т3: трийодтиронин; Т4: тетрайодтиронин; SeMet: селенометионин; SeCys: селеноцистеин
Введение
Оценки распространенности первичного гипотиреоза во всем мире колеблются от 1% до 10. 3%, а при гипертиреозе от 0,5% до 2,5% [1]. Имеются ограниченные данные о распространенности и типе заболевания щитовидной железы (БТ) в новозеландском сообществе. В исследовании Hamilton, в котором участвовали 662 пациента общей практики, оценивается общая распространенность TD у женщин около 4,8% и около 1,1% у мужчин. Следовательно, женщины в 4,5 раза чаще, чем мужчины, страдают ДТ. Европейская этническая группа Новой Зеландии имела наибольшую распространенность TD — 3,5%, затем этническая принадлежность маори — 2,1%, народы тихоокеанских островов — 1,8%, азиаты 1.8%, другие этнические группы 2,0%. Среди пациентов с TD гипотиреоз диагностирован у 2,5% в популяции, исследованной Гамильтоном, в то время как в общей практике на гипотиреоз приходится 78,9% диагностированных заболеваний щитовидной железы. Эти данные сопоставимы (с 3,1% TD у взрослых) с национальной и международной литературой, при этом TD более распространена у женщин и пожилых людей.
3%, а при гипертиреозе от 0,5% до 2,5% [1]. Имеются ограниченные данные о распространенности и типе заболевания щитовидной железы (БТ) в новозеландском сообществе. В исследовании Hamilton, в котором участвовали 662 пациента общей практики, оценивается общая распространенность TD у женщин около 4,8% и около 1,1% у мужчин. Следовательно, женщины в 4,5 раза чаще, чем мужчины, страдают ДТ. Европейская этническая группа Новой Зеландии имела наибольшую распространенность TD — 3,5%, затем этническая принадлежность маори — 2,1%, народы тихоокеанских островов — 1,8%, азиаты 1.8%, другие этнические группы 2,0%. Среди пациентов с TD гипотиреоз диагностирован у 2,5% в популяции, исследованной Гамильтоном, в то время как в общей практике на гипотиреоз приходится 78,9% диагностированных заболеваний щитовидной железы. Эти данные сопоставимы (с 3,1% TD у взрослых) с национальной и международной литературой, при этом TD более распространена у женщин и пожилых людей.
Секреция тиреоидных гормонов регулируется осью гипоталамус-гипофиз-тиреоид ic (ось HPT) посредством стимулирующего действия тиреотропин-рилизинг-гормона (TRH) и тиреотропного гормона (TSH) [2].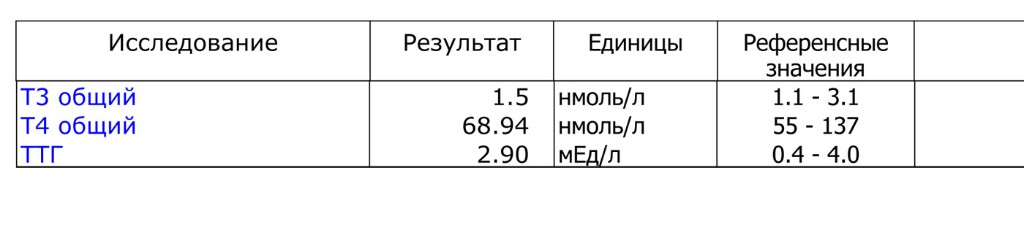 ТТГ стимулирует тироидную железу к синтезу тетрайодтиронина (Т4) и трийодтиронина (Т3). Т4 полностью синтезируется щитовидной железой и действует как прогормон для выработки Т3, который необходим для нормального роста и развития, энергетического гомеостаза и потребления O2 клетками ткани. Превращение Т4 в Т3 в тканях организма обеспечивает отрицательную обратную связь как на уровне передней доли гипофиза, так и на уровне гипоталамуса [3].
ТТГ стимулирует тироидную железу к синтезу тетрайодтиронина (Т4) и трийодтиронина (Т3). Т4 полностью синтезируется щитовидной железой и действует как прогормон для выработки Т3, который необходим для нормального роста и развития, энергетического гомеостаза и потребления O2 клетками ткани. Превращение Т4 в Т3 в тканях организма обеспечивает отрицательную обратную связь как на уровне передней доли гипофиза, так и на уровне гипоталамуса [3].
Щитовидная железа имеет высокую концентрацию в тканях основного питательного микроэлемента селена (Se), больше, чем печень или любой другой орган или ткань тела [4].Селен играет решающую роль в поддержании метаболического, иммуноэндокринного и клеточного гомеостаза благодаря своим антиоксидантным и противовоспалительным свойствам [5]. Биологическое действие селена в основном опосредовано экспрессией по крайней мере 30 селенопротеинов, кодируемых 25 генами, которые содержат 21 st аминокислот селеноцистеина в их активном центре [6].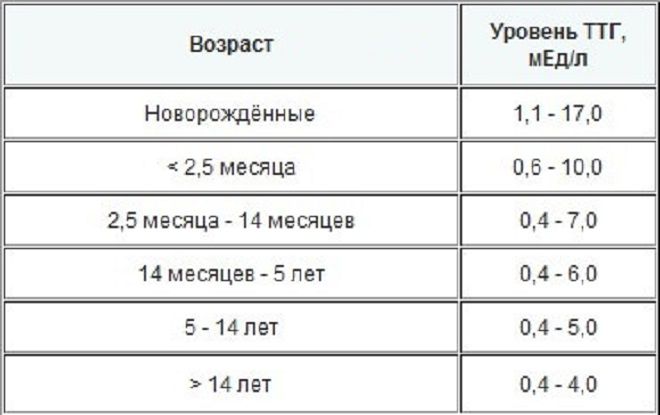 Существенная роль селенопротеинов заключается в их участии в деградации пероксидов, клеточной окислительно-восстановительной регуляции и регуляции транскрипции, дейодировании тироидных гормонов и сперматогенезе [7, 8].Основными селенопротеинами, экспрессируемыми в щитовидной железе, являются глутатионпероксидазы (GPX), тиоредоксинредуктаза (TRs) и дейодиназы (Ds) [9, 10]. Процесс йодирования тиреоглобулина (Tg) катализируется селеноферментной тироидпероксидазой (TPO), что требует более высокой концентрации пероксида водорода (h3O2), генерируемого тироцитами [11, 12]. Селеноферменты GPX предотвращают перекисное окисление липидов и защищают клеточные мембраны от окислительного повреждения. GPX1 является одним из наиболее распространенных селеноферментов и очень чувствителен к дефициту селена [13, 14].
Существенная роль селенопротеинов заключается в их участии в деградации пероксидов, клеточной окислительно-восстановительной регуляции и регуляции транскрипции, дейодировании тироидных гормонов и сперматогенезе [7, 8].Основными селенопротеинами, экспрессируемыми в щитовидной железе, являются глутатионпероксидазы (GPX), тиоредоксинредуктаза (TRs) и дейодиназы (Ds) [9, 10]. Процесс йодирования тиреоглобулина (Tg) катализируется селеноферментной тироидпероксидазой (TPO), что требует более высокой концентрации пероксида водорода (h3O2), генерируемого тироцитами [11, 12]. Селеноферменты GPX предотвращают перекисное окисление липидов и защищают клеточные мембраны от окислительного повреждения. GPX1 является одним из наиболее распространенных селеноферментов и очень чувствителен к дефициту селена [13, 14].
Селеноферменты дейодиназы присутствуют в щитовидной железе и во всех тканях организма [15]. На клеточном уровне передача сигналов тироидных гормонов может изменяться из-за локальной активации и инактивации тироидных гормонов через пути дейодирования внутри клеток-мишеней [16-18]. Дейодиназа 1 типа (D1) и дейодиназа 2 типа (D2) увеличивают клеточную активность щитовидной железы, превращая прогормон Т4 в активный Т3, тогда как дейодиназа 3 типа (D3) снижает клеточную активность щитовидной железы, превращая Т4 в обратный Т3, а Т3 — до 3 , 3′-дийодтиронин (Т2) [19, 20].Эти пути контролируют биодоступность и биоактивность тироидных гормонов на различных уровнях клеточной организации, и их влияние гораздо менее изучено [21].
Дейодиназа 1 типа (D1) и дейодиназа 2 типа (D2) увеличивают клеточную активность щитовидной железы, превращая прогормон Т4 в активный Т3, тогда как дейодиназа 3 типа (D3) снижает клеточную активность щитовидной железы, превращая Т4 в обратный Т3, а Т3 — до 3 , 3′-дийодтиронин (Т2) [19, 20].Эти пути контролируют биодоступность и биоактивность тироидных гормонов на различных уровнях клеточной организации, и их влияние гораздо менее изучено [21].
Селен действует как антиоксидант в плазме и внеклеточной жидкости, где селен в виде аминокислоты селеноцистеина включается в селенопротеин P и связывается с альбумином в виде селенометионина (SeMet) [22, 23]. Печень секретирует большую часть селенопротеидов и является основным местом метаболизма селена и гомеостаза.
Селенопротеин P (SEPP1) и GPX3 присутствуют в плазме человека и могут использоваться в качестве биомаркера селенового нутритивного статуса [24]. Измерения SEPP1 и GPX3 в плазме могут определить риск дефицита питательных веществ селена. Согласно Xia и соавторам [25], SEPP1 является лучшим биомаркером плазмы, потому что его оптимизация требует большего потребления селена, чем активность GPX3. При дефиците селена синтез некоторых селеноферментов, таких как глутатионпероксидаза, имеет приоритет над синтезом других [26, 27].Изменения статуса селена могут влиять на иммунный ответ, нейродегенерацию, сердечно-сосудистые заболевания и рак [28].
Согласно Xia и соавторам [25], SEPP1 является лучшим биомаркером плазмы, потому что его оптимизация требует большего потребления селена, чем активность GPX3. При дефиците селена синтез некоторых селеноферментов, таких как глутатионпероксидаза, имеет приоритет над синтезом других [26, 27].Изменения статуса селена могут влиять на иммунный ответ, нейродегенерацию, сердечно-сосудистые заболевания и рак [28].
Потребление селена населением Новой Зеландии
Согласно исследованию питания Новой Зеландии за 2008/09 год (NZANS), в котором была собрана информация от 4721 взрослого новозеландца в возрасте 15 лет и старше, потребление селена увеличилось с 1997 по 2008/09 год. Потребление Se оставалось недостаточным примерно для одной трети мужчин (31,5%) и более половины (58.2%) женщин [29]. Среднее обычное дневное потребление селена составляло 67,0 мкг для мужчин и 47,1 мкг для женщин. Пожилое население, как мужчины, так и женщины в возрасте от 71 года (52,0 мкг и 39,5 мкг соответственно), и женщины в возрасте 15–18 лет (38,7 мкг) потребляли меньше селена, чем мужчины и женщины в возрасте 31-50 лет (78,0 мкг). и 51,9 мкг соответственно). В Новой Зеландии рекомендуется потребление селена в среднем 60 мкг в день для мужчин и 53 мкг в день для женщин, чтобы добиться максимальной активности GPX в плазме или эритроцитах [30].
и 51,9 мкг соответственно). В Новой Зеландии рекомендуется потребление селена в среднем 60 мкг в день для мужчин и 53 мкг в день для женщин, чтобы добиться максимальной активности GPX в плазме или эритроцитах [30].
Основным источником селена в Новой Зеландии является хлеб (15%), за ним следуют рыба и морепродукты (12%) и птица (10%). Потребление Se в Новой Зеландии улучшилось после увеличения импорта австралийской и другой импортной пшеницы с высоким содержанием Se. Фрукты, овощи и зерновые, выращиваемые в Новой Зеландии, содержат более низкие уровни селена, чем растительные продукты из других стран с более высоким содержанием селена в почве [31, 32].
Основная цель исследования заключалась в том, чтобы определить различия в гормональном статусе (ТТГ, Т3 и Т4) между здоровыми участниками и участниками с тиреоидитом Хашимото.Вторичной целью исследования была оценка состояния питания Se и его взаимосвязи с уровнями гормонов щитовидной железы в сыворотке крови как в контрольной группе, так и в группе с гипотиреозом, принимавшей лекарства с L-тироксином.
Пациенты и метод
Это исследование является пилотным, перекрестным и наблюдательным. Участников исследования разделили на две группы: контрольную группу со здоровыми участниками и группу женщин с тиреоидитом Хашимото (HT), принимавших L-тироксин.Никаких изменений в распорядке дня участников не требовалось. Селен в плазме, ТТГ, Т4, Т3, креатинин и е-СКФ (скорость клубочковой фильтрации) определяли у женщин в обеих группах и сравнивали с золотыми стандартами. ТТГ, Т3 и Т4 в плазме измеряли с помощью метода конкурентных иммуноанализов лабораторией LabTests в Окленде. Селен в сыворотке измеряли с помощью масс-спектрометрии клеток с индуктивно связанной плазмой и динамической реакцией в Canterbury Health Laboratories в Крайстчерче, Новая Зеландия.Данных об антителах к тиреопероксидазе (анти-ТПО) у женщин с ГТ не было.
Статистический анализ
Данные были проанализированы с помощью SPSS для Windows (версия 22. 0, SPSS Inc., Чикаго, Иллинойс, США). Из-за небольшого размера выборки для анализа данных использовались непараметрические тесты. Описательная статистика и корреляционный анализ использовались для определения взаимосвязей между переменными. Результаты концентраций содержимого плазмы выражали как среднее ± стандартное отклонение.Значения с p <0,05 были приняты за достоверные.
0, SPSS Inc., Чикаго, Иллинойс, США). Из-за небольшого размера выборки для анализа данных использовались непараметрические тесты. Описательная статистика и корреляционный анализ использовались для определения взаимосвязей между переменными. Результаты концентраций содержимого плазмы выражали как среднее ± стандартное отклонение.Значения с p <0,05 были приняты за достоверные.
Результаты
Выборка исследования состояла из восьми женщин с ГТ, принимавших L-левотироксин, и 12 женщин с хорошим здоровьем в контрольной группе. Две женщины с диагнозом субклинический гипотиреоз были исключены из статистического анализа данных. Женщины с ГТ были старше, имели более низкий уровень ТТГ в плазме, более низкое соотношение Т3 / Т4 и более высокие уровни Т4 и селена (Таблица 1). Уровни Т3 в плазме были практически идентичны в обеих группах.Значения креатинина и е-СКФ находились в оптимальном диапазоне в обеих группах.
Таблица 1.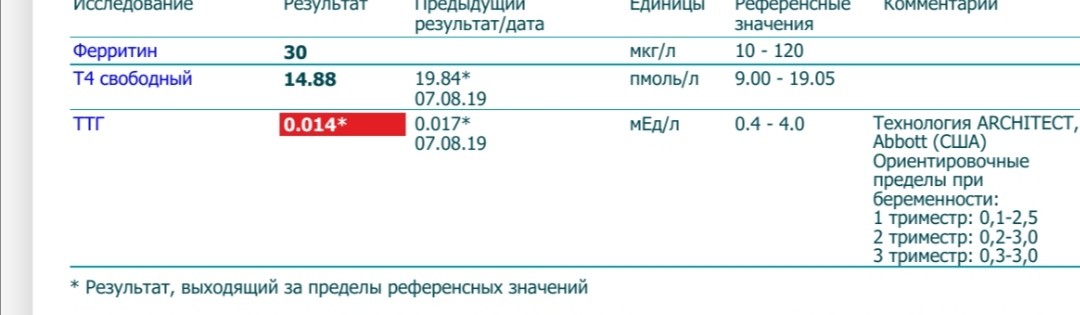 Описательная статистика (среднее ± стандартное отклонение)
Описательная статистика (среднее ± стандартное отклонение)
Контрольная группа n = 13 | Группа по лекарствам n = 8 | ||||
Среднее ± SD | Диапазон | Среднее ± SD | Диапазон | ||
Возраст | 52.69 ± 7,39 | 37-64 | 58,00 ± 6,74 | 48-65 | |
Диапазон значений | |||||
TSH | 0,30 — 4,00 мМЕ / л | 2. | 1,40 — 2,90 | 1,55 ± 1,02 | 0,63–3,30 |
T4 | 10,0 -20,0 пмоль / л | 14,61 ± 1,44 | 12.00-17.00 | 15.50 ± 1,41 | 14.00-18.00 |
T3 | 3,0 — 6,5 пмоль / л | 4,76 ± 0,58 | 3.90 — 6.10 | 4,46 ± 0,72 | 3,50 — 6,00 |
Соотношение T3 / T4 | 0.30 — 0,325 | 0,33 ± 0,05 | 0,26 -0,44 | 0,29 ± 0,06 | 0,23-0,43 |
Селен | 0,45 — 1,40 мкмоль / л | 1,28 ± 0,15 | 1. | 1,35 ± 0,17 | 1,16 — 1,69 |
Креатинин | 45-90 мкмоль / л | 67,69 ± 8,66 | 51,00 — 82,00 | 66,37 ± 10,36 | 49.00-84.00 |
e-GFR | > 90 мл / мин / 1,73 м2 | 85,69 ± 6,55 | 69,00 — 90,00 | 84,37 ± 9,47 | 64.00-90.00 |
Наблюдалась значимая положительная взаимосвязь между возрастом и T4 (p <0.01, ро Спирмена = 0,926 **), а также Т3 и селен (p <0,02, ро Спирмена = 0,778 *) у женщин с гипотиреозом. Кроме того, была положительная взаимосвязь между Т3 и соотношением Т3 / Т4 (p <0,01, rho Спирмена = 0,794 *). Значительная отрицательная связь между креатинином и e-СКФ (p <0,007, rho Спирмена = -0,851 **) была выявлена в группе гипотиреоза и контрольной группе (p <0,000, rho Спирмена = -0,843 **).
Кроме того, была положительная взаимосвязь между Т3 и соотношением Т3 / Т4 (p <0,01, rho Спирмена = 0,794 *). Значительная отрицательная связь между креатинином и e-СКФ (p <0,007, rho Спирмена = -0,851 **) была выявлена в группе гипотиреоза и контрольной группе (p <0,000, rho Спирмена = -0,843 **).
В контрольной группе наблюдалась значимая положительная взаимосвязь между Т3 и соотношением Т3 / Т4 (p <0.008, rho Спирмена = 0,701 **) и значимая положительная взаимосвязь между T4 и соотношением T3 / T4 (p <0,03, rho Спирмена = 0,600 *) (Таблица 2).
Таблица 2. Связь между переменными в группе гипотиреоза (ро Спирмена)
Возраст | ТШ | T3 | Т4 | Селен | Креатинин | GFR | ||
TSH | -. | |||||||
. 217 | ||||||||
T3 | -.066 | .228 | ||||||
. | .588 | |||||||
T4 | .926 ** | -.442 | -.173 | |||||
.001 | .273 | .682 | ||||||
Селен | . | .381 | .778 * | . 147 | ||||
.713 | .352 | .023 | .728 | |||||
Креатинин | -.476 | -.120 | -.313 | -.395 | -. | |||
. 233 | . 778 | .450 | .333 | .333 | ||||
GFR | .000 | . 518 | . 535 | -.070 | .546 | -.851 ** | ||
1. | . 188 | . 172 | . 869 | . 162 | .007 | |||
T3T4ratio | -.606 | .422 | .794 * | -.671 | .398 | .085 | .331 | |
.111 | . 298 | .019 | .069 | . | . 842 | .423 | ||
Значения переменных как для контрольной группы, так и для группы гипотиреоза, принимающей лекарства, были распределены на 10 -й , 25 -й , 50 -й и 75 -й процентили (Таблица 3).
Таблица 3. Значения переменных, распределенных по процентилям в обеих группах
* Важные выводы **. Корреляция значима на уровне 0,01 (двусторонний). |
*. Корреляция значима на уровне 0,05 (двусторонний). |
Процентили | 10 -я | 25 -я | 50 -я | 75 -я | 90 -я |
Группа гипотиреоза на лечении L-тироксином | |||||
Возраст | 48. | 51,00 | 59,50 | 64,00 | |
TSH | 0,63 | 0,71 | 1,25 | 2.57 | |
T3 | 3,5 * | 4,10 | 4,35 | 4,72 | |
T4 | 14.00 * | 14,25 | 15,00 | 16,75 * | |
Соотношение T3 / T4 | 0,23 | 0,24 | 0,28 * | 0. | |
Селен | 1,16 * | 1,23 | 1,29 | 1,46 | |
Контрольная группа | |||||
Возраст | 40.60 | 46,50 | 54,00 | 58,50 | 62,80 |
TSH | 1,44 | 1,70 | 2.10 | 2,22 | 2,74 |
T3 | 4,02 | 4,20 | 4,90 | 5,10 | 5. |
T4 | 12,40 | 14,00 | 14,00 | 16,00 * | 16.60 |
Соотношение T3 / T4 | 0.26 | 0,28 | 0,34 * | 0,35 * | 0,41 |
Селен | 1.04 | 1,14 | 1.29 | 1,38 | 1,51 |
Обсуждение
В этом исследовании с относительно небольшим размером выборки (n꞊ 23) участниками были европейские женщины со средним возрастом 53,50 ± 7,76 в контрольной группе и 56,33 ± 7,16 в группе женщин с длительной АГ (таблица 1).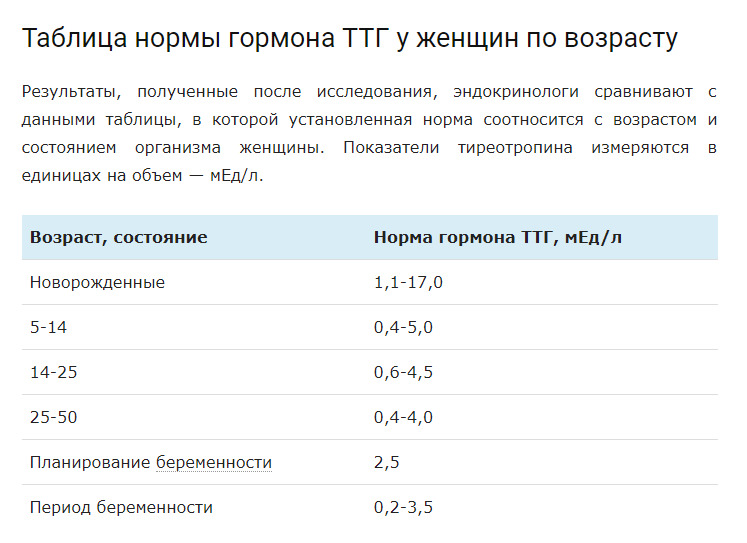 Две женщины с субклиническим гипотиреозом были исключены из анализа данных.Уровни Т3 и Т4 в плазме находились в оптимальном диапазоне, тогда как уровни ТТГ в плазме составляли 10 мМЕ / л и 4,7 мМЕ / л соответственно. Соответственно, субклинический гипотиреоз характеризуется нормальным уровнем Т3 и Т4 в плазме и повышенным ТТГ [33, 34]. Эксперты согласны с тем, что субклинический гипотиреоз — это ранняя легкая недостаточность функции щитовидной железы [35, 36]. Гормональный фон, связанный с субклиническим гипотиреозом, представляет собой компенсированное состояние, при котором высокий уровень ТТГ в плазме способствует поддержанию нормального уровня гормонов щитовидной железы.Стандартным препаратом при субклиническом гипотиреозе и пожизненном лечении гипотиреоза является заместительная гормональная терапия однократной суточной дозой L-тироксина [37]. По данным Американской тироидной ассоциации (ATA), цель терапии L-тироксином — восстановить клинически и биохимически эутиреоидное состояние у пациентов.
Две женщины с субклиническим гипотиреозом были исключены из анализа данных.Уровни Т3 и Т4 в плазме находились в оптимальном диапазоне, тогда как уровни ТТГ в плазме составляли 10 мМЕ / л и 4,7 мМЕ / л соответственно. Соответственно, субклинический гипотиреоз характеризуется нормальным уровнем Т3 и Т4 в плазме и повышенным ТТГ [33, 34]. Эксперты согласны с тем, что субклинический гипотиреоз — это ранняя легкая недостаточность функции щитовидной железы [35, 36]. Гормональный фон, связанный с субклиническим гипотиреозом, представляет собой компенсированное состояние, при котором высокий уровень ТТГ в плазме способствует поддержанию нормального уровня гормонов щитовидной железы.Стандартным препаратом при субклиническом гипотиреозе и пожизненном лечении гипотиреоза является заместительная гормональная терапия однократной суточной дозой L-тироксина [37]. По данным Американской тироидной ассоциации (ATA), цель терапии L-тироксином — восстановить клинически и биохимически эутиреоидное состояние у пациентов. Обычная доза левотироксина составляет от 1,6 до 1,8 мкг / кг в день, тогда как пожилым пациентам требуется меньшая доза — 1 мкг / кг в день или даже меньше, в зависимости от возраста, веса и сердечного статуса.
Обычная доза левотироксина составляет от 1,6 до 1,8 мкг / кг в день, тогда как пожилым пациентам требуется меньшая доза — 1 мкг / кг в день или даже меньше, в зависимости от возраста, веса и сердечного статуса.
Результаты исследования показали, что уровни ТТГ, Т4 и Т3 в плазме, а также соотношения Т3 / Т4 между двумя группами различались. Средние уровни ТТГ в плазме были немного ниже у женщин с ГТ, составляя 1,55 ± 1,02 и 2,06 ± 0,41 соответственно, хотя ATA рекомендовала стремиться к ТТГ в нижней половине нормального диапазона (0,4-4,5 мМЕ / л). , около 2,5 мМЕ / л у пациентов с первичным гипотиреозом [38]. Уровни ТТГ двух участников исследования были ближе к нижнему пределу нормального диапазона, равному 0.63 млU / л и 0,81 млU / л соответственно (менее 0,1 мМЕ / л), которые были приписаны чрезмерному лечению L-тироксином. Исследования доказали, что постоянное поддержание уровня ТТГ ниже оптимального референсного диапазона может быть связано с фибрилляцией предсердий, остеопорозом и переломами костей [39–41]. С другой стороны, поддержание уровня ТТГ выше нормы может вызвать развитие метаболической дисфункции [42]. Первоначальное лечение L-тироксином при гипотиреозе требует контроля уровня ТТГ каждые шесть-восемь недель с корректировкой дозировки L-тироксина [43].Как только ТТГ стабилизируется, необходимо проводить полугодовое или ежегодное тестирование [44].
С другой стороны, поддержание уровня ТТГ выше нормы может вызвать развитие метаболической дисфункции [42]. Первоначальное лечение L-тироксином при гипотиреозе требует контроля уровня ТТГ каждые шесть-восемь недель с корректировкой дозировки L-тироксина [43].Как только ТТГ стабилизируется, необходимо проводить полугодовое или ежегодное тестирование [44].
Кроме того, средние уровни Т3 в плазме были почти идентичными в обеих группах, составляя 4,76 ± 0,58 и 4,46 ± 0,72 соответственно, тогда как уровни Т4 в плазме были значительно выше в группе гипотиреоза, чем в контрольной группе (15,50 ± 1,41 и 14,61 ± 1,44 соответственно. ). Повышенный Т4 и небольшое снижение ТТГ в плазме (1,55 ± 1,02) и соотношения Т3 / Т4 (0,29 ± 0,06 и 0,33 ± 0,05 соответственно) в группе гипотиреоза указывает на то, что для достижения нормального уровня Т3 более высокие дозы L Пациентам следует назначать -тироксин [45].В подтверждение этих результатов исследование Mortoglou и Candiloros (2004) продемонстрировало аналогичный сценарий случая, когда пациентам с гипотиреозом давали более высокую дозу L-тироксина для поддержания среднего уровня Т3 в плазме [46].
У женщин с ГТ наблюдалась значимая положительная взаимосвязь между селеном в плазме и Т3 ( p <0,05, а коэффициент Спирмена был 0,778). В этой связи обе переменные имеют тенденцию к увеличению, а это означает, что производство Т3 будет увеличиваться, если уровни селена в плазме увеличиваются.Дефицит селена подавляет превращение Т4 в Т3 под действием селеноферментных дейодиназ I и II типа. В процессе дейодирования селен в форме SeCys играет доминирующую роль, что подчеркивает зависимость активности дейодиназ 1 и 2 типов от уровней селена в плазме [47]. Однако в настоящем исследовании исходные уровни селена в плазме были выше у женщин с ГТ (1,35 ± 0,17), чем в контрольной группе (1,28 ± 0,15), а также были выше, чем исходные уровни селена, рекомендованные Томсоном и соавторами [ 48].Согласно Thomson и др. . Уровни селена в плазме 0,82–0,90 мкгмоль / л должны быть достаточными для оптимального функционирования дейодиназ. Однако Karunasinghe et al. [49] предположили, что основная потребность в селене может варьироваться в зависимости от генотипа для ряда вариаций селенопротеиновых генов, предполагая, что эффективное потребление селена с пищей для одного человека может отличаться от такового для других. При отсутствии этой информации рекомендуемые уровни селена в плазме должны быть в пределах 1.27 — 1,90 мкмоль / л.
[49] предположили, что основная потребность в селене может варьироваться в зависимости от генотипа для ряда вариаций селенопротеиновых генов, предполагая, что эффективное потребление селена с пищей для одного человека может отличаться от такового для других. При отсутствии этой информации рекомендуемые уровни селена в плазме должны быть в пределах 1.27 — 1,90 мкмоль / л.
в плазме были основаны на измерении SEPP1, который является наиболее надежным биомаркером селенового статуса, и его полная экспрессия требует значительно более высокой дозы селена [50]. SEPP1 и селеноферментные дейодиназы занимают высокое место в иерархии поставок селена, и на них не может влиять маргинальный дефицит селена, как у GPx [51]. Максимальная активность селенофермента достигается при уровне селена в крови выше 1,27 мкмоль / л, или, согласно недавнему исследованию Rayman [52], концентрация селена в плазме находится в диапазоне 1.От 6 до 1,9 мкмоль / л считаются оптимальными для щитовидной железы и хорошего здоровья в целом.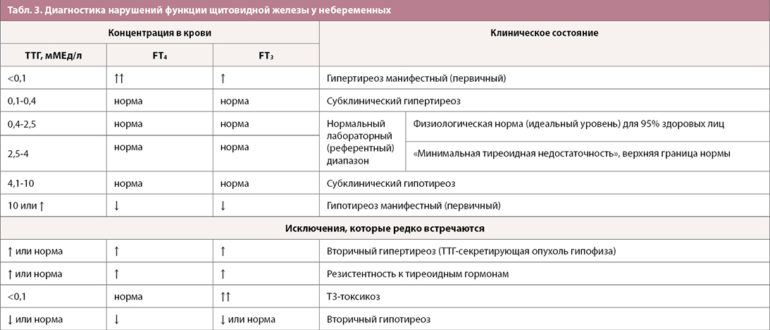 Однако в отношении оптимальных уровней селена в плазме существует согласие между этими двумя исследованиями, проведенными Rayman (2012) и Karunasinghe с соавторами (2012). Уровни селена в плазме были немного выше в группе гипотиреоза, чем в контрольной группе, при этом средние уровни селена в плазме были ближе к нижнему пределу оптимального диапазона (1,28 ± 0,15 и 1,35 ± 0,17 соответственно), что можно объяснить различной диетой в пострадавшие.
Однако в отношении оптимальных уровней селена в плазме существует согласие между этими двумя исследованиями, проведенными Rayman (2012) и Karunasinghe с соавторами (2012). Уровни селена в плазме были немного выше в группе гипотиреоза, чем в контрольной группе, при этом средние уровни селена в плазме были ближе к нижнему пределу оптимального диапазона (1,28 ± 0,15 и 1,35 ± 0,17 соответственно), что можно объяснить различной диетой в пострадавшие.
Тиреоидит Хашимото является частью спектра аутоиммунных заболеваний щитовидной железы, которые группируются в семьях [53]. Он демонстрирует организованную лимфоцитарную инфильтрацию, которая с возрастом приводит к апоптозу тироцитов и фиброзу щитовидной железы [54]. Это привлекает внимание к женщинам с гипотиреозом в исследовании, которые были старше, чем женщины в контрольной группе, и у которых было соотношение ТТГ, Т3 и Т3 / Т4 (из-за высокого Т4), а также уровень селена менее 10% (< 10 -е ) женщин контрольной группы. Это открытие указывает на то, что для поддержания адекватных уровней Т3 в качестве заместительной терапии следует назначать более высокие дозы L-тироксина (Т4) (Таблица 3). Плохое содержание селена на уровне 10 -го процентиля 1,16 мкмоль / л, что ниже рекомендуемого, связано с ослабленным процессом периферического дейодирования, повышенным Т4 и более низким соотношением Т3 / Т4. Добавки селена с селенитом селена или SeMet могут быть эффективными в замедлении прогрессирования аутоиммунного тиреоидита (АИТ), что отражается снижением аутоантител в сыворотке с большим или меньшим успехом [55-59].
Это открытие указывает на то, что для поддержания адекватных уровней Т3 в качестве заместительной терапии следует назначать более высокие дозы L-тироксина (Т4) (Таблица 3). Плохое содержание селена на уровне 10 -го процентиля 1,16 мкмоль / л, что ниже рекомендуемого, связано с ослабленным процессом периферического дейодирования, повышенным Т4 и более низким соотношением Т3 / Т4. Добавки селена с селенитом селена или SeMet могут быть эффективными в замедлении прогрессирования аутоиммунного тиреоидита (АИТ), что отражается снижением аутоантител в сыворотке с большим или меньшим успехом [55-59].
Что касается чисто физиологической взаимосвязи между креатинином и СКФ, то оценки СКФ, основанные на креатинине сыворотки, обычно используются для оценки функции почек и / или экскреции креатинина [60]. Однако существует связь между сывороточным креатинином и генами СКФ с хромосомой 2, что означает, что эта область содержит ген, влияющий на фенотипические вариации сывороточного креатинина и СКФ [61].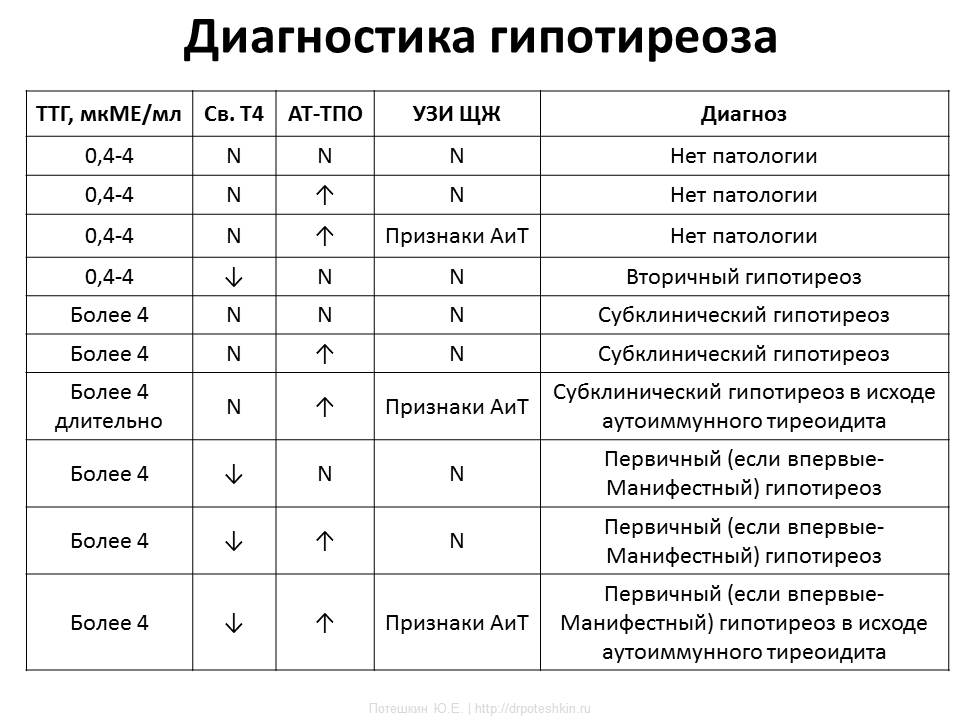
Выводы
Это исследование имело относительно небольшой размер выборки и дало важные результаты.У женщин с тиреоидитом Хашимото была выявлена значимая взаимосвязь между Т3 и селеном, а также возрастом и Т4. В обеих группах наблюдался умеренный дефицит селена, от которого страдали женщины с гипотиреозом. Нарушение периферического дейодирования у женщин с гипотиреозом требовало увеличения дозировки L-тироксина, что, в свою очередь, увеличивало уровень Т4 и снижало ТТГ гипофиза, чтобы достичь желаемого уровня Т3. Недавние исследования показали, что для повышения уровня селена в плазме добавка селена с селенометионином (SeMet) или селенитом селена может замедлить процесс разрушения щитовидной железы аутоантителами щитовидной железы при тиреоидите Хашимото за счет уменьшения аутоиммунного воспаления.Процесс добавления селена имеет переменные показатели успеха в Новой Зеландии и во всем мире. Следовательно, необходимы дальнейшие исследования.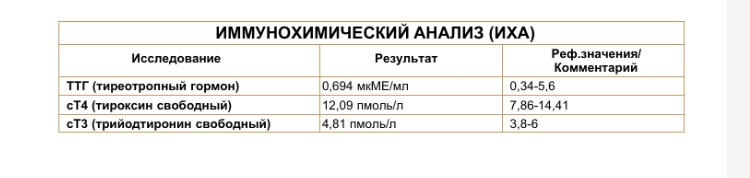
Экспертные группы не рекомендуют скрининг ТТГ на субклинический гипотиреоз среди населения в целом, хотя ATA рекомендовала скрининг у всех взрослых, начиная с 35 лет, включая женщин фертильного возраста, и каждые 5 лет в дальнейшем, чтобы отсрочить развитие явный гипотиреоз и его заболеваемость.
Благодарности
Я очень благодарен за финансовую поддержку, которую я получил от Школы межпрофессиональных исследований в области здравоохранения, и за помощь моих коллег в наборе участников.Все участники исследования прочитали Информационный лист участников и дали письменное согласие. Комитет по этике Оклендского технологического университета (AUTEC) № 13/17, согласно Хельсинкской декларации, одобрил протокол исследования.
Список литературы
- Гиббонс В., Конаглен Дж. В., Лиллис С., Нарас В., Лоуренсон Р. (2008) Эпидемиология заболеваний щитовидной железы в общей практике Гамильтона (Новая Зеландия).
 Aust N Z J Public Health 32: 421-423.[Crossref]
Aust N Z J Public Health 32: 421-423.[Crossref] - Schimmel M, Utiger RD (1977) Тиреоидальное и периферическое производство гормонов щитовидной железы: обзор последних результатов и их клинического значения. Анн Интер Мед 87: 760-768. [Crossref]
- Fonseca TL, Correa-Medina M, Campos MP, Wittmann G, Werneck-de-Castro JP, et al. (2013) Координация выработки Т3 в гипоталамусе и гипофизе регулирует экспрессию ТТГ. J Clin Invest 123: 1492-1500. [Crossref]
- Aaseth J, Frey H, Glattre E, Norheim G, Ringstad J, et al.(1990) Концентрация селена в щитовидной железе человека. Biol Trace Elem Res 24: 147-152. [Crossref]
- Brown KM, Arthur JR (2001) Селен, селенопротеины и здоровье человека: обзор. Public Health Nutr 4: 593-599. [Crossref]
- Крюков Г.В., Кастеллано С., Новоселов С.В., Лобанов А.В., Зехтаб О.
 и др. (2003) Характеристика селенопротеомов млекопитающих. Наука 300: 1439-1443. [Crossref]
и др. (2003) Характеристика селенопротеомов млекопитающих. Наука 300: 1439-1443. [Crossref] - Köhrle J, Jakob F, Contempré B, Dumont JE (2005) Селен, щитовидная железа и эндокринная система. Endocr Ред. 26: 944-984. [Crossref]
- Rayman MP (2009) Селенопротеины и здоровье человека: выводы из эпидемиологических данных. Biochim Biophys Acta 1790: 1533-1540. [Crossref]
- Кастеллано С., Лобанов А.В., Чаппл С., Новоселов С.В., Альбрехт М. и др. (2005) Разнообразие и функциональная пластичность селенопротеинов эукариот: идентификация и характеристика семейства SelJ. P Natl Acad Sci USA 102: 16188-16193.[Crossref]
- Папп Л.В., Лу Дж., Холмгрен А., Ханна К.К. (2007) От селена до селенопротеинов: синтез, идентичность и их роль в здоровье человека. Антиоксиданты и редокс сигн. 9: 775-806. [Crossref]
- Beckett GJ, Arthur JR (2005) Селен и эндокринные системы.
 Дж. Эндокринол 184: 455-465. [Crossref]
Дж. Эндокринол 184: 455-465. [Crossref] - Duntas LH (2010) Селен и щитовидная железа: тесная связь. J Clin Endocrinol Metab 95: 5180-5188. [Crossref]
- Rayman MP (2000) Важность селена для здоровья человека. Ланцет 356: 233-241. [Crossref]
- Марджис Р., Дананд К., Тейшейра Ф. К. и Марджис-Пинейро М. 2008. Семейство глутатионпероксидазы — эволюционный обзор. Febs Journal, 275, 3959-3970.
- Геребен Б., Завацкий А.М., Рибич С., Ким Б.В., Хуанг С.А. и др. (2008) Клеточные и молекулярные основы передачи сигналов гормона щитовидной железы, регулируемого дейодиназой 1. Обзоры эндокринной системы 29: 898-938. [Crossref]
- Bianco AC, Kim BW (2006) Дейодиназы: последствия местного контроля действия гормонов щитовидной железы. Дж. Клин Инвест 116: 2571-2579. [Crossref]
- Silva JE, Dick TE, Larsen PR (1978) Вклад местного тканевого монодейодирования тироксина в ядерный 3, 5, 3′-трийодтиронин в гипофизе, печени и почках эутиреоидных крыс.
 Эндокринология 103: 1196-1207.[Crossref]
Эндокринология 103: 1196-1207.[Crossref] - Ларсен П.Р., Сильва Дж.Э., Каплан М.М. (1981) Взаимосвязь между циркулирующими и внутриклеточными гормонами щитовидной железы: физиологические и клинические последствия. Endocr Ред. 2: 87-102. [Crossref]
- Геребен Б., Завацкий А.М., Рибич С., Ким Б.В., Хуанг С.А. и др. (2008) Клеточные и молекулярные основы передачи сигналов гормона щитовидной железы, регулируемого дейодиназой. Endocr Ред. 29: 898-938. [Crossref]
- Holtorf K (2014) Конверсия периферических гормонов щитовидной железы и ее влияние на ТТГ и метаболическую активность. J Restor Med 3: 30-52.
- Little AG (2016) Обзор периферических уровней регуляции тироидных гормонов. J. Comp Physiol B 186: 677-688. [Crossref]
- Schmutzler C, Gotthardt I, Hofmann PJ, Radovic B, Kovacs G, et al. (2007) Разрушители эндокринной системы и щитовидная железа — комбинированный анализ потенциальных новых биомаркеров in vitro и in vivo.
 Environ Health Persp 115: 77. [Crossref]
Environ Health Persp 115: 77. [Crossref] - Whanger P (1998) Метаболизм селена у человека. Дж. TraceElem Exp Med 1: 227-240.
- Burk RF, Hill KE (2005) Селенопротеин P: внеклеточный белок с уникальными физическими характеристиками и ролью в гомеостазе селена. Annu Rev Nutr 25: 215-235. [Crossref]
- Xia Y, Hill KE, Li P, Xu J, Zhou D и др. (2010) Оптимизация селенопротеина Р и других биомаркеров селена в плазме для оценки потребности в питательных веществах селеном: плацебо-контролируемое двойное слепое исследование приема добавок селенометионина у китайских субъектов с дефицитом селена. Am J Clin Nutr 92: 525-531. [Crossref]
- Ривз М.А., Хоффманн П.Р. (2009) Селенопротеом человека: недавнее понимание функций и регуляции. Cell Mol Life Sci 66: 2457-2478. [Crossref]
- Combs GF Jr (2015) Биомаркеры статуса селена.
 Питательные вещества 7: 2209-2236. [Crossref]
Питательные вещества 7: 2209-2236. [Crossref] - Rayman MP (2005) Селен в профилактике рака: обзор доказательств и механизма действия. Proc Nutr Soc 64: 527-542. [Crossref]
- Университет Отаго и Министерство здравоохранения (2011 г.). В центре внимания — питание: основные выводы исследования питания взрослого населения Новой Зеландии за 2008/09 год. Веллингтон, Новая Зеландия.
- Rayman MP (2004) Использование дрожжей с высоким содержанием селена для повышения уровня селена: каковы результаты? Br J Nutr 92: 557-573. [Crossref]
- Mann J, Truswell S (2012) Основы питания человека, Oxford University Press.
- Thomson CD (2004) Оценка требований к селену и адекватность статуса селена: обзор. Eur J Clin Nutr 58: 391-402. [Crossref]
- Canaris GJ, Manowitz NR, Mayor G, Ridgway EC (2000) Исследование распространенности заболеваний щитовидной железы в Колорадо.
 Arch Intern Med 160: 526-534. [Crossref]
Arch Intern Med 160: 526-534. [Crossref] - Cooper DS, Biondi B (2012) Субклиническая болезнь щитовидной железы. Ланцет 379: 1142-1154.[Crossref]
- McDermott MT, Ridgway EC (2001) Субклинический гипотиреоз — это слабая тиреоидная недостаточность, которую необходимо лечить. J Clin Endocrinol Metab 86: 4585-4590. [Crossref]
- Surks MI, Ocampo E (1996) Субклиническая болезнь щитовидной железы. Am J Med 100: 217-223. [Crossref]
- Гарбер Дж. Р., Кобин Р. Х., Гариб Н., Хеннесси СП, Кляйн И. и др. (2012) Руководство по клинической практике гипотиреоза у взрослых: при поддержке Американской ассоциации клинических эндокринологов и Американской тироидной ассоциации. Щитовидная железа 22: 1200-1235. [Crossref]
- Chakera AJ, Pearce SH, Vaidya B (2012) Лечение первичного гипотиреоза: текущие подходы и будущие возможности.
 Drug Des Devel Ther 6: 1-11. [Crossref]
Drug Des Devel Ther 6: 1-11. [Crossref] - Галетта Ф., Франзони Ф., Фаллахи П., Токкини Л., Браччини Л. и др. (2008) Изменения вариабельности сердечного ритма и дисперсии QT у пациентов с явным гипотиреозом. Eur J Endocrinol 158: 85-90.[Crossref]
- Робертс К.Г., Ладенсон П.В. (2004) Гипотиреоз. Ланцет 363: 793-803. [Crossref]
- Boeving A, Paz-Filho G, Radominski RB, Graf H, Amaral de Carvalho G (2011) Целевые уровни тиреотропина с низким или высоким-нормальным уровнем во время лечения гипотиреоза: проспективное сравнительное исследование. Thyroid: J Am Thyroid Assoc 2: 355-360. [Crossref]
- Вайдья Б., Пирс SHS (2008) Управление гипотиреозом у взрослых. BMJ 337.
- Лаурберг П., Андерсен С., Педерсен И.Б., Карл А. (2005) Гипотиреоз у пожилых людей: патофизиология, диагностика и лечение. Наркотики и старение 22: 23-38.
 [Crossref]
[Crossref] - Pecina J, Bernard M, Furst J, Rohrer J (2012) Управление гипотиреозом: всегда ли необходима ежегодная проверка уровня ТТГ? J Fam Pract 6: E1-5. [Crossref]
- Mortoglou A, Candiloros H (2004) Отношение трийодтиронина к тироксину (T3 / T4) в сыворотке при различных заболеваниях щитовидной железы и после заместительной терапии левотироксином. Гормоны-Афины 3: 120-126. [Crossref]
- Carr D, McLeod DT, Parry G, Thornes HM (1988) Точная регулировка дозировки замещения тироксина: сравнение теста высвобождающего гормона тиреотрофина с использованием чувствительного анализа тиреотрофина с измерением свободных гормонов щитовидной железы и клинической оценкой. Clin Endocrinol 28: 325-333. [Crossref]
- Артур JR, Никол Ф., Беккет GJ (1990) Йодтиронин-5′-дейодиназа печени.Роль селена. Biochem J 272: 537-540. [Crossref]
- Thomson CD, McLachlan SK, Grant AM, Paterson E, Lillico AJ (2005) Влияние селена на статус щитовидной железы в популяции с маргинальным статусом селена и йода.
 British J Nutrition 94: 962-968.
British J Nutrition 94: 962-968. - Карунасингхе Н., Хан Д.Й., Чжу С., Ю Дж., Ланге К. и др. (2012) Сывороточный селен и однонуклеотидные полиморфизмы в генах селенопротеинов: взаимосвязь с маркерами окислительного стресса у мужчин из Окленда, Новая Зеландия. Гены и питание 7: 179-190. [Crossref]
- Бурк Р.Ф., Норсуорси Б.К., Хилл К.Е., Мотли А.К., Бирн Д.В. (2006) Влияние химической формы селена на биомаркеры плазмы в испытании высоких доз на людях. Cancer Epidem Biomar 15: 804-810. [Crossref]
- Thomson CD (2004) Потребление селена и йода и их статус в Новой Зеландии и Австралии. Brit J Nutr 9: 661-672. [Crossref]
- Rayman MP1 (2012) Селен и здоровье человека. Ланцет 379: 1256-1268. [Crossref]
- Weetman AP (2012) Иммунопатогенез хронического аутоиммунного тиреоидита через столетие после хашимото.
 Eur Thyroid J 243-250. [Crossref]
Eur Thyroid J 243-250. [Crossref] - Weetman A (2000) Хронический аутоиммунный тиреоидит. Щитовидная железа: фундаментальный и клинический текст. Филадельфия: Lippincott Williams & Wilkins, 721-32.
- Тулис К.А., Анастасилакис А.Д., Целлос Т.Г., Гулис Д.Г., Кувелас Д.и другие. (2010) Добавки селена в лечении тиреоидита Хашимото: систематический обзор и метаанализ. Thyroid, 20, 1163-1173. [Crossref]
- Thomson CD, Campbell JM, Miller J, Skeaff SA, Livingstone V (2009) Добавки селена и йода: влияние на функцию щитовидной железы у пожилых жителей Новой Зеландии. Am J Clin Nutr 90: 1038-1046. [Crossref]
- Turker O, Kumanlioglu K, Karapolat I, Dogan I. (2006) Лечение селеном при аутоиммунном тиреоидите: 9-месячное наблюдение с различными дозами. Дж. Эндокринол 190: 151-156. [Crossref]
- Gärtner R, Gasnier BCH, Dietrich JW, Krebs B, Angstwurm MWA и др.
 (2002) Добавление селена пациентам с аутоиммунным тиреоидитом снижает концентрацию антител к тироидной пероксидазе. J Clin Endocr Metab 87: 1687-1691. [Crossref]
(2002) Добавление селена пациентам с аутоиммунным тиреоидитом снижает концентрацию антител к тироидной пероксидазе. J Clin Endocr Metab 87: 1687-1691. [Crossref] - Караникас Г., Шуэц М., Контур С., Дуан Н., Коммата С. и др. (2008) Отсутствие иммунологической пользы селена у последовательных пациентов с аутоиммунным тиреоидитом. Thyroid: J Am Thyroid Assoc 18: 7-12. [Crossref]
- Inker LA, Schmid CH, Tighiouart H, Eckfeldt JH, Feldman HI, et al. (2012) Оценка скорости клубочковой фильтрации на основе сывороточного креатинина и цистатина C. New Engl J Med 367: 20-29.
- Hunt SC, Coon H, Hasstedt SJ, Cawthon RM, Camp NJ (2004) Связь сывороточного креатинина и скорости клубочковой фильтрации с хромосомой 2 в родословных Юты. Am J Hypertens 17: 511-515.[Crossref]
Гормон, стимулирующий щитовидную железу | Вы и ваши гормоны от Общества эндокринологов
Альтернативные названия тиреотропного гормона
ТШ; тиреотропин, тиреотрофин
Что такое тиреотропный гормон?
Гормон, стимулирующий щитовидную железу, вырабатывается и попадает в кровоток гипофизом.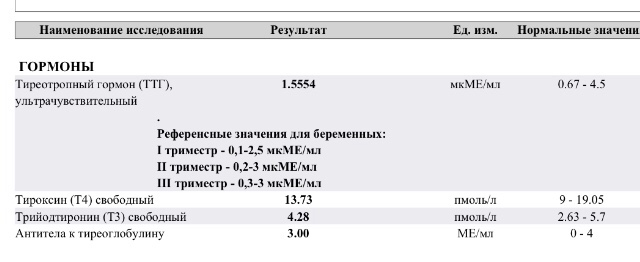 Он контролирует производство гормонов щитовидной железы, тироксина и трийодтиронина, щитовидной железой, связываясь с рецепторами, расположенными на клетках щитовидной железы.Тироксин и трийодтиронин необходимы для поддержания скорости метаболизма, работы сердца и пищеварительной системы, мышечного контроля, развития мозга и поддержания костей.
Он контролирует производство гормонов щитовидной железы, тироксина и трийодтиронина, щитовидной железой, связываясь с рецепторами, расположенными на клетках щитовидной железы.Тироксин и трийодтиронин необходимы для поддержания скорости метаболизма, работы сердца и пищеварительной системы, мышечного контроля, развития мозга и поддержания костей.
Как контролируется тиреотропный гормон?
Когда тиреотропный гормон связывается с рецептором на клетках щитовидной железы, это заставляет эти клетки производить тироксин и трийодтиронин и высвобождать их в кровоток. Эти гормоны негативно влияют на гипофиз и останавливают выработку тиреотропного гормона, если уровни тироксина и трийодтиронина слишком высоки.Они также отключают выработку гормона, называемого тиреотропин-рилизинг-гормоном. Этот гормон вырабатывается гипоталамусом, а также стимулирует гипофиз к выработке тиреотропного гормона.
Что произойдет, если у меня будет слишком много гормона, стимулирующего щитовидную железу?
Простой анализ крови может определить уровень гормона, стимулирующего щитовидную железу, в кровотоке. Если у человека слишком много, это может указывать на то, что его щитовидная железа не вырабатывает достаточно гормона щитовидной железы, то есть у него недостаточная активность щитовидной железы или гипотиреоз.Люди с недостаточной активностью щитовидной железы часто чувствуют себя вялыми, прибавляют в весе и чувствуют холод. Их щитовидная железа может увеличиваться, вызывая зоб. Лечение — это прием лекарств в виде таблеток для нормализации уровня гормонов щитовидной железы. Это также снижает количество стимулирующего гормона щитовидной железы в обращении. Особенно важно, чтобы беременные женщины получали правильное количество тиреотропного гормона и гормонов щитовидной железы, чтобы обеспечить здоровое развитие их детей.Гормон, стимулирующий щитовидную железу, является одним из гормонов, измеряемых у новорожденных. В редких случаях проблемы со стороны гипофиза или редкие генетические заболевания могут приводить к неадекватно высоким уровням тиреотропных гормонов и высоким уровням свободных гормонов щитовидной железы.
Если у человека слишком много, это может указывать на то, что его щитовидная железа не вырабатывает достаточно гормона щитовидной железы, то есть у него недостаточная активность щитовидной железы или гипотиреоз.Люди с недостаточной активностью щитовидной железы часто чувствуют себя вялыми, прибавляют в весе и чувствуют холод. Их щитовидная железа может увеличиваться, вызывая зоб. Лечение — это прием лекарств в виде таблеток для нормализации уровня гормонов щитовидной железы. Это также снижает количество стимулирующего гормона щитовидной железы в обращении. Особенно важно, чтобы беременные женщины получали правильное количество тиреотропного гормона и гормонов щитовидной железы, чтобы обеспечить здоровое развитие их детей.Гормон, стимулирующий щитовидную железу, является одним из гормонов, измеряемых у новорожденных. В редких случаях проблемы со стороны гипофиза или редкие генетические заболевания могут приводить к неадекватно высоким уровням тиреотропных гормонов и высоким уровням свободных гормонов щитовидной железы.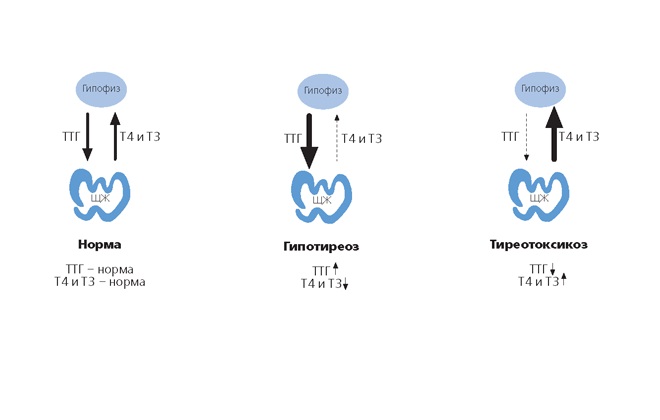
Что произойдет, если у меня слишком мало гормона, стимулирующего щитовидную железу?
Если у человека слишком мало гормона, стимулирующего щитовидную железу, наиболее вероятно, что его щитовидная железа вырабатывает слишком много гормона щитовидной железы, то есть у него повышенная активность щитовидной железы или гипертиреоз, который подавляет действие гормона, стимулирующего щитовидную железу.Люди с гиперактивной щитовидной железой имеют симптомы, противоположные тем, у которых есть гипотиреоз, то есть они теряют вес (несмотря на увеличение количества еды), чувствуют себя слишком горячими и могут испытывать учащенное сердцебиение или беспокойство. У них также может быть немного увеличенная щитовидная железа. Лечение — это лекарства в форме таблеток, которые снижают активность щитовидной железы и возвращают все уровни гормонов щитовидной железы в норму. В редких случаях проблемы с гипофизом могут также приводить к низкому уровню гормона, стимулирующего щитовидную железу, и низкому уровню свободных гормонов щитовидной железы.
Последний раз отзыв: март 2018
Выведение гормонов щитовидной железы и острый гипотиреоз
ВАЖНАЯ ИНФОРМАЦИЯ ПО БЕЗОПАСНОСТИ
Пациентам не следует использовать Thyrogen с радиоактивным йодом, если у них есть противопоказания к применению радиоактивного йода. Пожалуйста, проконсультируйтесь со своим врачом для получения списка противопоказаний для радиоактивного йода.
Тироген может вызывать серьезные побочные эффекты, в том числе:
Тироген-индуцированный гипертиреоз:
- Были сообщения о событиях, которые привели к смерти у пациентов, которые не перенесли операции по удалению щитовидной железы, а также у пациентов с раком щитовидной железы, который распространился на другие части тела.
- Пациенты старше 65 лет с большим количеством оставшейся ткани щитовидной железы после операции или с сердечными заболеваниями в анамнезе должны обсудить со своим врачом риски и преимущества тирогена.

- Тироген можно вводить в больнице пациентам с риском осложнений от введения тирогена.
Ход:
- С тех пор, как Thyrogen был впервые одобрен для использования, были сообщения о проблемах центральной нервной системы, таких как инсульт у молодых женщин, у которых больше шансов получить инсульт, и слабость на одной стороне тела.Связь между приемом THYROGEN и инсультом неизвестна. Пациенты должны оставаться гидратированными до лечения тирогеном.
Внезапное быстрое увеличение опухоли:
- Остатки ткани щитовидной железы после операции и раковые клетки, которые распространились на другие части тела, могут быстро расти и становиться болезненными после введения тирогена. Пациентам с раковыми клетками около трахеи, в центральной нервной системе или в легких может потребоваться лечение глюкокортикоидом (лекарство, помогающее предотвратить увеличение размера раковых клеток перед использованием тирогена.
 )
)
Риски, связанные с лечением радиойодом:
- Если ТИРОГЕН вводится с радиоактивным йодом (RAI), серьезные побочные эффекты RAI проявляются в этом комбинированном режиме. Пожалуйста, проконсультируйтесь со своим врачом для получения списка противопоказаний для радиоактивного йода.
ПОБОЧНЫЕ РЕАКЦИИ
В клинических исследованиях наиболее частыми побочными эффектами были тошнота и головная боль.
ИСПОЛЬЗОВАНИЕ В КОНКРЕТНЫХ ГРУППАХ ПАЦИЕНТОВ
Беременные пациентки: Немедленно сообщите об этом своему врачу в случае беременности.Если THYROGEN вводится с радиоактивным йодом, комбинированный режим не следует применять беременным женщинам. Тироген следует назначать беременной женщине только в том случае, если врач считает, что в этом есть явная необходимость.
Пациенты, кормящие грудью: Если ТИРОГЕН вводится с радиоактивным йодом, комбинированный режим не следует применять кормящим женщинам.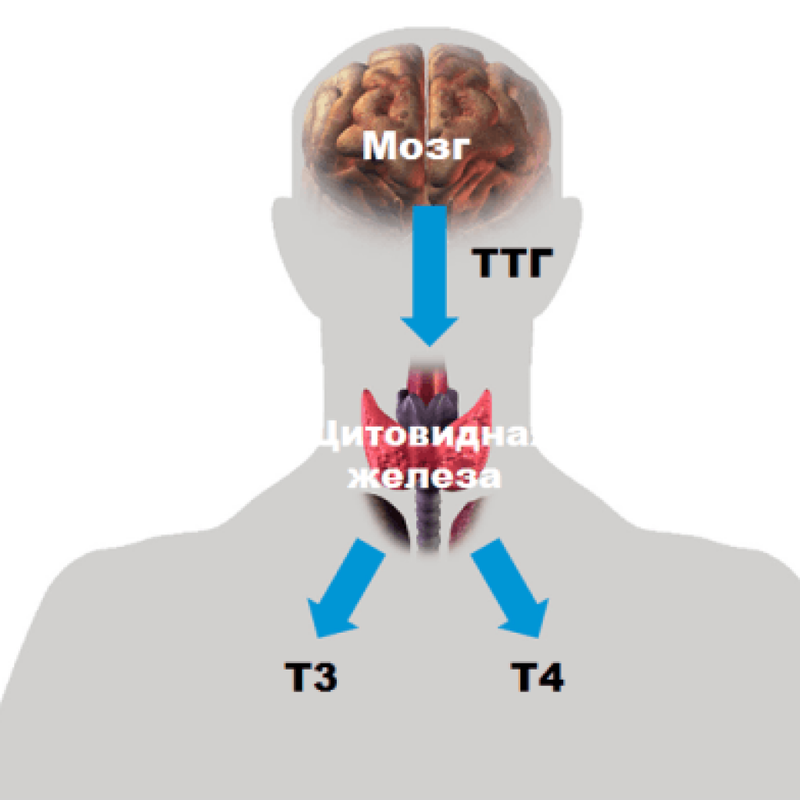 Неизвестно, может ли тироген появляться в материнском молоке. Кормящим женщинам следует обсудить преимущества и риски тирогена со своим врачом.
Неизвестно, может ли тироген появляться в материнском молоке. Кормящим женщинам следует обсудить преимущества и риски тирогена со своим врачом.
Дети: Безопасность и эффективность у маленьких пациентов (в возрасте до 18 лет) не установлены.
Пожилые люди: исследования не показывают разницы в безопасности и эффективности тирогена между взрослыми пациентами в возрасте до 65 лет и старше 65 лет.
Пациенты с заболеванием почек: Тироген выходит из организма гораздо медленнее у диализных пациентов и может приводить к более длительному повышению уровня ТТГ.
ПОКАЗАНИЯ И ИСПОЛЬЗОВАНИЕ
Тироген (тиреотропин альфа) используется для выявления заболеваний щитовидной железы путем тестирования крови на гормон, называемый тиреоглобулином, при последующем наблюдении за пациентами с определенным типом рака щитовидной железы, известным как хорошо дифференцированный рак щитовидной железы.Он используется с радиологическим тестом или без него с использованием формы йода.
Ограничения использования:
- Эффект тирогена на отдаленные исходы рака щитовидной железы не определен.
- Когда тироген используется для выявления рака щитовидной железы, есть шанс, что рак полностью или частично не будет обнаружен.
Тироген также используется, чтобы помочь пациентам подготовиться к лечению формой йода, называемой радиоактивным йодом, для удаления остатков ткани щитовидной железы у пациентов, перенесших операцию по удалению всей щитовидной железы у пациентов с хорошо дифференцированным раком щитовидной железы, у которых нет признаки рака щитовидной железы, который распространился на другие части тела.
Ограничения использования:
- В исследовании людей, готовящихся к лечению той или иной формой йода после операции на щитовидной железе, результаты были схожими между теми, кто получал тироген, и теми, кто прекратил прием гормонов щитовидной железы в течение 5 лет после лечения. Исследователи не знают, будут ли результаты подобными в течение более длительного периода времени.

Щелкните, чтобы увидеть полную информацию о назначении.
(PDF) Значения тиреотропного гормона во время беременности: споры об отсечении продолжаются?
Журнал акушерства и гинекологии Индии (сентябрь – октябрь 2019 г.) 69 (5): 389–394 Значения тиреотропного гормона при беременности…
393
1 3
Negro etal.[15] сравнили 14 материнских и неонатальных
неблагоприятных исходов у 245 женщин с положительной реакцией на тироидную пероксидазу, эути-
женщин с нормальным туберкулезом (ТТГ <2,5 мМЕ / л) в первом триместре с 3348
женщинами, которые были отрицательными на эутиреоид и тироидную пероксидазу
в первом триместре [15]. Они сравнили такие параметры, как
, такие как артериальная гипертензия, преэклампсия, гестационный диабет, кесарево сечение
, преждевременные роды, респираторный дистресс, прием в ОИТН
, низкий вес при рождении, преждевременные роды, низкие баллы по шкале Апгар,
неонатальная смерть и другие. осложнения.Они обнаружили, что все
осложнения.Они обнаружили, что все
14 параметров оказали значительное неблагоприятное влияние на
TPO-положительных женщин.
В одном индийском исследовании [16] сообщается, что у эутиреоидных женщин с положительным результатом на ТПО антитела
в 4–5 раз выше частота выкидышей
и маловесной массы тела независимо от гестационного возраста
по сравнению с женщинами с отрицательным ТПО. Однако,
они не обнаружили никакой корреляции с другим осложнением
, как это было обнаружено в исследовании Negro et al.[15].
Общие данные не являются убедительными ни для рекомендации
рутинного скрининга на аутоантитела щитовидной железы, ни для рекомендации
для лечения эмпирической терапии LT4 [17].
Заключение
Обзор различных отчетов показывает, что более строгие критерии
2,5 cuto ff могут считаться слишком низкими. Многим женщинам
будет без необходимости поставлен диагноз SCH, и
могут подвергнуться терапевтическому бремени лечения LT4. Мы должны попытаться получить
Мы должны попытаться получить
нормативных данных и референсного диапазона, специфичного для местного населения —
и получить весь диапазон процентильных значений [14, 18],
изучить исход беременности проспективно, а затем рекомендовать
исправить нормальный референсный диапазон. по результату.Всегда выгодно использовать данные, специфичные для этнической принадлежности,
; следовательно, мы должны использовать
индийских эталонных диапазонов. Я уверен, что индийский референсный диапазон
для значений ТТГ, рассчитанный с помощью хорошо спланированного проспективного исследования, будет иметь большое значение для улучшения исхода беременности
и уменьшения диагностических и терапевтических ошибок
заболеваний щитовидной железы во время беременности.
Пока не будут получены окончательные доказательства относительно нормативных данных
для TSH cuto ff споры продолжаются…
Ссылки
1.Аджмани С. Н., Аггарвал Д., Бхатия П. и др. Распространенность явной и
Н., Аггарвал Д., Бхатия П. и др. Распространенность явной и
субклинической дисфункции щитовидной железы среди беременных женщин и ее
влияние на исход для матери и плода. J Obstet Gynecol India.
2014; 64 (2): 105.
2. Фриц М.А., Сперо Л. Репродукция и щитовидная железа, глава №20, Клини-
кал гинекологическая эндокринология и бесплодие. 8-е изд. Wolters Klu-
wer Health Lippincot Williams and Wilkins; 2010. С. 340–2.
3.Стагнаро-Грин А, Абалович М, Александр Е, etal. Рекомендации
Американской тироидной ассоциации по диагностике и лечению заболеваний щитовидной железы во время беременности и в послеродовом периоде.
Щитовидная железа. 2011; 21: 1081–125.
4. Де Гроот Л., Абалович М., Александр Е.К., etal. Лечение дисфункции щитовидной железы
во время беременности и в послеродовом периоде: руководство по клинической практике общества эндо-
. J Clin Endocrinol Metab.
2012; 97: 2543–65.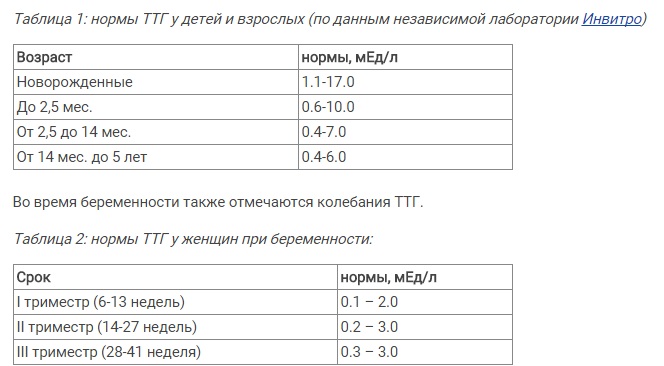
5. Александр Е.К., Пирс Э.Н., Брент Г.А. и др. Рекомендации
Американской тироидной ассоциации по диагностике и лечению
заболеваний щитовидной железы во время беременности и в послеродовом периоде, 2017 г. Щитовидная железа.
2017; 27 (3): 315–89.
6. Ли Й. Дж., Ким Ч., Квак Дж. Й. и др. Субклинический гипотиреоз
, диагностированный с помощью теста на стимуляцию тиреотропин-рилизинг гормона у
бесплодных женщин с базальным уровнем тиреотропного гормона
из 2.От 5 до 5,0 мМЕ / л. Obstet Gynecol Sci. 2014; 57: 507–512.
7. Марака С., Сингх Оспина Н.М., Масторакос Г. и др. Subclini-
гипотиреоз у женщин, планирующих зачатие и во время беременности
: кого и как лечить? J Endocr Soc.
2018; 2 (6): 533–46.
8. Хаммонд К. Р., Катальдо Н. А., Хаббард Дж. А. и др. Гестационный
гипотиреоз: развитие умеренного гипотиреоза на ранних сроках беременности
у ранее эутиреоидных женщин. Fertil Steril.
Fertil Steril.
2015; 103 (6): 1532–6.
9. Марваха Р.К., Чопра С., Гопалакришнан С. и др. Установление
контрольного диапазона гормонов щитовидной железы у здоровых беременных индийских
женщин. BJOG. 2008. 115: 602–6.
10. Калра С., Агарвал С., Аггарвал Р. и др. Специфический для триместра тироид-
стимулирующий гормон: индийская перспектива. Индийский J Endocrinol
Metab. 2018; 22 (1): 1.
11. Каннан С., Махадеван С., Сигамани А.Систематический обзор
нормативных значений тестов функции щитовидной железы для каждого триместра у
индийских женщин. Индийский J Endocr Metab. 2018; 22: 7–12.
12. Maraka S, Singh ON, Mastorakos G, etal. Субклиническая гипотеза —
Роидизм у женщин, планирующих зачатие и во время беременности:
кого и как лечить? J Endocr Soc. 2018; 2 (6): 533.
13. Рех А., Грифо Дж., Дано ff А. Что такое нормальный уровень гормона, стимулирующего щитовидную железу (ТТГ), —
? Влияние более строгих пороговых значений ТТГ
на исход беременности после искусственного оплодотворения.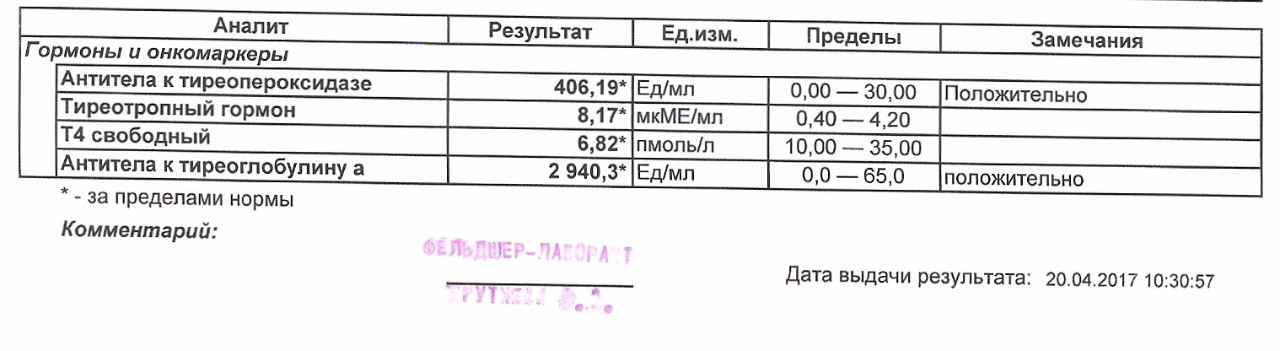 Fertil Steril.
Fertil Steril.
2010; 94 (7): 2920–2.
14. Lara MC, Sánchez ÁV, Solano CC, Pazos ES, Álvarez MI, Macías
CG, Ortega CA, Corral LJ, Alba JJ. Скрининг гипотиреоза
в первом триместре беременности. BMC Беременность и роды.
2017; 17 (1): 438.
15. Негр Р., Шварц А., Жисмонди Р. и др. Положительный результат на тироидные антитела
в первом триместре беременности
связан с отрицательными исходами беременности.J Clin Endocrinol Metab.
2011; 96 (6): E920–24.
16. Мина А., Нагар П. Исход беременности у эутиреоидных женщин
с антителами к тироидной пероксидазе. J Obstet Gynecol India.
2016; 66 (3): 160–5.
17. Мехран Л., Тохиди М., Сарвгхади Ф. и др. Лечение щитовидной железы
эутиреоидных женщин с антителами к пероксидазе во время беременности: сравнение
Американской тироидной ассоциации и
Эндокринного общества.J Thyroid Res. 2013; 2013, номер статьи 542692. https
: //doi. org/10.1155/2013/54269 2.
org/10.1155/2013/54269 2.
18. Медичи М., Кореваар Т.И., Виссер В.Е., etal. Функция щитовидной железы при беременности
: что нормально? Clin Chem. 2015; 61 (5): 704–13.
Примечание издателя Springer Nature сохраняет нейтралитет в отношении
судебных исков на опубликованных картах и институциональных ассоциациях.
Тест на ТТГ (тиреотропный гормон)
Что такое тест на ТТГ (тиреотропный гормон)?
Определение:
ТТГ — это тест, который измеряет количество гормона ТТГ в крови.
Альтернативные названия: Тиротропин; Стимулирующий гормон щитовидной железы
Порядок проведения теста:
Взрослый или ребенок:
Кровь берется из вены, обычно с внутренней стороны локтя или тыльной стороны руки. Место прокола очищается антисептиком, и на плечо накладывается жгут, чтобы оказать давление и ограничить кровоток по вене. В результате вены под жгутом наполняются кровью.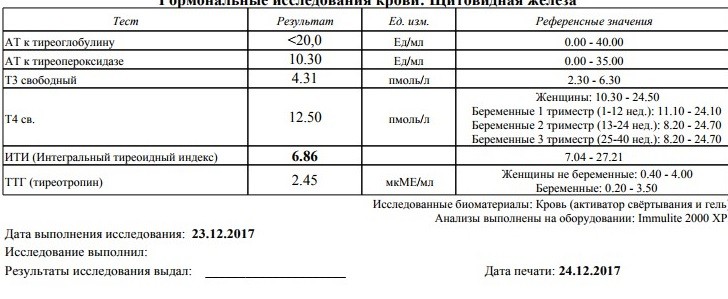 В вену вводится игла, и кровь собирается в герметичный флакон или шприц.Затем жгут снимают для восстановления кровообращения. После взятия крови иглу удаляют, а место прокола закрывают, чтобы остановить кровотечение.
В вену вводится игла, и кровь собирается в герметичный флакон или шприц.Затем жгут снимают для восстановления кровообращения. После взятия крови иглу удаляют, а место прокола закрывают, чтобы остановить кровотечение.
Младенцы или маленькие дети:
Область очищается антисептиком и прокалывается острой иглой или ланцетом. Кровь можно собрать в пипетку (небольшую стеклянную пробирку), на предметное стекло, на тест-полоску или в небольшой контейнер. При кровотечении можно наложить повязку на место прокола.
Как подготовиться к экзамену:
Обычно никакой специальной подготовки не требуется.
Как будет выглядеть тест:
Когда игла вводится для забора крови, некоторые люди чувствуют умеренную боль, в то время как другие ощущают только покалывание или покалывание. После этого может появиться некоторая пульсация.
Зачем проводится тест:
ТТГ измеряется как скрининговый тест на аномальную функцию щитовидной железы (гипертиродизм или гипотиреодизм).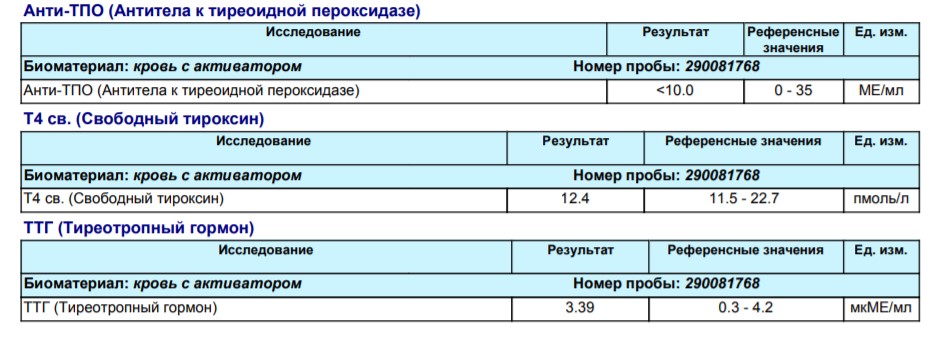 Также измеряется, чтобы контролировать лечение этих состояний. Тест также проводится у бесплодных женщин, чтобы проверить, не является ли заболевание щитовидной железы причиной бесплодия.
Также измеряется, чтобы контролировать лечение этих состояний. Тест также проводится у бесплодных женщин, чтобы проверить, не является ли заболевание щитовидной железы причиной бесплодия.
TRH, гормон, вырабатываемый в гипоталамусе, стимулирует выработку ТТГ гипофизом. Впоследствии ТТГ стимулирует выработку тироидными гормонами Т3 и Т4. Эти гормоны взаимодействуют с гипоталамусом и гипофизом, регулируя высвобождение как ТТГ, так и ТРГ.
При некоторых заболеваниях этот путь регуляции изменяется, что приводит к недостаточной или избыточной продукции гормона щитовидной железы. При клиническом подозрении на заболевание щитовидной железы в качестве первоначального теста определяют уровень ТТГ.
Нормальные значения:
Нормальные значения составляют от 0,4 до 4,0 мМЕ / л для тех, у кого нет симптомов недостаточной или чрезмерной активности щитовидной железы. Если вы лечитесь от заболевания щитовидной железы, ваш ТТГ должен составлять от 0,5 до 2,0 мМЕ / л.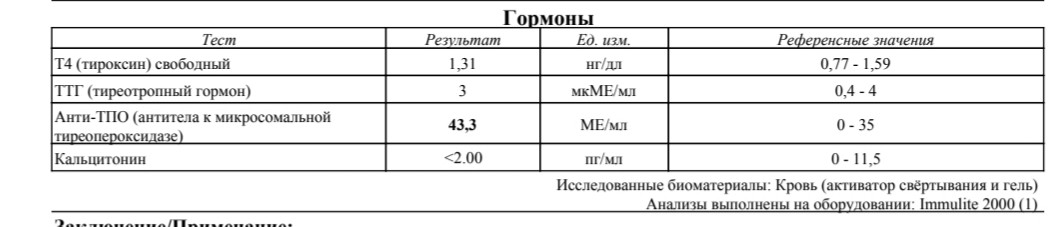 Это означает, что с вами обращаются должным образом.
Это означает, что с вами обращаются должным образом.
У некоторых людей с уровнем ТТГ более 2,0 мМЕ / л, у которых нет признаков или симптомов, указывающих на недостаточную активность щитовидной железы, в будущем может развиться гипотиреоз. Всем, у кого ТТГ выше 2.Следовательно, при 0 мМЕ / л врач должен очень внимательно следить за этим.
Нормальные диапазоны значений могут незначительно отличаться в разных лабораториях.
Что означают аномальные результаты:
Уровни выше нормы могут указывать на:
- Врожденный гипотиреоз (кретинизм)
- Первичный гипотиреоз
- ТТГ-зависимый гипертиреоз
- ТТГ-зависимый гипертиреоз
- Устойчивость к тиреоидному гормону
- работники или ветеринары)
Уровни ниже нормы могут указывать на:
- Гипертиреоз
- Дефицит ТТГ
- Лекарства (агноисты дофамина, глюкокортикоиды, аналоги соматостатина, бексаротин)
000 000 000 Особые рекомендации:
Лекарства которые могут повлиять на измерения ТТГ включают: антитиреоидные препараты, литий, йодид калия, амиодарон, дофамин и преднизон.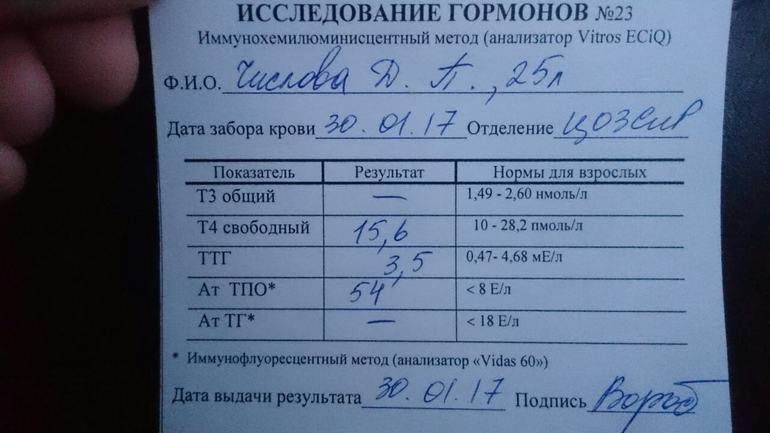

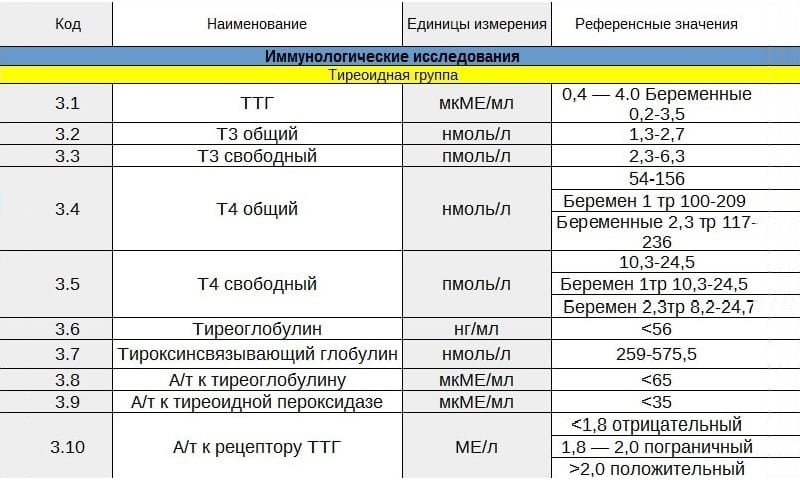
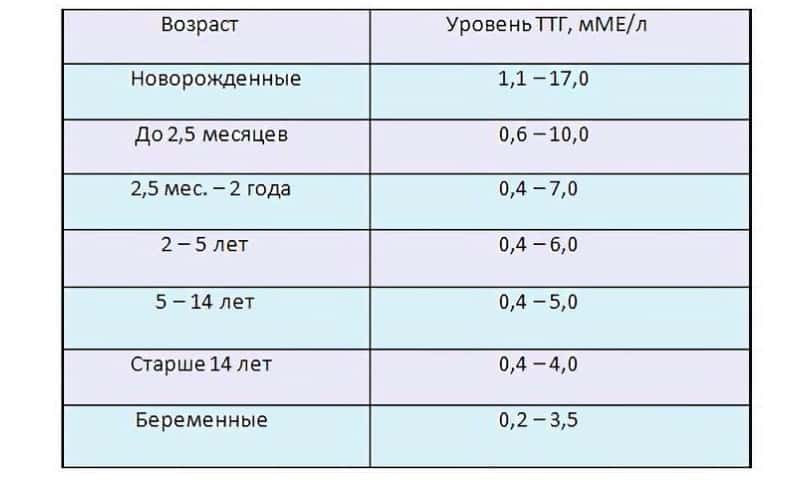 Уровень ТТГ при гипотиреозе является одним из главных показателей развития заболевания, так как чаще всего на этой стадии болезнь себя не выказывает.
Уровень ТТГ при гипотиреозе является одним из главных показателей развития заболевания, так как чаще всего на этой стадии болезнь себя не выказывает.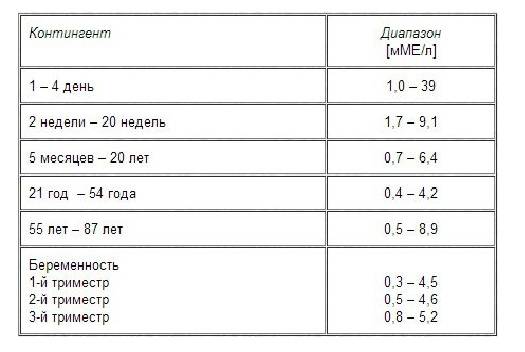



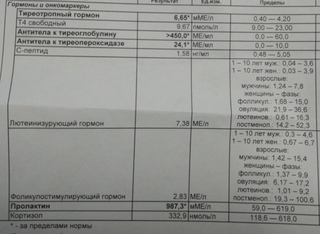
 Обычно пациенты с гипотиреозом говорят так: «Сразу после пробуждения мне хочется снова лечь спать».
Обычно пациенты с гипотиреозом говорят так: «Сразу после пробуждения мне хочется снова лечь спать».
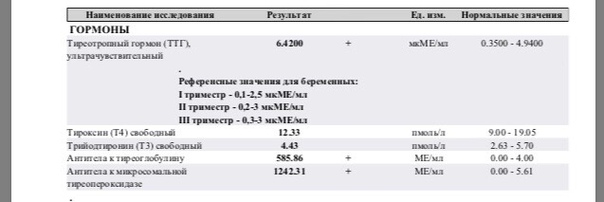
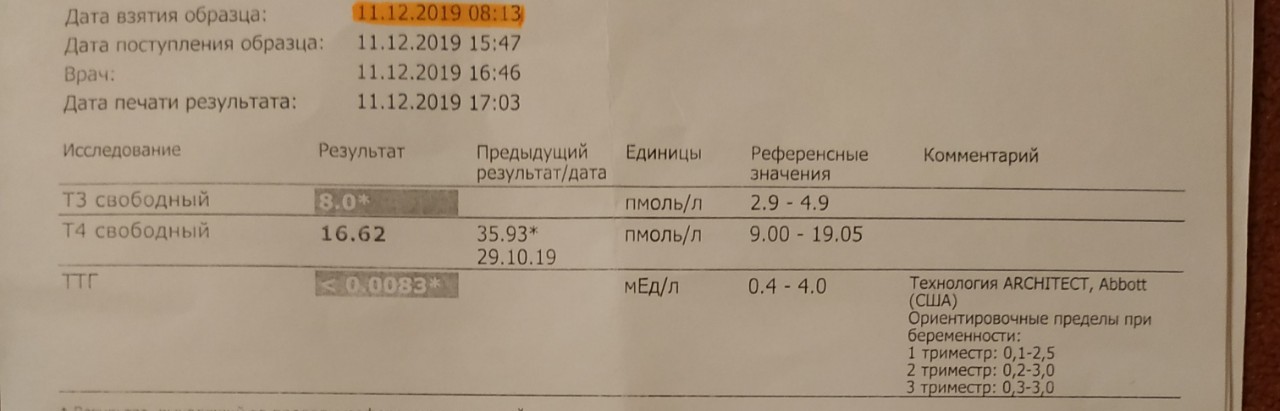 06 ± 0,41
06 ± 0,41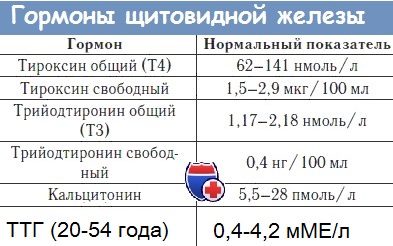 00 -1,52
00 -1,52 491
491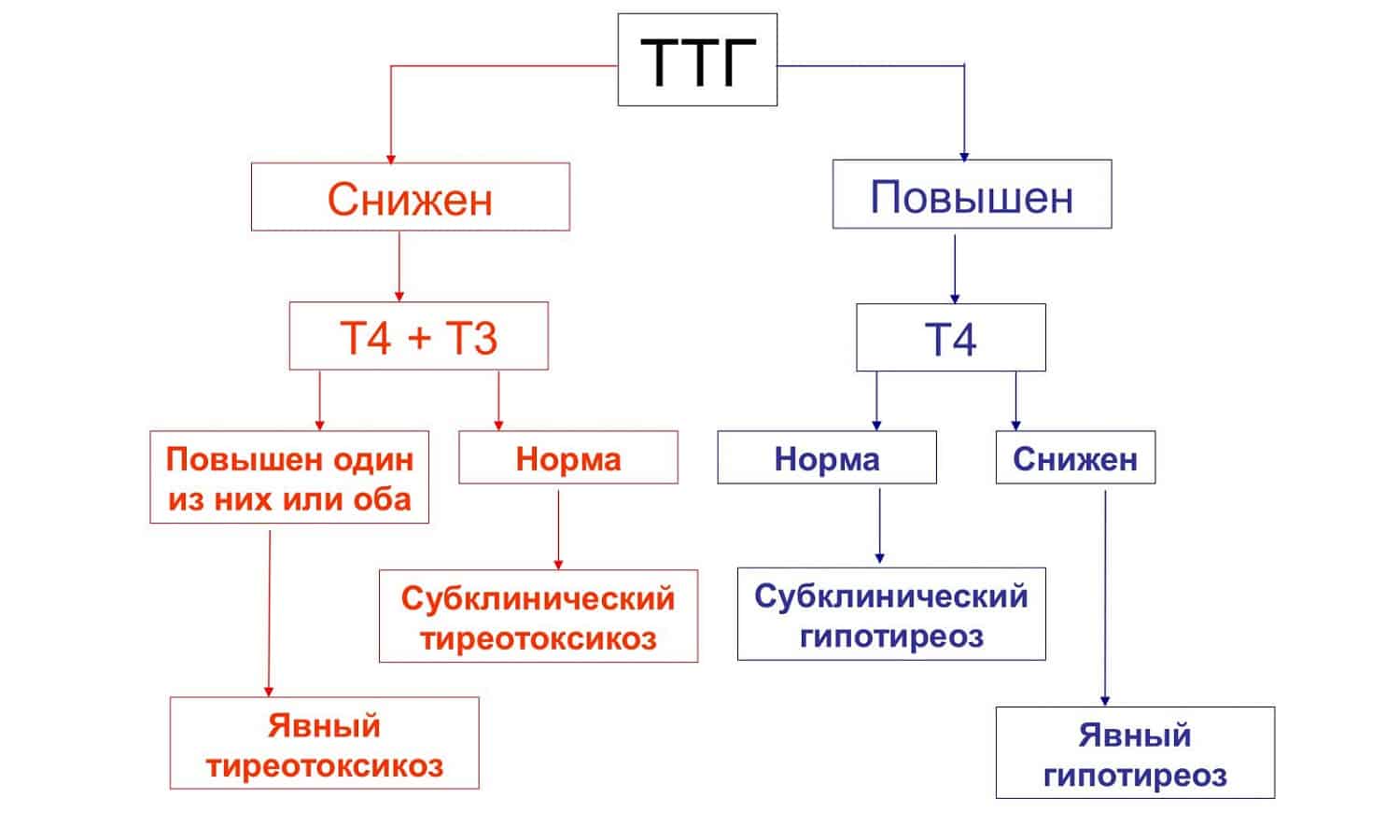 876
876 156
156 395
395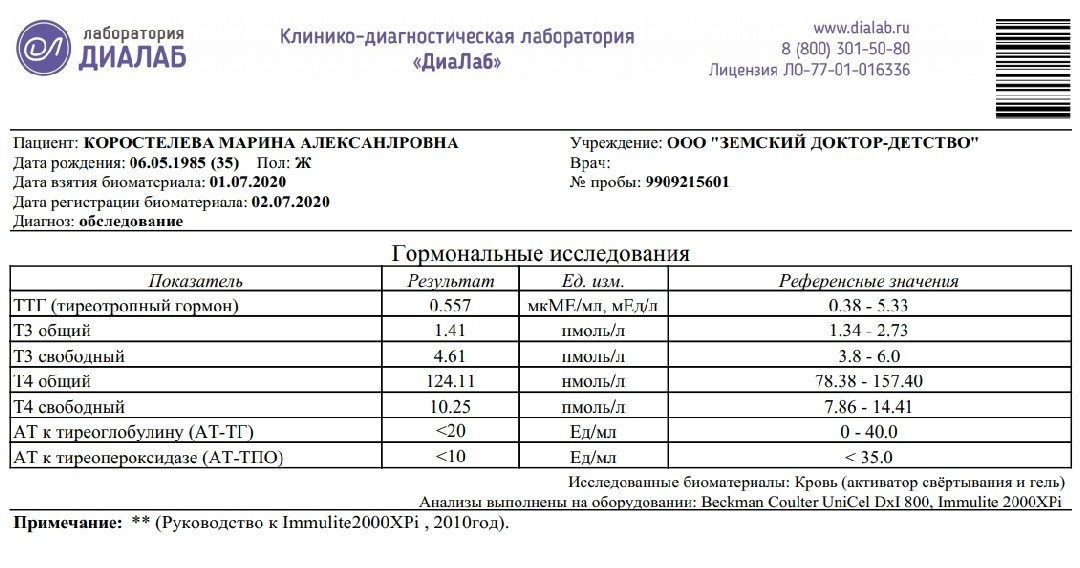 329
329 00
00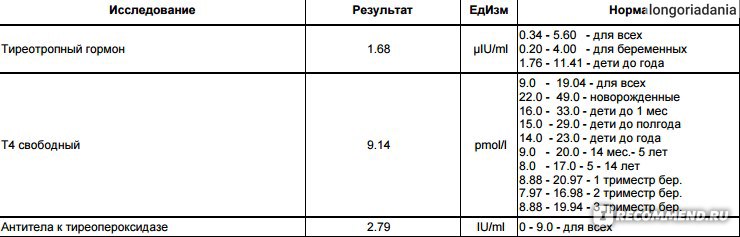 31 *
31 * 74
74 Aust N Z J Public Health 32: 421-423.[Crossref]
Aust N Z J Public Health 32: 421-423.[Crossref] и др. (2003) Характеристика селенопротеомов млекопитающих. Наука 300: 1439-1443. [Crossref]
и др. (2003) Характеристика селенопротеомов млекопитающих. Наука 300: 1439-1443. [Crossref]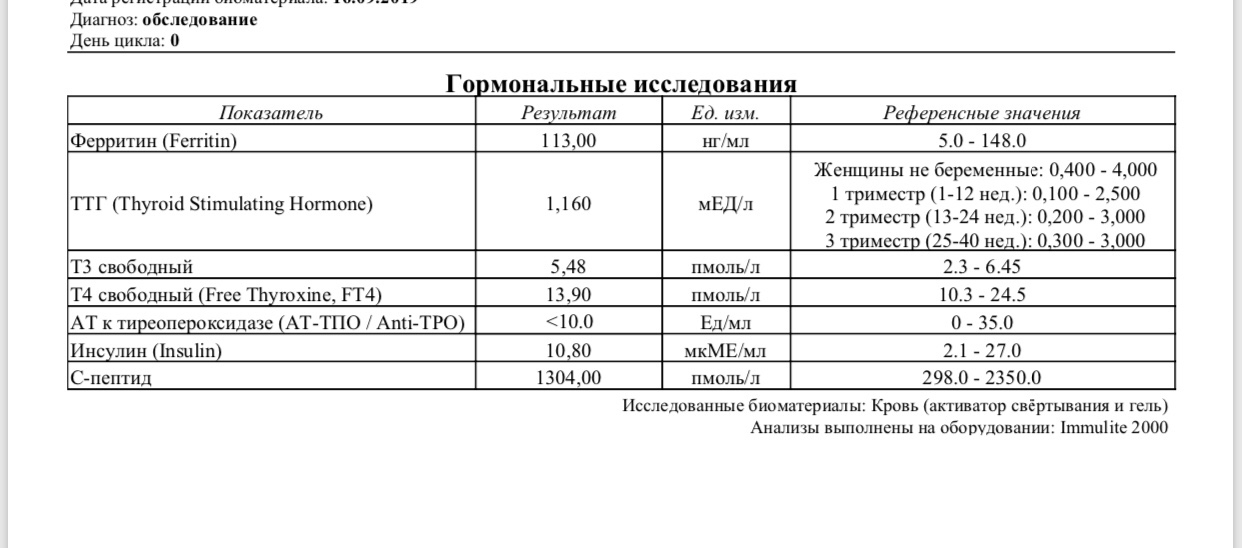 Дж. Эндокринол 184: 455-465. [Crossref]
Дж. Эндокринол 184: 455-465. [Crossref]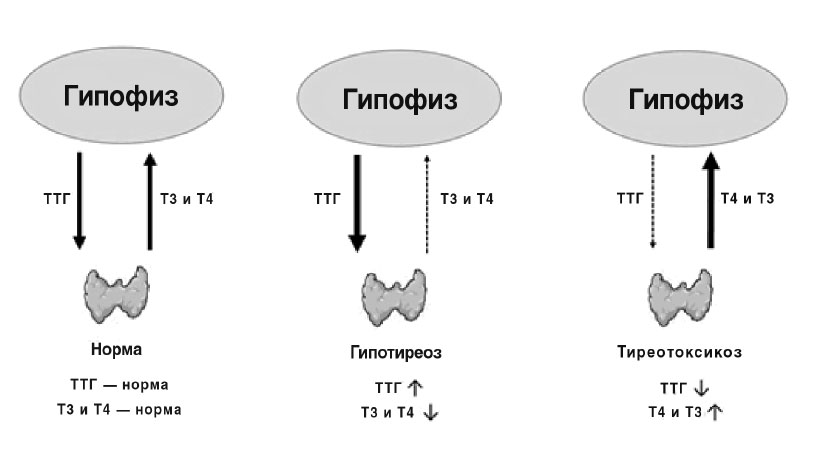 Эндокринология 103: 1196-1207.[Crossref]
Эндокринология 103: 1196-1207.[Crossref] Environ Health Persp 115: 77. [Crossref]
Environ Health Persp 115: 77. [Crossref]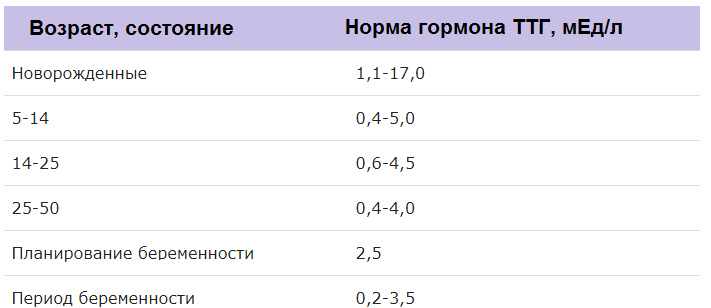 Питательные вещества 7: 2209-2236. [Crossref]
Питательные вещества 7: 2209-2236. [Crossref]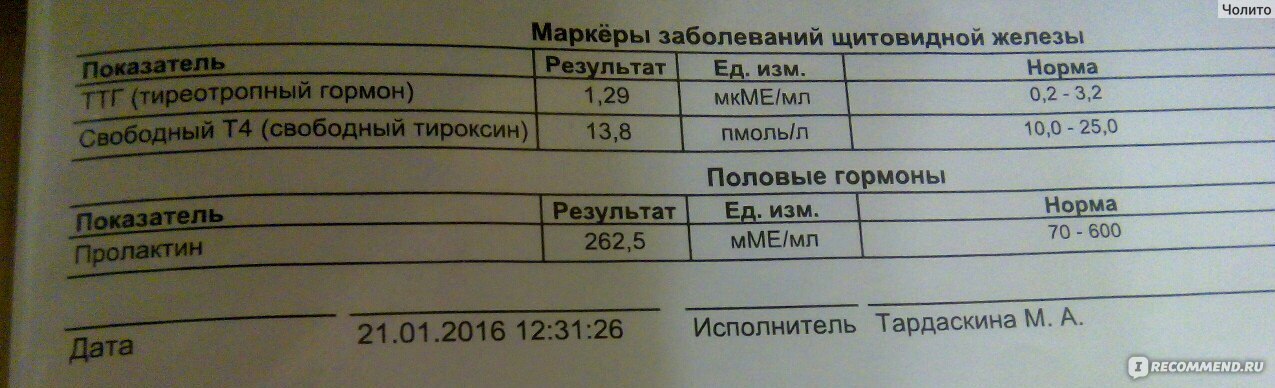 Arch Intern Med 160: 526-534. [Crossref]
Arch Intern Med 160: 526-534. [Crossref] Drug Des Devel Ther 6: 1-11. [Crossref]
Drug Des Devel Ther 6: 1-11. [Crossref] [Crossref]
[Crossref] British J Nutrition 94: 962-968.
British J Nutrition 94: 962-968.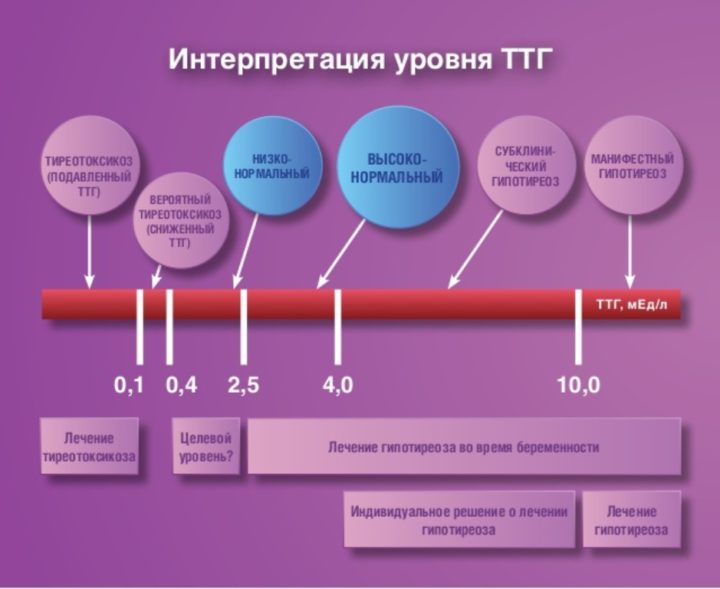 Eur Thyroid J 243-250. [Crossref]
Eur Thyroid J 243-250. [Crossref] (2002) Добавление селена пациентам с аутоиммунным тиреоидитом снижает концентрацию антител к тироидной пероксидазе. J Clin Endocr Metab 87: 1687-1691. [Crossref]
(2002) Добавление селена пациентам с аутоиммунным тиреоидитом снижает концентрацию антител к тироидной пероксидазе. J Clin Endocr Metab 87: 1687-1691. [Crossref]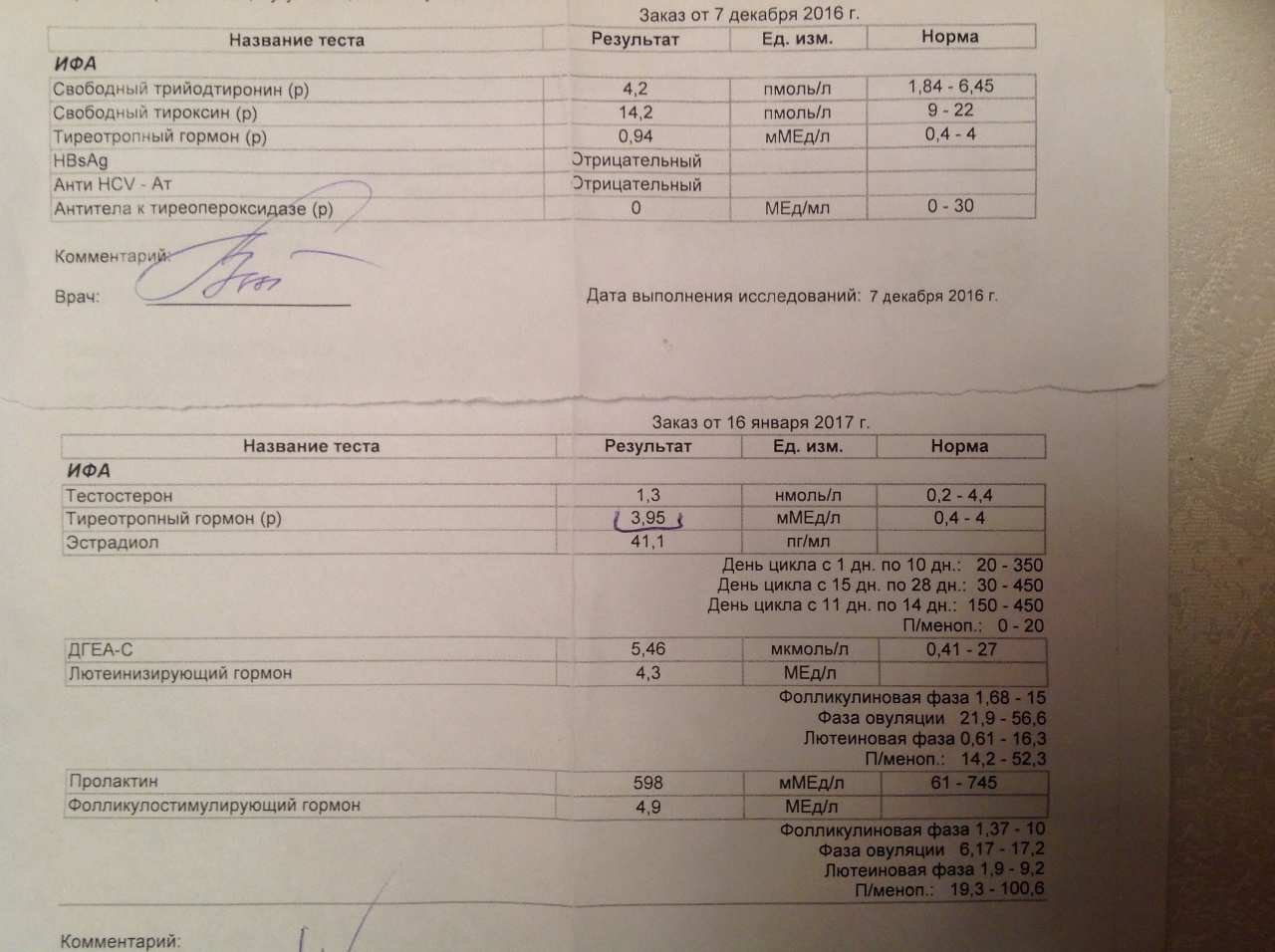
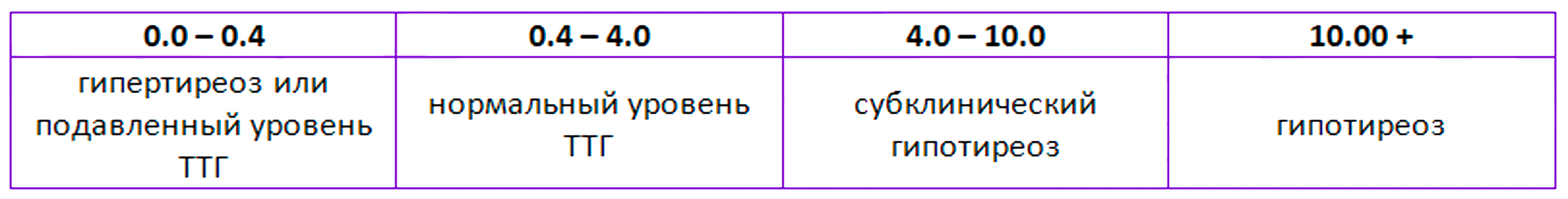 )
)








 Одним из показателей состояния здоровья человека при проведении биохимического анализа крови и мочи является креатинин.
Одним из показателей состояния здоровья человека при проведении биохимического анализа крови и мочи является креатинин.  Повышение нормы креатинина свидетельствует от ряде серьезных заболеваний.
Повышение нормы креатинина свидетельствует от ряде серьезных заболеваний. Народные средства могут помочь для налаживания работы почек и тем самым способствовать выведению креатинина из организма. Но дадут они кратковременный эффект и полностью полагаться на средства народной медицины не стоим.
Народные средства могут помочь для налаживания работы почек и тем самым способствовать выведению креатинина из организма. Но дадут они кратковременный эффект и полностью полагаться на средства народной медицины не стоим.











 Нужно использовать кончики указательного и среднего пальцев, чтобы нащупать пульс.
Нужно использовать кончики указательного и среднего пальцев, чтобы нащупать пульс. Например, считается, что частота сердечных сокращений в состоянии покоя у спортсменов колеблется в пределах 50 или менее. Это достигается их строгой физической подготовкой и режимом упражнений.
Например, считается, что частота сердечных сокращений в состоянии покоя у спортсменов колеблется в пределах 50 или менее. Это достигается их строгой физической подготовкой и режимом упражнений. Факторы образа жизни, способствующие тахикардии, включают курение, недостаточную физическую нагрузку, недостаточный сон, слишком много кофе или алкоголя.
Факторы образа жизни, способствующие тахикардии, включают курение, недостаточную физическую нагрузку, недостаточный сон, слишком много кофе или алкоголя. Это особенно верно, если присутствуют дополнительные симптомы.
Это особенно верно, если присутствуют дополнительные симптомы.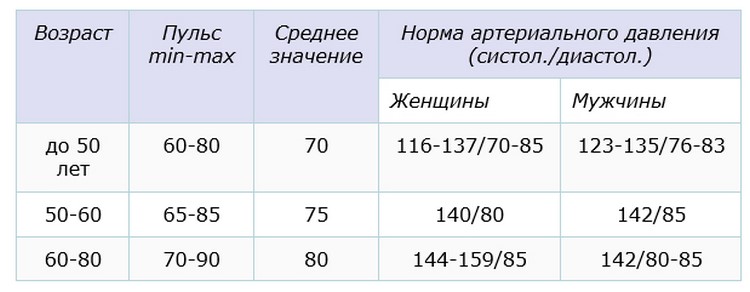 Мы чувствуем пульс как удар в больших артериях. Лучшим временем для измерения пульса является утро.
Мы чувствуем пульс как удар в больших артериях. Лучшим временем для измерения пульса является утро. Чтобы пульс поднялся на 10-12 ударов, нужно поменять положение своего тела. Например, вы долго лежали и резко встали. При минимальных изменениях пульс быстро стабилизируется. Для различных возрастов есть своя норма:
Чтобы пульс поднялся на 10-12 ударов, нужно поменять положение своего тела. Например, вы долго лежали и резко встали. При минимальных изменениях пульс быстро стабилизируется. Для различных возрастов есть своя норма:
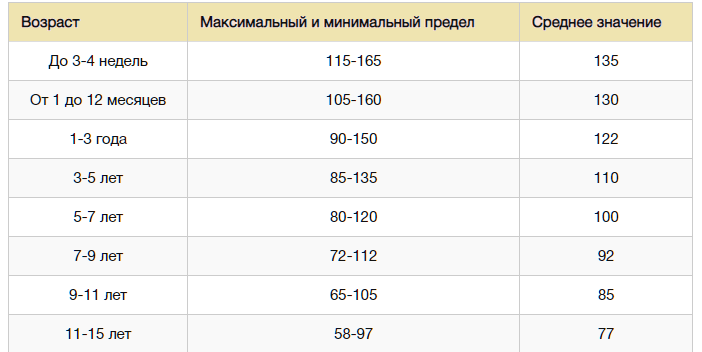 Если вам 60, то максимальный пульс должен быть 160.
Если вам 60, то максимальный пульс должен быть 160.
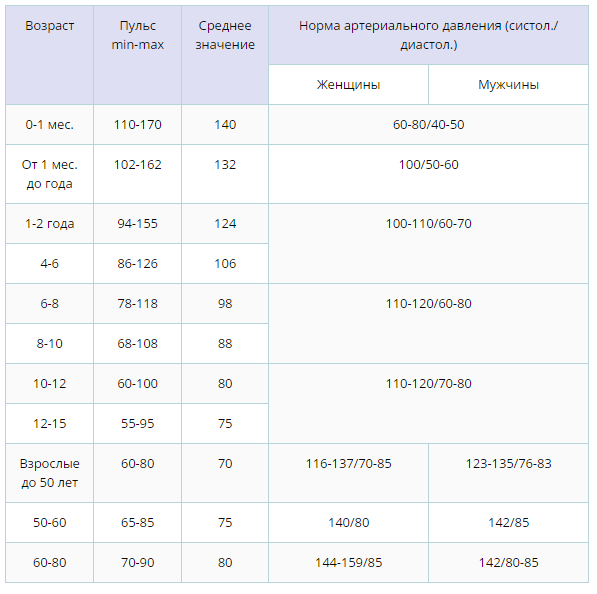
 Для повышения пульса пожилые люди могут пить напитки, в которых содержится кофеин: черный и зеленый чай, натуральный кофе. Кофеин увеличивает сердцебиение. Тем, у кого иногда падает пульс, можно взять за привычку выпивать по утрам горячий крепкий кофе или чай, который зарядит на большую часть дня;
Для повышения пульса пожилые люди могут пить напитки, в которых содержится кофеин: черный и зеленый чай, натуральный кофе. Кофеин увеличивает сердцебиение. Тем, у кого иногда падает пульс, можно взять за привычку выпивать по утрам горячий крепкий кофе или чай, который зарядит на большую часть дня;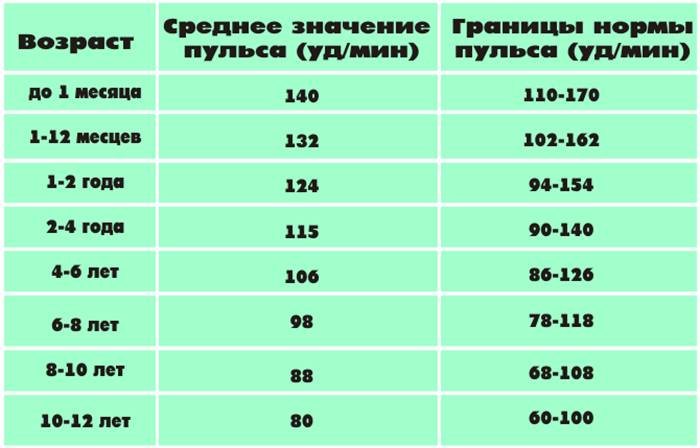 Можно использовать эфирные масла;
Можно использовать эфирные масла;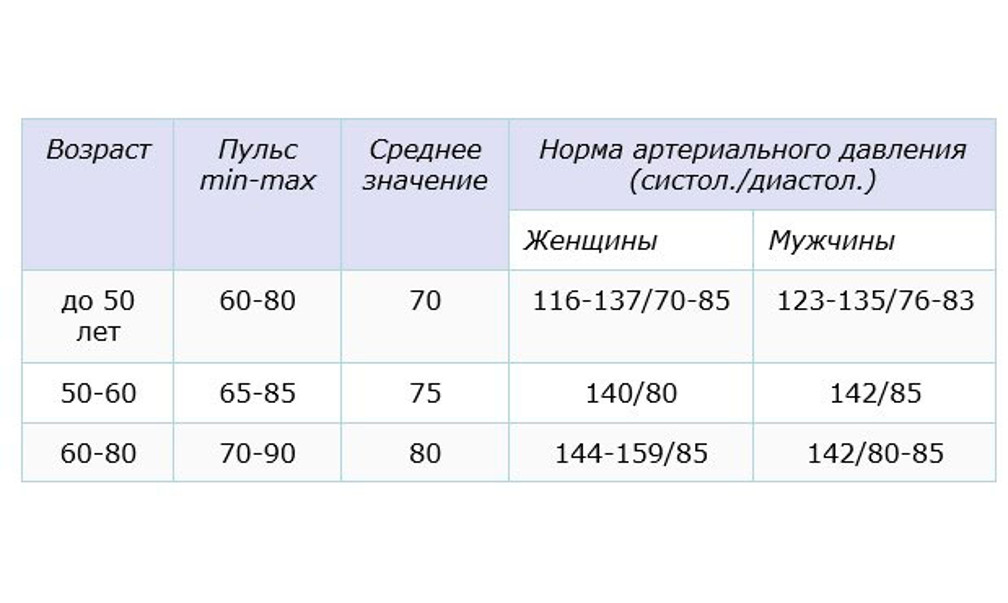
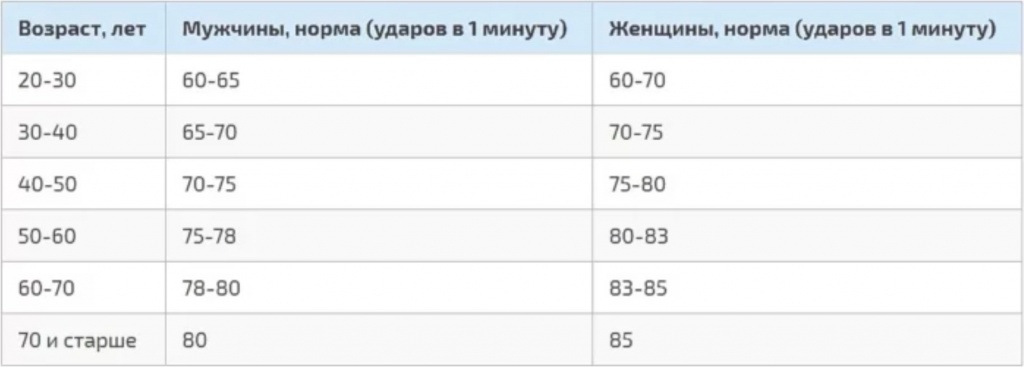 Лучше пить соки, воду, морсы;
Лучше пить соки, воду, морсы; Это действие позволит снизить пульс у пожилого человека. Надавите несильно на глазные яблоки при закрытых глазах. Эту процедуру нужно делать 30 секунд, и пульс стабилизируется;
Это действие позволит снизить пульс у пожилого человека. Надавите несильно на глазные яблоки при закрытых глазах. Эту процедуру нужно делать 30 секунд, и пульс стабилизируется;
 Понять что это такое достаточно просто, пульс – это колебание стенок сосудов. Появляются колебания тогда, когда сокращается сердечная мышца. По пульсу, вернее по его частоте и силе, можно ориентировочно определить ритмичность биения сердца, характер его работы, здоровье и нынешнее состояние крупных сосудов.
Понять что это такое достаточно просто, пульс – это колебание стенок сосудов. Появляются колебания тогда, когда сокращается сердечная мышца. По пульсу, вернее по его частоте и силе, можно ориентировочно определить ритмичность биения сердца, характер его работы, здоровье и нынешнее состояние крупных сосудов.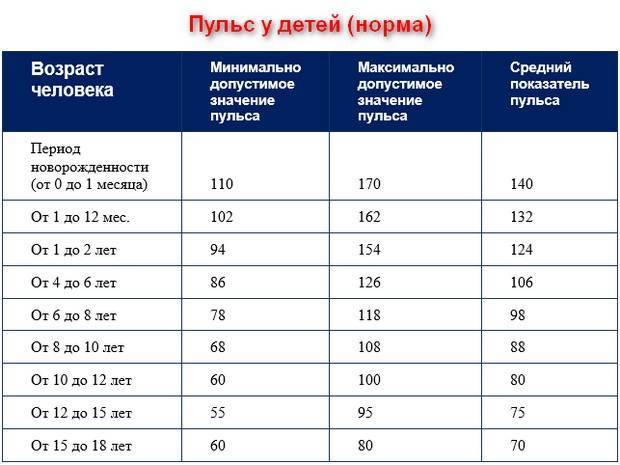 Если за первые 30 секунд ритмичность установить не удается, то пульс следует мерить в течение минуты. Если на запястье не удается измерить пульс, его так же можно нащупать в висках.
Если за первые 30 секунд ритмичность установить не удается, то пульс следует мерить в течение минуты. Если на запястье не удается измерить пульс, его так же можно нащупать в висках.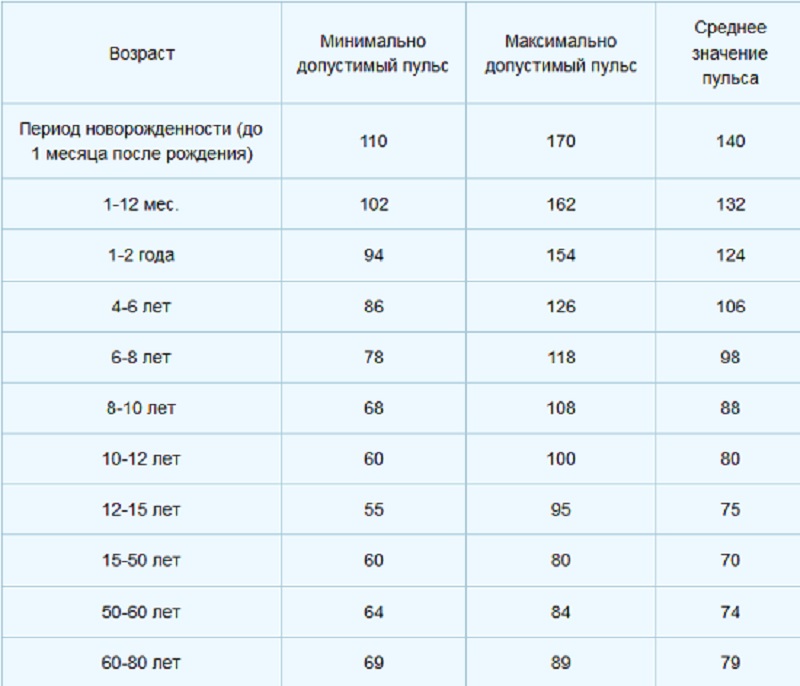 Так же обязательно следует учитывать физическое состояние здоровья мужчины (ребенка, мальчика, парня) и его физическую подготовку, время приема пищи (как давно он кушал) и чем занимался перед измерением пульса (спал, ходил, бегал).
Так же обязательно следует учитывать физическое состояние здоровья мужчины (ребенка, мальчика, парня) и его физическую подготовку, время приема пищи (как давно он кушал) и чем занимался перед измерением пульса (спал, ходил, бегал).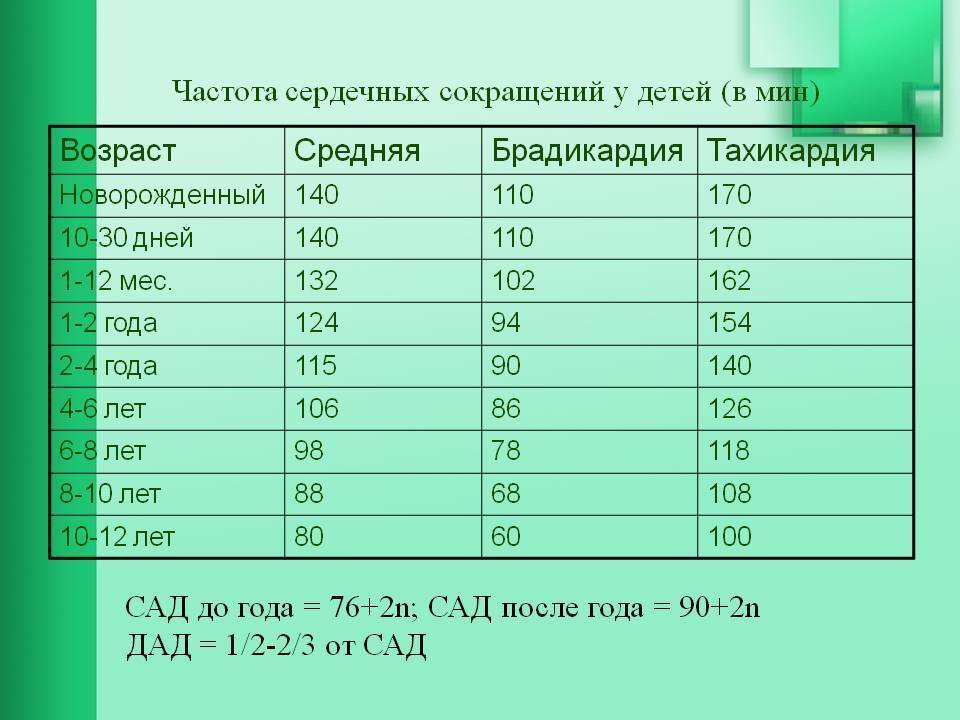 Мерить пульс ребенка следует намного чаще, чем взрослому, чтобы определить его состояние здоровья. После 1 месяца жизни пульс у ребенка снижается и только когда ему исполняется 12-13 лет, нормы становятся похожими на нормы взрослого человека.
Мерить пульс ребенка следует намного чаще, чем взрослому, чтобы определить его состояние здоровья. После 1 месяца жизни пульс у ребенка снижается и только когда ему исполняется 12-13 лет, нормы становятся похожими на нормы взрослого человека.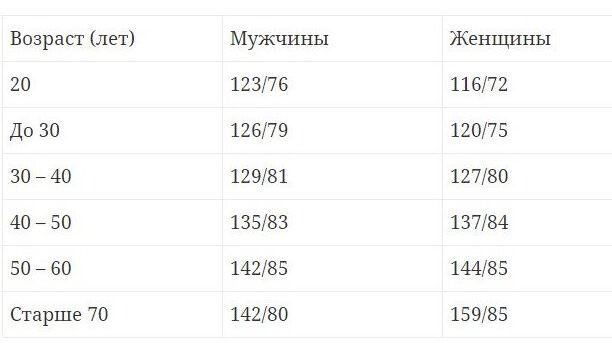

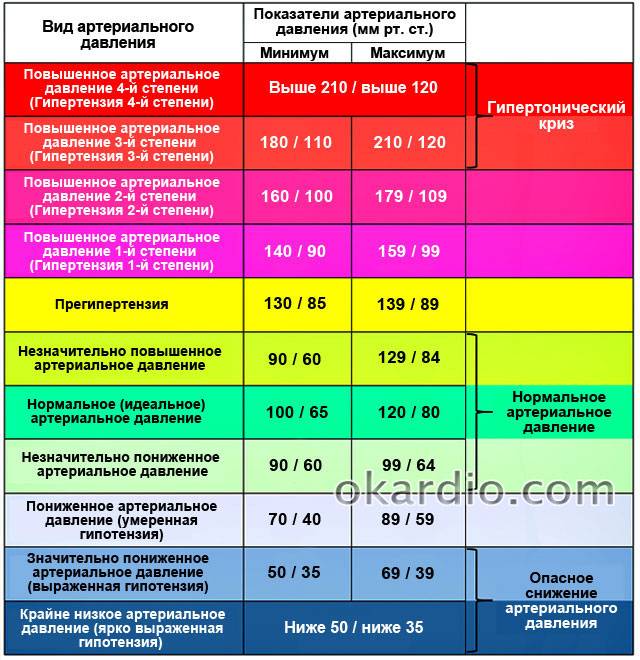 Например, если вам 30 лет, то формула будет выглядеть следующим образом: 220 – 30 = 190 (максимальный пульс), далее 190 * 0,6 = 114 — это нижняя граница первой зоны интенсивности, 190 * 0,7 = 133 — это верхняя граница первой пульсовой зоны. Таким образом можно рассчитать пульсовые значения для любой зоны интенсивности.
Например, если вам 30 лет, то формула будет выглядеть следующим образом: 220 – 30 = 190 (максимальный пульс), далее 190 * 0,6 = 114 — это нижняя граница первой зоны интенсивности, 190 * 0,7 = 133 — это верхняя граница первой пульсовой зоны. Таким образом можно рассчитать пульсовые значения для любой зоны интенсивности.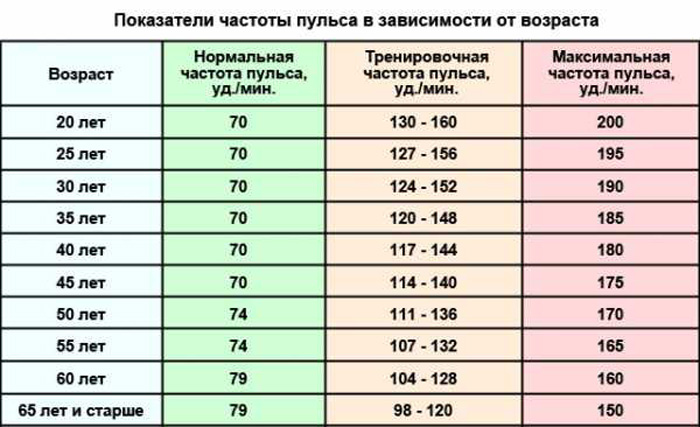 Эта система требует накопления «мусора», который необходимо выводить из работающих мышц.
Эта система требует накопления «мусора», который необходимо выводить из работающих мышц.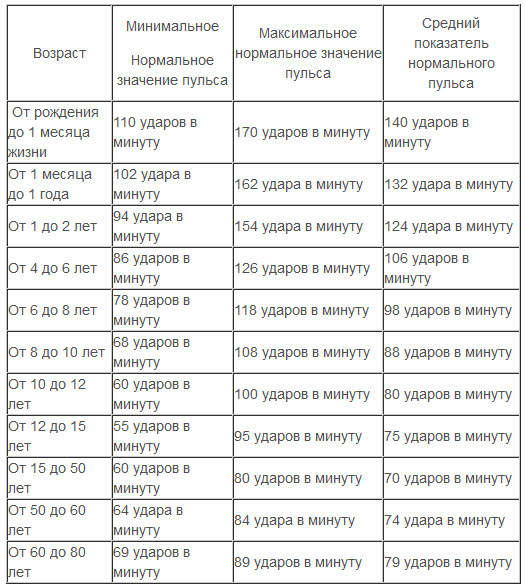
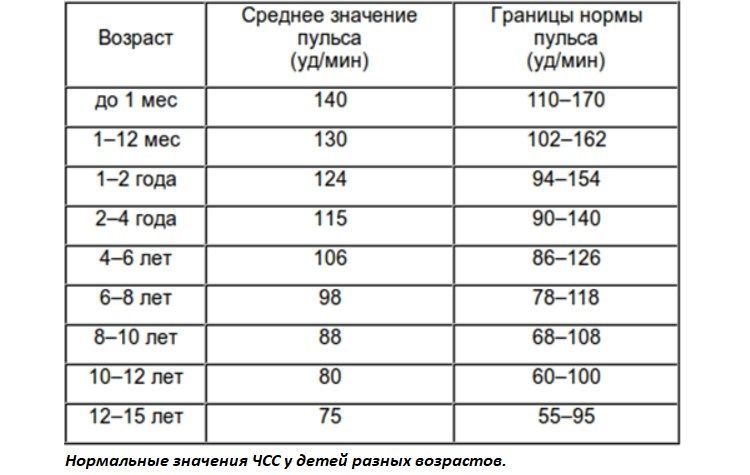
 «С каждой тренировкой вам будет всё сложнее доходить до верхней границы, и это будет означать, что вы становитесь выносливее. То есть даже при самой интенсивной нагрузке ваш пульс будет спокойнее, чем у человека с меньшей выносливостью при той же нагрузке», — объясняет тренер студии персональных тренировок Elastic.
«С каждой тренировкой вам будет всё сложнее доходить до верхней границы, и это будет означать, что вы становитесь выносливее. То есть даже при самой интенсивной нагрузке ваш пульс будет спокойнее, чем у человека с меньшей выносливостью при той же нагрузке», — объясняет тренер студии персональных тренировок Elastic.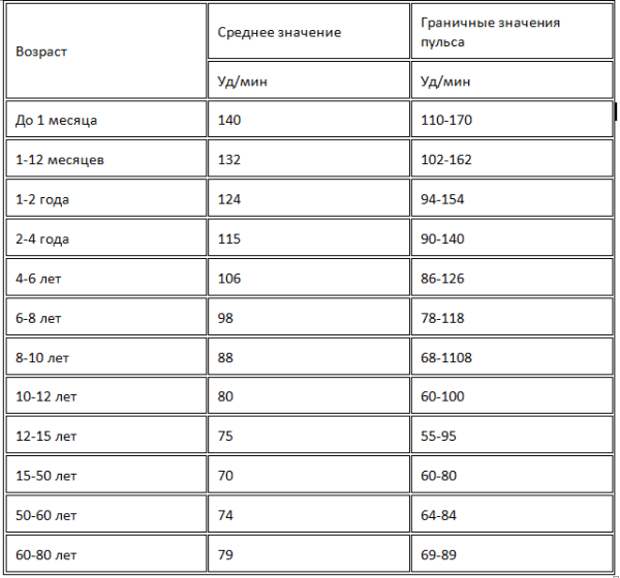

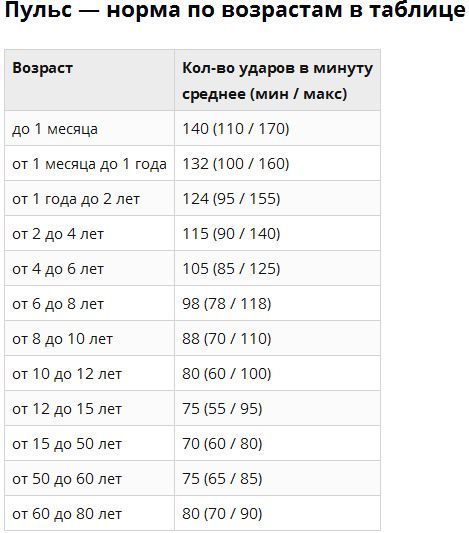
 Частота всего 40 ударов в минуту может быть нормальной и просто быть результатом снижения реакции на адреналин или бета-адренергическую стимуляцию. Или такие низкие темпы могут быть следствием опасной аритмии. Ключ к быстрому определению того, является ли медленное сердцебиение пожилого пациента безвредным или опасным, — это прослушивание первого тона сердца (S1).
Частота всего 40 ударов в минуту может быть нормальной и просто быть результатом снижения реакции на адреналин или бета-адренергическую стимуляцию. Или такие низкие темпы могут быть следствием опасной аритмии. Ключ к быстрому определению того, является ли медленное сердцебиение пожилого пациента безвредным или опасным, — это прослушивание первого тона сердца (S1). Эти позиции до закрытия зависят от длины интервала PR перед комплексом QRS. При коротком интервале PR широко открытые клапаны внезапно закрываются, вызывая громкий S1. При длительном интервале PR открытым клапанам требуется больше времени, чтобы оставаться закрытыми, что приводит к мягкому S1. Таким образом, чем короче интервал PR, тем громче S1; и чем длиннее интервал PR, тем мягче S1.
Эти позиции до закрытия зависят от длины интервала PR перед комплексом QRS. При коротком интервале PR широко открытые клапаны внезапно закрываются, вызывая громкий S1. При длительном интервале PR открытым клапанам требуется больше времени, чтобы оставаться закрытыми, что приводит к мягкому S1. Таким образом, чем короче интервал PR, тем громче S1; и чем длиннее интервал PR, тем мягче S1.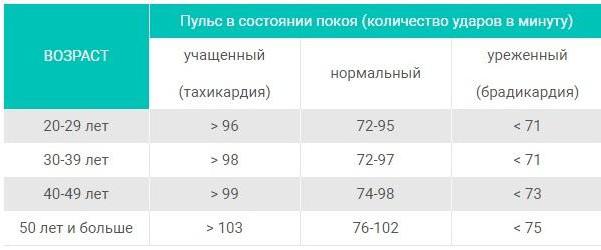 Прежде чем пациент получит эффективную стимуляцию, 0.5 мг атропина в / в. может быть прописан. Эта доза может быть повторена до общей дозы 3 мг. Или от 2 до 10 мкг / мин адреналина внутривенно. или от 2 до 10 мкг / кг / мин дофамина внутривенно. может быть прописан.
Прежде чем пациент получит эффективную стимуляцию, 0.5 мг атропина в / в. может быть прописан. Эта доза может быть повторена до общей дозы 3 мг. Или от 2 до 10 мкг / мин адреналина внутривенно. или от 2 до 10 мкг / кг / мин дофамина внутривенно. может быть прописан.
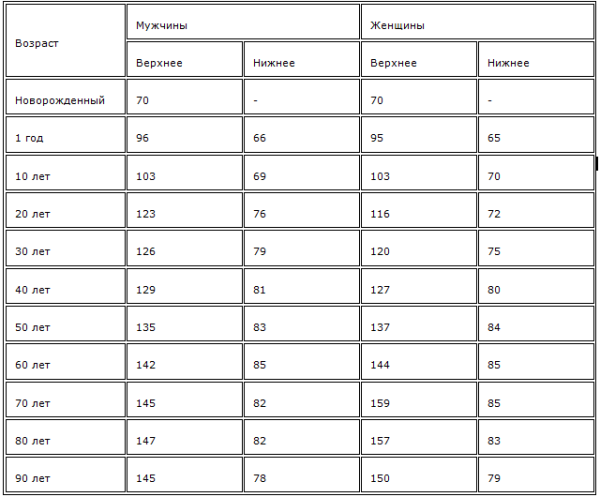 Это помогает снизить риск депрессии и ранней смерти среди пациентов с сердечными заболеваниями, а также помогает улучшить кровяное давление, уровень сахара в крови, кислород в крови и общее качество жизни.
Это помогает снизить риск депрессии и ранней смерти среди пациентов с сердечными заболеваниями, а также помогает улучшить кровяное давление, уровень сахара в крови, кислород в крови и общее качество жизни.

 Самые современные мониторы могут загружать результаты на ваш компьютер или включать системы GPS.
Самые современные мониторы могут загружать результаты на ваш компьютер или включать системы GPS.
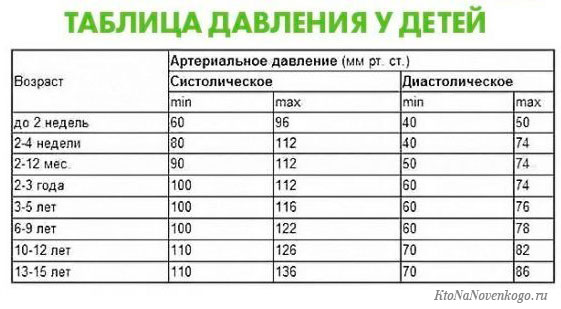 Ann Intern Med. 2017; 166: 430-7.
Ann Intern Med. 2017; 166: 430-7.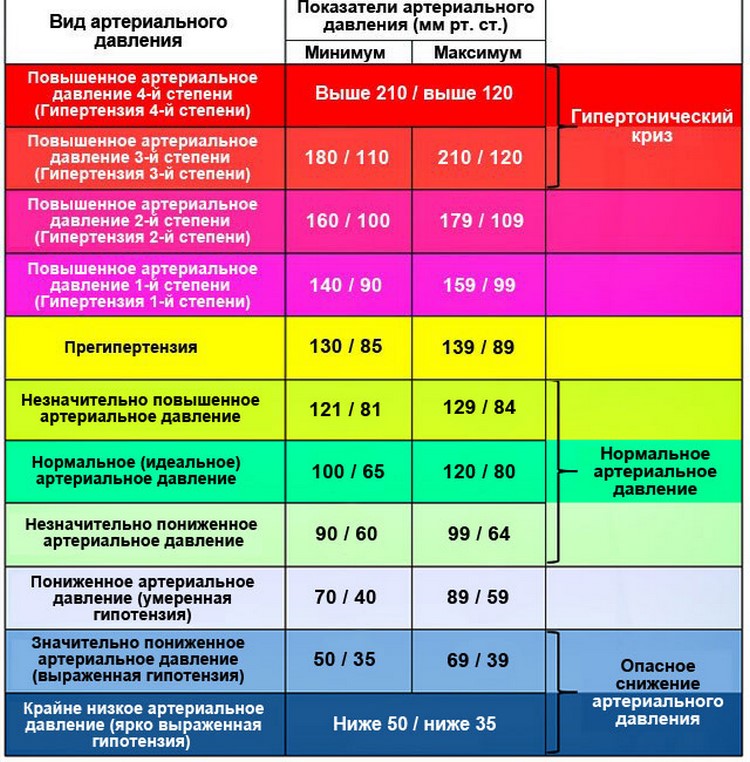
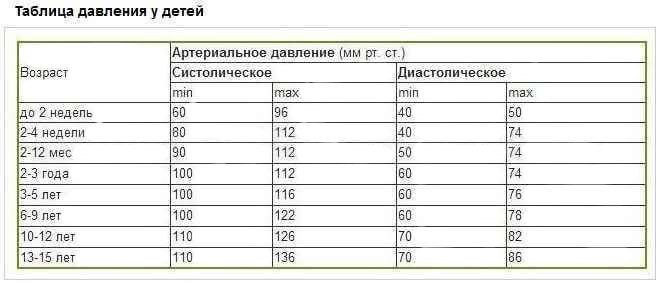
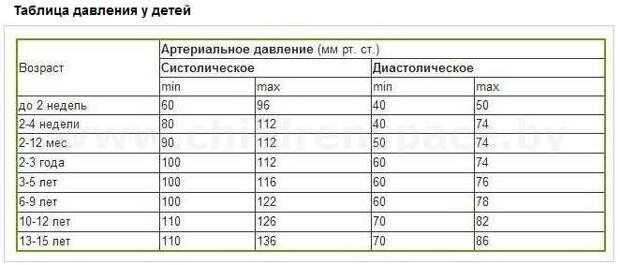 Ст. Или более
Ст. Или более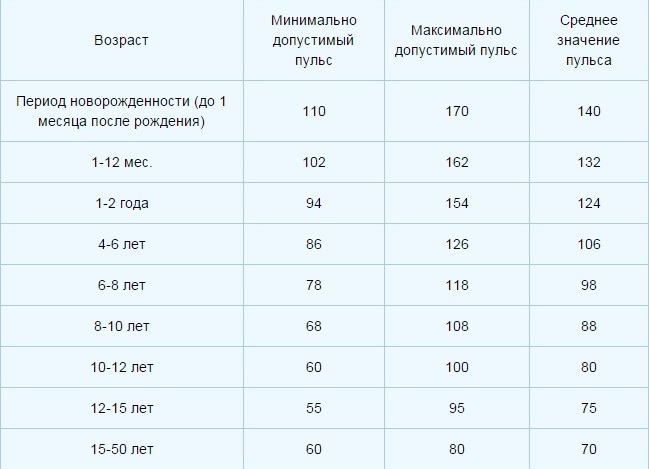 Это давление, когда сердце отдыхает между ударами.
Это давление, когда сердце отдыхает между ударами.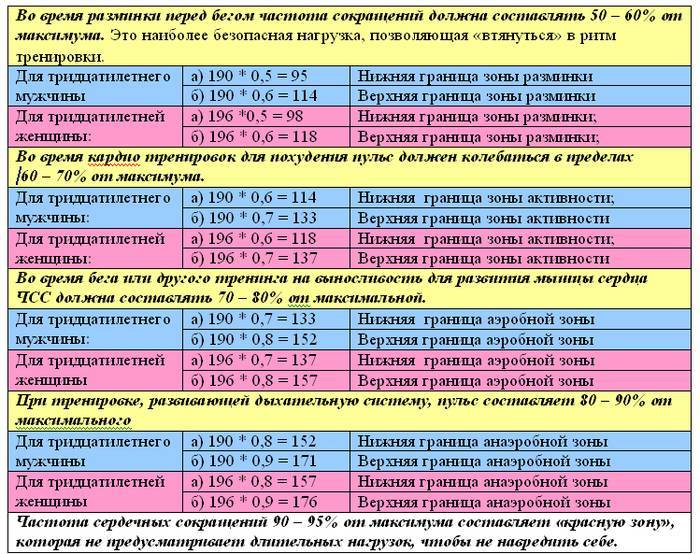 С.
С.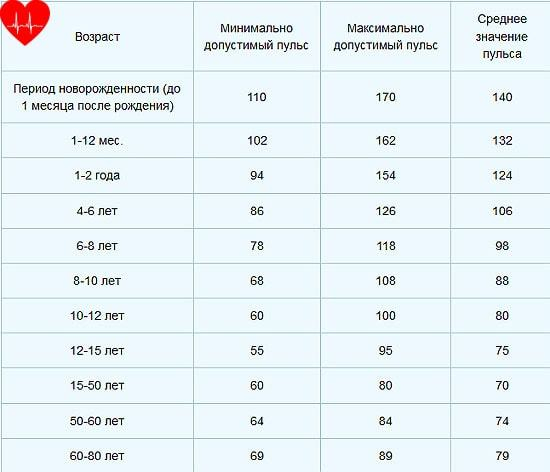 Артериальное давление может быть слишком низким или слишком высоким.Соблюдение диеты с упором на фрукты и овощи, сокращение потребления соли, регулярное вырезание и поддержание здорового веса могут помочь держать ваше кровяное давление под контролем.
Артериальное давление может быть слишком низким или слишком высоким.Соблюдение диеты с упором на фрукты и овощи, сокращение потребления соли, регулярное вырезание и поддержание здорового веса могут помочь держать ваше кровяное давление под контролем. Он может ходить, подниматься по лестнице и даже тренироваться на эллиптическом тренажере без каких-либо симптомов.
Он может ходить, подниматься по лестнице и даже тренироваться на эллиптическом тренажере без каких-либо симптомов.
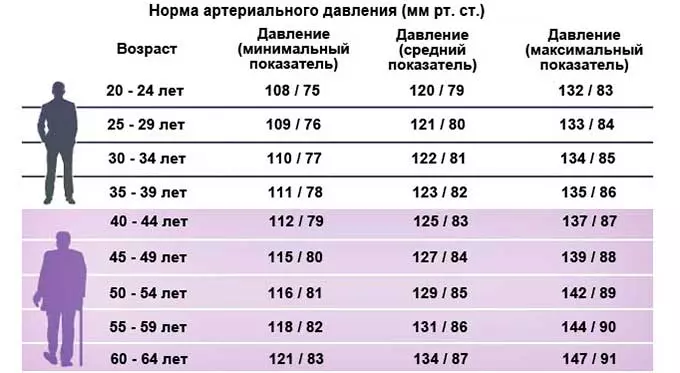 Его направили к электрофизиологу, и в качестве лечебной меры была рекомендована абляция. Пациент изначально не решался проводить инвазивную процедуру и предпочел попробовать флекаинид.
Его направили к электрофизиологу, и в качестве лечебной меры была рекомендована абляция. Пациент изначально не решался проводить инвазивную процедуру и предпочел попробовать флекаинид.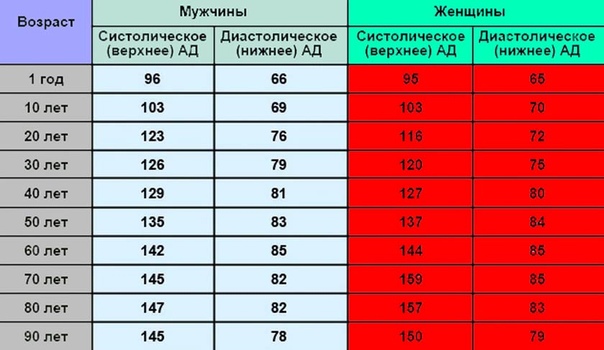 и др. Структура, функция и клиническая значимость проводящей системы сердца, включая атриовентрикулярное кольцо и ткани тракта оттока. Pharmacol Ther . 139 (2): 260—288.
и др. Структура, функция и клиническая значимость проводящей системы сердца, включая атриовентрикулярное кольцо и ткани тракта оттока. Pharmacol Ther . 139 (2): 260—288.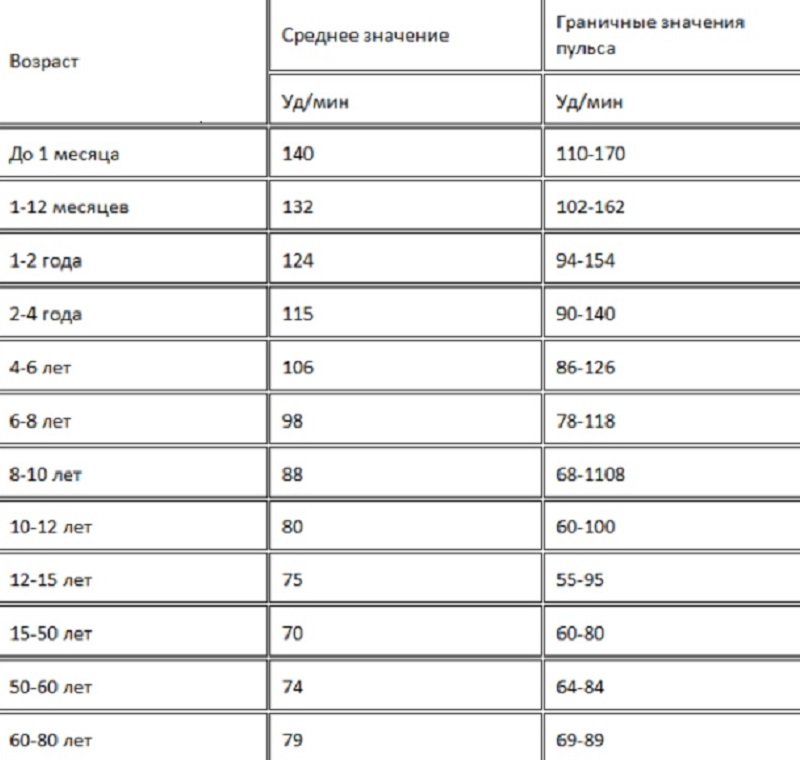 Другие мои лекарства включают тироксин. Мне 90 лет, хорошее здоровье, легкий артрит, внимательный и ориентированный.Что могло вызвать такой эпизод?
Другие мои лекарства включают тироксин. Мне 90 лет, хорошее здоровье, легкий артрит, внимательный и ориентированный.Что могло вызвать такой эпизод? Показатель 160 у 90-летнего небезопасен, и тот факт, что у вас снизилось артериальное давление, вызывает беспокойство: я бы подумал о том, чтобы госпитализировать вас в этой ситуации, и, конечно, порекомендовал бы вас осмотреть и сделайте ЭКГ в то время.
Показатель 160 у 90-летнего небезопасен, и тот факт, что у вас снизилось артериальное давление, вызывает беспокойство: я бы подумал о том, чтобы госпитализировать вас в этой ситуации, и, конечно, порекомендовал бы вас осмотреть и сделайте ЭКГ в то время.
 Ваш пульс ниже, когда вы отдыхаете, и повышается, когда вы занимаетесь спортом, а ваше сердце больше работает, чтобы обеспечить жизненно важные органы богатой кислородом кровью.Согласно Medline Plus, пожилые женщины имеют такой же нормальный диапазон пульса в состоянии покоя, что и их более молодые сверстницы.
Ваш пульс ниже, когда вы отдыхаете, и повышается, когда вы занимаетесь спортом, а ваше сердце больше работает, чтобы обеспечить жизненно важные органы богатой кислородом кровью.Согласно Medline Plus, пожилые женщины имеют такой же нормальный диапазон пульса в состоянии покоя, что и их более молодые сверстницы.
 У 70-летней женщины в плохой физической форме частота сердечных сокращений может составлять 84 или более ударов в минуту, в то время как ее подруга того же возраста в хорошей форме может бегать от 65 до 68 ударов в минуту. 70-летняя спортивная женщина в хорошей физической форме может ожидать пульс в состоянии покоя от 54 до 59.
У 70-летней женщины в плохой физической форме частота сердечных сокращений может составлять 84 или более ударов в минуту, в то время как ее подруга того же возраста в хорошей форме может бегать от 65 до 68 ударов в минуту. 70-летняя спортивная женщина в хорошей физической форме может ожидать пульс в состоянии покоя от 54 до 59. Некоторые говорят, что вместо того, чтобы рисовать линию со скоростью 100 ударов в минуту, поводом для беспокойства может считаться любое значение выше 90 — а, возможно, даже 80.
Некоторые говорят, что вместо того, чтобы рисовать линию со скоростью 100 ударов в минуту, поводом для беспокойства может считаться любое значение выше 90 — а, возможно, даже 80.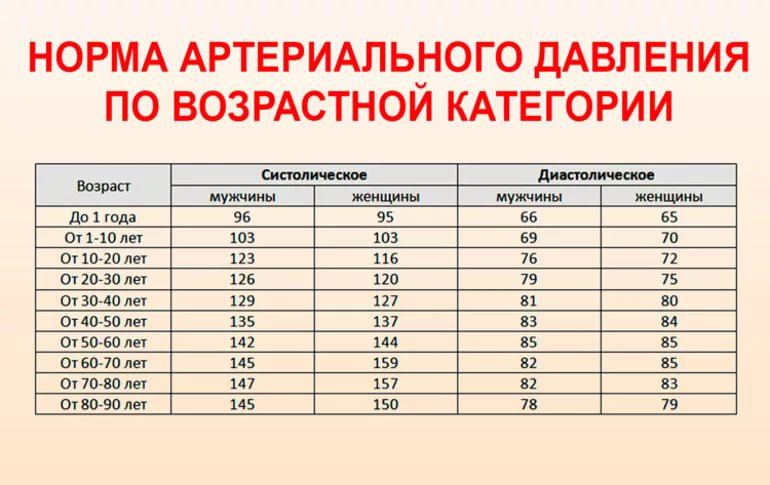

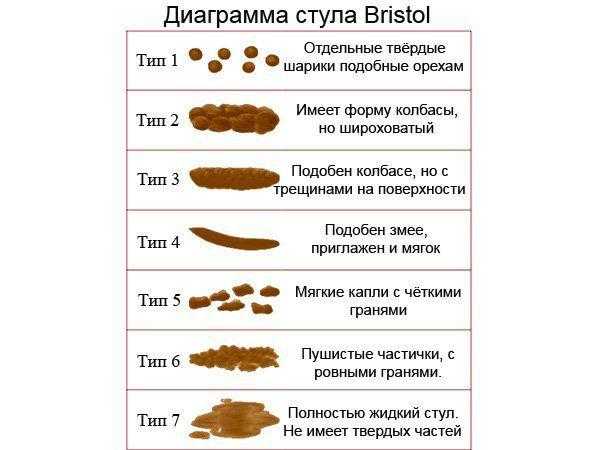
 Льюисом из Школы медицины] Кардиффского университета). Известна также как «Шкала Мейерса» (англ. Meyers Scale).
Льюисом из Школы медицины] Кардиффского университета). Известна также как «Шкала Мейерса» (англ. Meyers Scale).
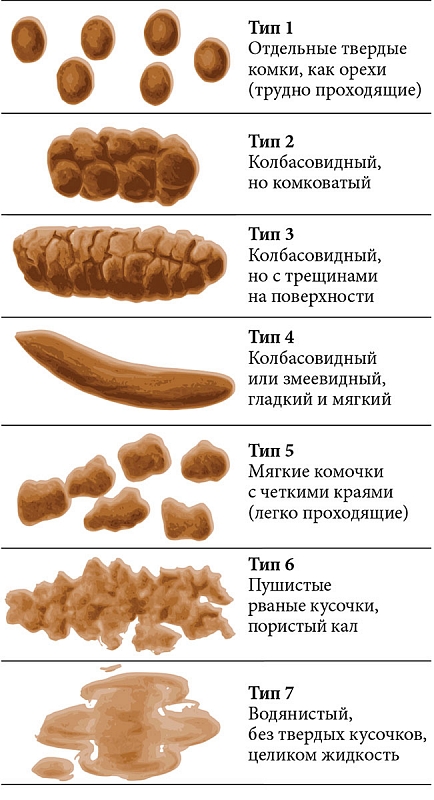



 В течение первого месяца ребенок может какать от одного до четырех раз каждые сутки, хотя некоторые малыши делают это реже. Чаще всего новорожденный при этом морщится и прикладывает видимые усилия.
В течение первого месяца ребенок может какать от одного до четырех раз каждые сутки, хотя некоторые малыши делают это реже. Чаще всего новорожденный при этом морщится и прикладывает видимые усилия. Также существует вероятность небольших запоров, вызванных составом смеси. Если вы заметили подобные проблемы, стоит перейти на другую смесь. Кроме того, необходимо проконсультироваться с педиатром. Дети, питающиеся грудным молоком, в большинстве не страдают от запоров.
Также существует вероятность небольших запоров, вызванных составом смеси. Если вы заметили подобные проблемы, стоит перейти на другую смесь. Кроме того, необходимо проконсультироваться с педиатром. Дети, питающиеся грудным молоком, в большинстве не страдают от запоров. Некоторые люди могут ходить в туалет один раз в да-три дня. Это, конечно не может считаться нормальным процессом, но и к патологическим их отнести нельзя, если других отклонений нет (цвет, форма, запах).
Некоторые люди могут ходить в туалет один раз в да-три дня. Это, конечно не может считаться нормальным процессом, но и к патологическим их отнести нельзя, если других отклонений нет (цвет, форма, запах).
 Последние также должны вызывать тревогу и быть поводом обратиться за медицинской помощью.
Последние также должны вызывать тревогу и быть поводом обратиться за медицинской помощью.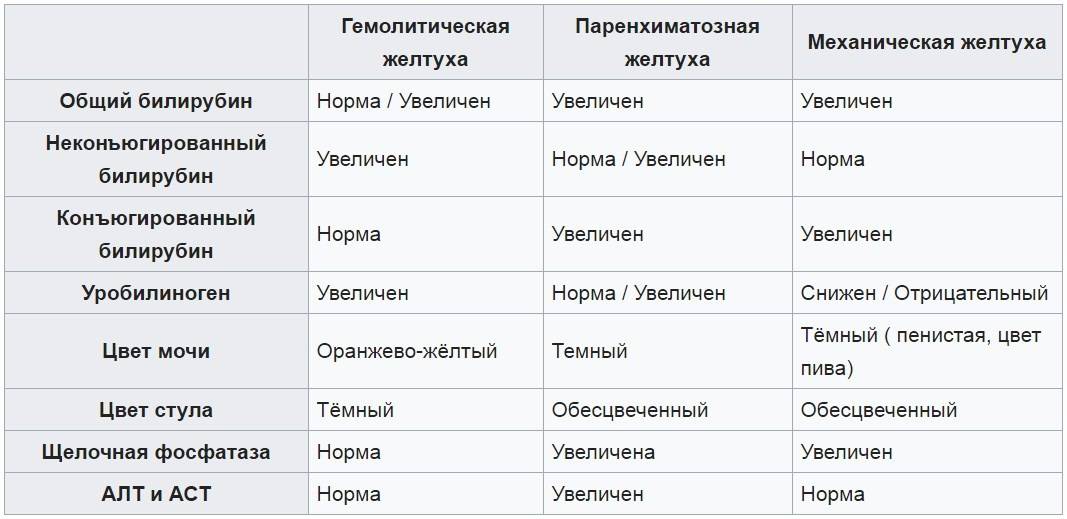
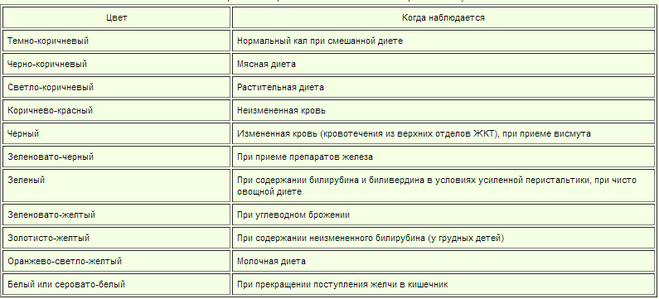
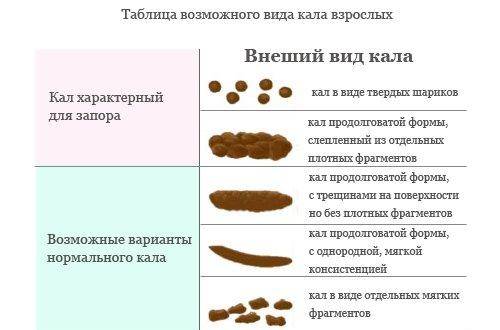
 Если же продуктов, провоцирующих изменение стула в рационе, не было, тогда следует обратиться к доктору, который на основании симптомов и дополнительного обследования определит причину и назначит адекватное лечение.
Если же продуктов, провоцирующих изменение стула в рационе, не было, тогда следует обратиться к доктору, который на основании симптомов и дополнительного обследования определит причину и назначит адекватное лечение. Это считается нормой. По консистенции кал здорового младенца зернистый и пастообразный, иногда жидкий. У малышей на ГВ нормальный стул имеет сладковатый запах.
Это считается нормой. По консистенции кал здорового младенца зернистый и пастообразный, иногда жидкий. У малышей на ГВ нормальный стул имеет сладковатый запах. В этот период обычно начинается прикорм «зеленой» пищей, например, брокколи, шпинатом или горошком. Подобная пища приводит к изменению цвета какашек. Также зеленый кал встречается у малышей, которым дают добавки железа.
В этот период обычно начинается прикорм «зеленой» пищей, например, брокколи, шпинатом или горошком. Подобная пища приводит к изменению цвета какашек. Также зеленый кал встречается у малышей, которым дают добавки железа. Это сигнал возможной инфекции или пищевой аллергии. Диарею необходимо лечить с первого же дня, потому что жидкий стул может быстро привести к обезвоживанию детского организма.
Это сигнал возможной инфекции или пищевой аллергии. Диарею необходимо лечить с первого же дня, потому что жидкий стул может быстро привести к обезвоживанию детского организма.
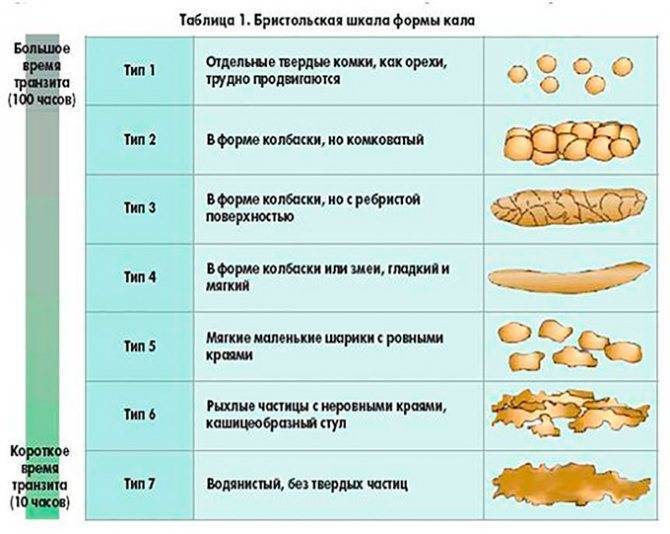


 Её воспаление приводит к снижению секреции панкреатического сока и неполному расщеплению еды, попадающей в двенадцатипёрстную кишку. Помимо этого, отёк и компрессия отводящих протоков — причина нарушения выхода жёлчи из пузыря. При этом каловые массы становятся светлыми или бесцветными. Оттенок зависит от уровня закупорки выводных путей.
Её воспаление приводит к снижению секреции панкреатического сока и неполному расщеплению еды, попадающей в двенадцатипёрстную кишку. Помимо этого, отёк и компрессия отводящих протоков — причина нарушения выхода жёлчи из пузыря. При этом каловые массы становятся светлыми или бесцветными. Оттенок зависит от уровня закупорки выводных путей. Больному назначают анальгетики, спазмолитики, ферменты, лечебную диету. Возвращение свойств кала к норме человек отмечает после стихания клинических проявлений болезни.
Больному назначают анальгетики, спазмолитики, ферменты, лечебную диету. Возвращение свойств кала к норме человек отмечает после стихания клинических проявлений болезни. Пациенту назначаются пробиотики и диета. Сложные гастроэнтериты – показание для применения антибиотиков и инфузионной детоксикации. Цвет стула нормализуется после устранения причины сбоев.
Пациенту назначаются пробиотики и диета. Сложные гастроэнтериты – показание для применения антибиотиков и инфузионной детоксикации. Цвет стула нормализуется после устранения причины сбоев.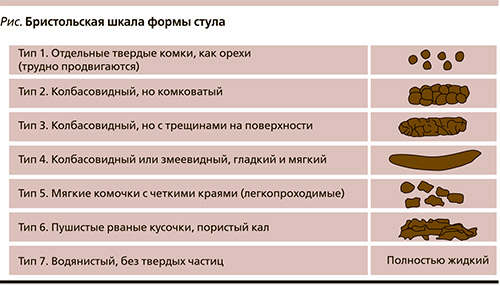
 Желтуха инфекционного происхождения больше не является приговором.
Желтуха инфекционного происхождения больше не является приговором.

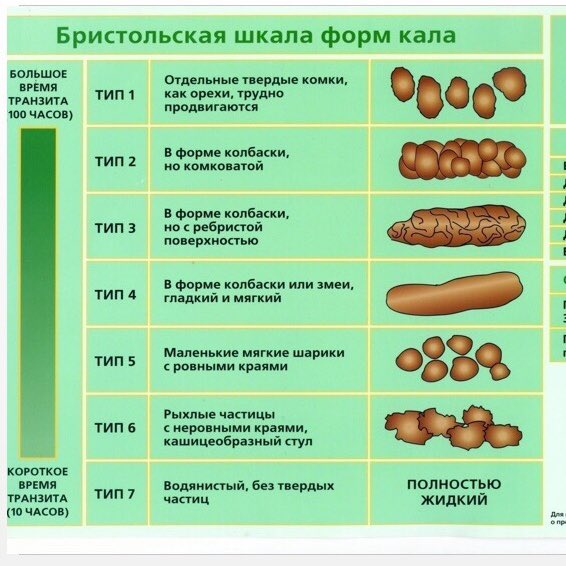 При наличии органической патологии больная структура может выглядеть отёкшей, увеличенной. При функциональных нарушениях визуально заметных изменений нет. В такой ситуации диагноз ставится на основании лабораторных обследований и проб.
При наличии органической патологии больная структура может выглядеть отёкшей, увеличенной. При функциональных нарушениях визуально заметных изменений нет. В такой ситуации диагноз ставится на основании лабораторных обследований и проб.
 Но его оттенок может варьироваться в зависимости от типа диеты, питающей организм.
Но его оттенок может варьироваться в зависимости от типа диеты, питающей организм.
 В том случае, если в кишечник попадает большое количество свеклы, красного винограда или чернослива, то стул темнеет и может быть черного цвета. При подозрении на то, что именно продукты спровоцировали изменение окраски стула, то необходимо исключить их на несколько дней из своего рациона и внимательно следить за окраской каловых масс. В том случае, если спустя 3-4 дня после того, как человек перестал потреблять такие продукты кал остается черным, то необходимо искать иную причину такой патологии.
В том случае, если в кишечник попадает большое количество свеклы, красного винограда или чернослива, то стул темнеет и может быть черного цвета. При подозрении на то, что именно продукты спровоцировали изменение окраски стула, то необходимо исключить их на несколько дней из своего рациона и внимательно следить за окраской каловых масс. В том случае, если спустя 3-4 дня после того, как человек перестал потреблять такие продукты кал остается черным, то необходимо искать иную причину такой патологии.

 Именно по этой причине при окрашивании стула в темный или черный цвет рекомендуется посетить врача и пройти все необходимые исследования.
Именно по этой причине при окрашивании стула в темный или черный цвет рекомендуется посетить врача и пройти все необходимые исследования.
 При кровотечении в пищеварительной системе лечение таблетками не принесет положительного эффекта и обычно требуется помощь специалиста. Самостоятельное лечение таких патологий, как дивертикулит и язва желудка, может быть крайне опасно и возможно появление дополнительных осложнений.
При кровотечении в пищеварительной системе лечение таблетками не принесет положительного эффекта и обычно требуется помощь специалиста. Самостоятельное лечение таких патологий, как дивертикулит и язва желудка, может быть крайне опасно и возможно появление дополнительных осложнений.


 В данном случае меняется и цвет фекалий, запах, химический состав и консистенция.
В данном случае меняется и цвет фекалий, запах, химический состав и консистенция. У людей с удаленным желчным пузырем эта четко установленная функция отсутствует.
У людей с удаленным желчным пузырем эта четко установленная функция отсутствует.
 Поэтому при первых признаках диареи следует установить ее этиологию и в максимально быстрые сроки приступить к лечению.
Поэтому при первых признаках диареи следует установить ее этиологию и в максимально быстрые сроки приступить к лечению. Они также подавляют патогенные микроорганизмы и бактерии. Самыми эффективными в этом плане считаются бификол, лактобактерин и линекс.
Они также подавляют патогенные микроорганизмы и бактерии. Самыми эффективными в этом плане считаются бификол, лактобактерин и линекс. Первый рефлекс, который на них реагирует, именно рвотный.
Первый рефлекс, который на них реагирует, именно рвотный. Но при нарушениях в работе организма цвет стула может измениться до светлого, бело-желтого, серого, как глина, землистого, желто-зеленого, зелено-серого, песочного, желто-коричневого, оранжевого, темно-оранжевого, красного или черного. Разноцветный кал не есть норма, но встречается он достаточно редко, самым же распространенным цветом измененных фекалий является жёлтый.
Но при нарушениях в работе организма цвет стула может измениться до светлого, бело-желтого, серого, как глина, землистого, желто-зеленого, зелено-серого, песочного, желто-коричневого, оранжевого, темно-оранжевого, красного или черного. Разноцветный кал не есть норма, но встречается он достаточно редко, самым же распространенным цветом измененных фекалий является жёлтый.

 Но если ни одна из вышеперечисленных причин не подходит, то следует подумать, о чем это говорит, и нацелиться на более неприятные факторы.
Но если ни одна из вышеперечисленных причин не подходит, то следует подумать, о чем это говорит, и нацелиться на более неприятные факторы.

 Далее он назначит лечение исходя из установленного диагноза.
Далее он назначит лечение исходя из установленного диагноза.

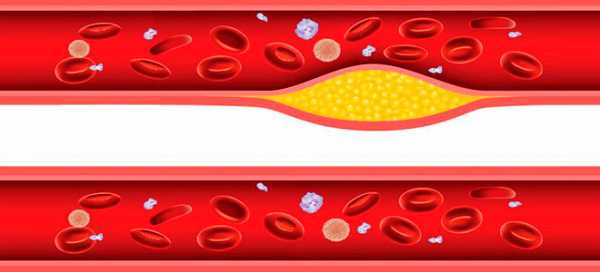


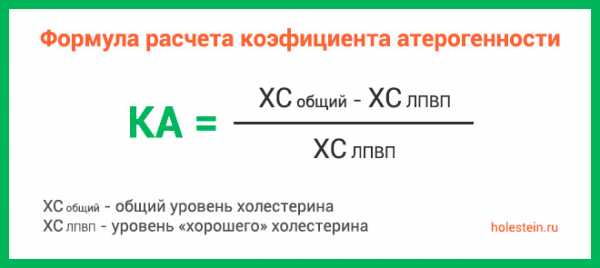
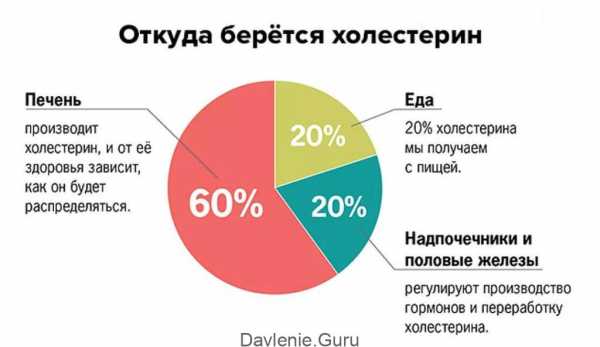

 Уровень холестерина в крови очень важно поддерживать в норме. Ведь от этого зависит наше здоровье, долголетие и радость в жизни.
Уровень холестерина в крови очень важно поддерживать в норме. Ведь от этого зависит наше здоровье, долголетие и радость в жизни.


 Холестерин по размеру и составу может быть плохим и хорошим
Холестерин по размеру и составу может быть плохим и хорошим








 днако, поводов для серьезного беспокойства нет, в период вынашивания ребенка ее сердце функционирует за двоих и способно выдержать такую нагрузку.
днако, поводов для серьезного беспокойства нет, в период вынашивания ребенка ее сердце функционирует за двоих и способно выдержать такую нагрузку.
 Переохлаждение или долгое пребывание на солнце, чрезмерное принятие кофеиносодержащих напитков или обильное застолье также могут повысить пульсацию. При устранении этих причин все восстановится.
Переохлаждение или долгое пребывание на солнце, чрезмерное принятие кофеиносодержащих напитков или обильное застолье также могут повысить пульсацию. При устранении этих причин все восстановится. К 20 годам женский организм окончательно формируется. Он наконец-таки прошел юношескую пертурбацию.
К 20 годам женский организм окончательно формируется. Он наконец-таки прошел юношескую пертурбацию. У женщин более частый ритм сердца, чем у противоположного пола. Это обусловлено тем, что дамы более низкорослые, чем мужчины, поэтому их система кровообращения короче, что позволяет крови проходить круг за более короткий промежуток времени.
У женщин более частый ритм сердца, чем у противоположного пола. Это обусловлено тем, что дамы более низкорослые, чем мужчины, поэтому их система кровообращения короче, что позволяет крови проходить круг за более короткий промежуток времени. Какой пульс считается нормальным у женщин 40 лет? Многие зрелые женщины отмечают, что перейдя сороковую отметку, их организм замедляет свои обороты и начинает потихоньку стареть.
Какой пульс считается нормальным у женщин 40 лет? Многие зрелые женщины отмечают, что перейдя сороковую отметку, их организм замедляет свои обороты и начинает потихоньку стареть. После наступления менопаузы женщинам необходимо чаще проверять здоровье, чтобы исключить или же вовремя заметить болезнь.
После наступления менопаузы женщинам необходимо чаще проверять здоровье, чтобы исключить или же вовремя заметить болезнь.







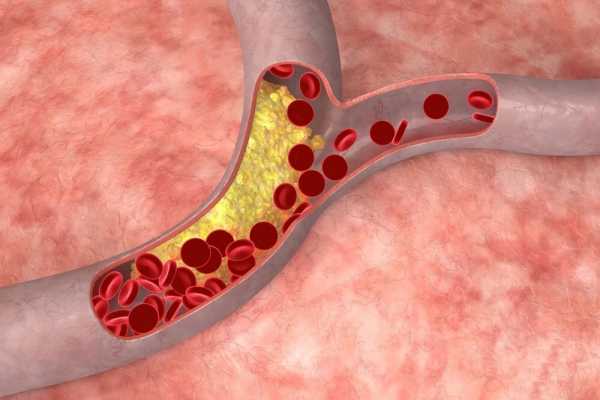





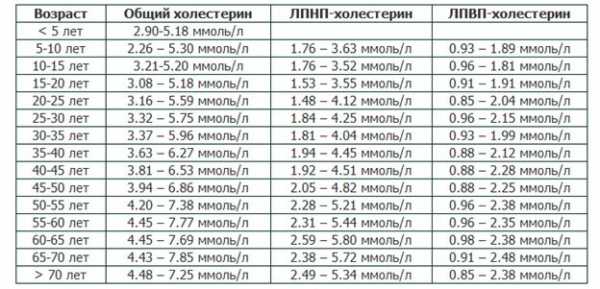
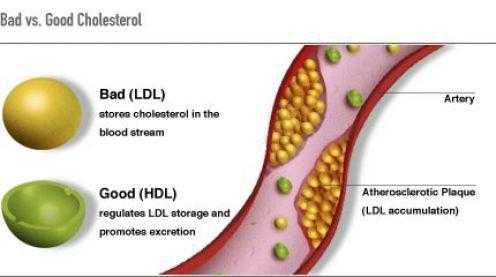

















 Если обследование назначено на вечернее время, разрешается с утра пить воду.
Если обследование назначено на вечернее время, разрешается с утра пить воду.
 Насыщение периферической крови кислородом (сатурация). Отклонение данного показателя от нормы может указывать на проблемы с дыханием, а также сердечно-сосудистой деятельностью. Прибор позволяет выявить это еще до появления иных симптомов. Косвенными признаками недостатка кислорода является посинение кожного покрова, изменение сердечного ритма, слабость и ухудшение общего состояния организма.;
Насыщение периферической крови кислородом (сатурация). Отклонение данного показателя от нормы может указывать на проблемы с дыханием, а также сердечно-сосудистой деятельностью. Прибор позволяет выявить это еще до появления иных симптомов. Косвенными признаками недостатка кислорода является посинение кожного покрова, изменение сердечного ритма, слабость и ухудшение общего состояния организма.; Это компактный прибор в виде прищепки, которая крепится на палец. Для измерения не требуется нарушать целостность кожи – устройство определяет насыщение крови кислородом сквозь нее за счет двух световых волн, имеющих разный спектр. Длительность регистрации данных зависит от цели исследования. Для разового определения насыщения крови кислородом достаточно нескольких минут, то есть это показатель состояния пользователя в конкретный момент времени. Поскольку данные показатели, при наличии определенных заболеваний и сопутствующих факторов могут быстро меняться, то более полную картину даст длительный мониторинг. Для более информативных данных следует исследовать изменения показателей в ночное и дневное время, при физических нагрузках и в других различных условиях.
Это компактный прибор в виде прищепки, которая крепится на палец. Для измерения не требуется нарушать целостность кожи – устройство определяет насыщение крови кислородом сквозь нее за счет двух световых волн, имеющих разный спектр. Длительность регистрации данных зависит от цели исследования. Для разового определения насыщения крови кислородом достаточно нескольких минут, то есть это показатель состояния пользователя в конкретный момент времени. Поскольку данные показатели, при наличии определенных заболеваний и сопутствующих факторов могут быстро меняться, то более полную картину даст длительный мониторинг. Для более информативных данных следует исследовать изменения показателей в ночное и дневное время, при физических нагрузках и в других различных условиях.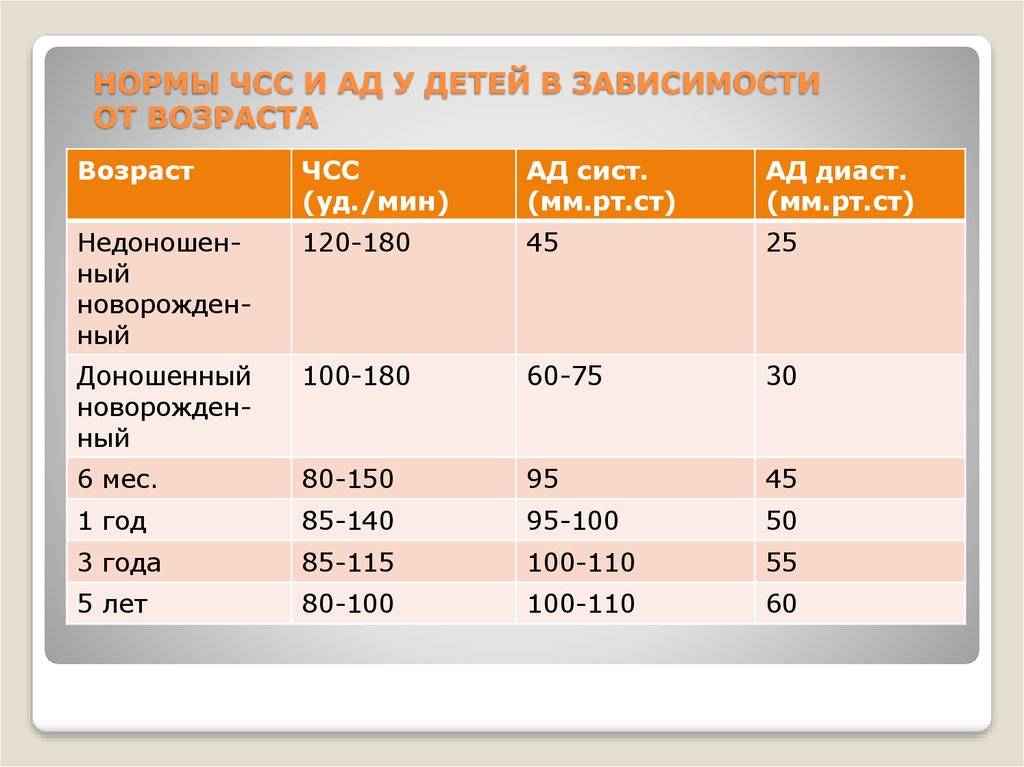 Когда человек находится под наркозом он не может контролировать свое состояние и неизвестно, как его организм отреагирует на препарат, поэтому требуется пульсоксиметр. Это позволяет врачу видеть малейшие изменения в состоянии пациента и при необходимости, поддерживать жизненно важные процессы;
Когда человек находится под наркозом он не может контролировать свое состояние и неизвестно, как его организм отреагирует на препарат, поэтому требуется пульсоксиметр. Это позволяет врачу видеть малейшие изменения в состоянии пациента и при необходимости, поддерживать жизненно важные процессы; Есть портативные и стационарные приборы. Первый вариант удобен для самостоятельного использования в домашних условиях, для врачей скорой помощи, спортивных медиков. Стационарные модели в основном применяются в клинических условиях;
Есть портативные и стационарные приборы. Первый вариант удобен для самостоятельного использования в домашних условиях, для врачей скорой помощи, спортивных медиков. Стационарные модели в основном применяются в клинических условиях;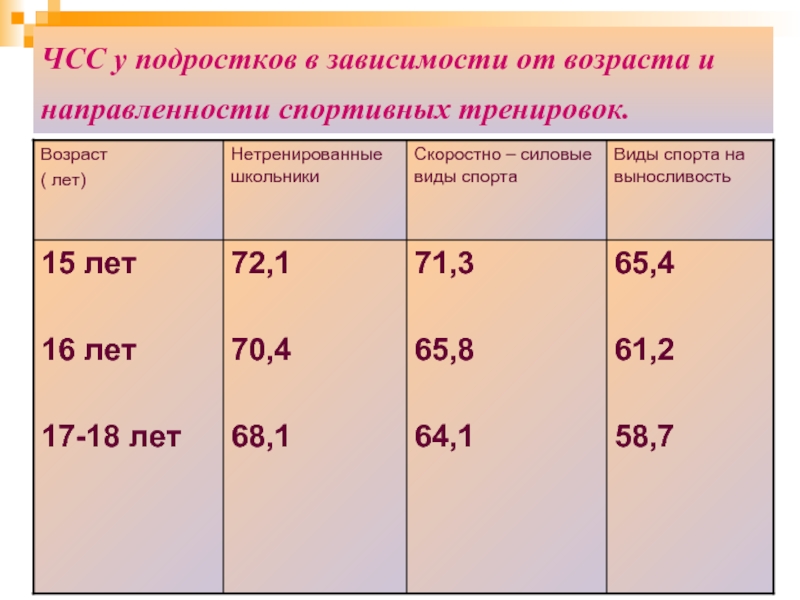
 Величина до 20% означает отличную реакцию сердечно-сосудистой системы на нагрузку, от 21 до 40 % — хорошую; от 41 до 65% -удовлетворительную; от 66 до 75% — плохую; от 76 и более — очень плохую.
Величина до 20% означает отличную реакцию сердечно-сосудистой системы на нагрузку, от 21 до 40 % — хорошую; от 41 до 65% -удовлетворительную; от 66 до 75% — плохую; от 76 и более — очень плохую.
 Белый или красный демограф может наблюдаться при отклонениях в деятельности вегетативной нервной системы (при переутомлении, во время болезни, при неполном выздоровлении).
Белый или красный демограф может наблюдаться при отклонениях в деятельности вегетативной нервной системы (при переутомлении, во время болезни, при неполном выздоровлении).
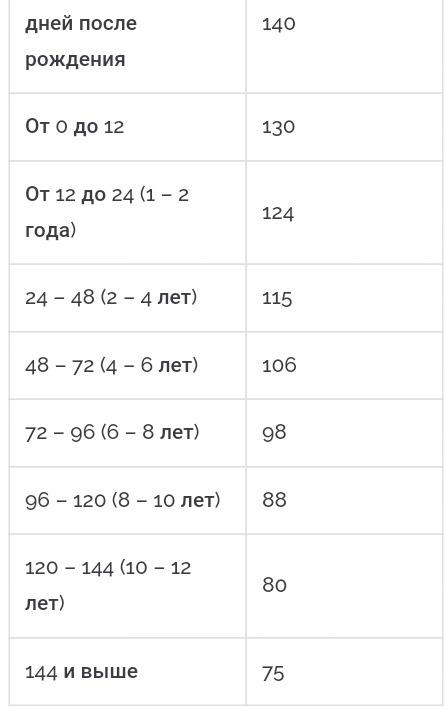 Примерами этих упражнений являются: бег и кросс на 1000, 2000, 2500, 3000, 5000м; плавание на 200.400, 500 м, бег 12 мин.
Примерами этих упражнений являются: бег и кросс на 1000, 2000, 2500, 3000, 5000м; плавание на 200.400, 500 м, бег 12 мин.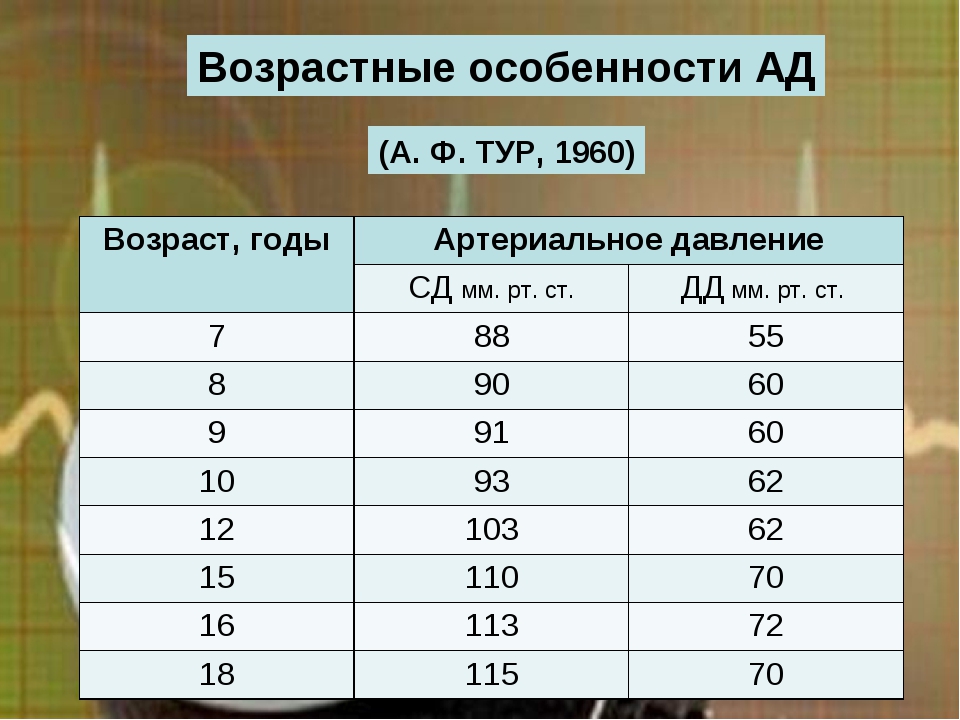 Любое отклонение от нормального поведения является причиной для беспокойства. Если в норме ваша кошка держится независимо, а тут вдруг ищет вашего общества и не отходит от вас ни на шаг или, наоборот, целый день не покидает своего места, то постарайтесь выяснить, что случилось.
Любое отклонение от нормального поведения является причиной для беспокойства. Если в норме ваша кошка держится независимо, а тут вдруг ищет вашего общества и не отходит от вас ни на шаг или, наоборот, целый день не покидает своего места, то постарайтесь выяснить, что случилось.
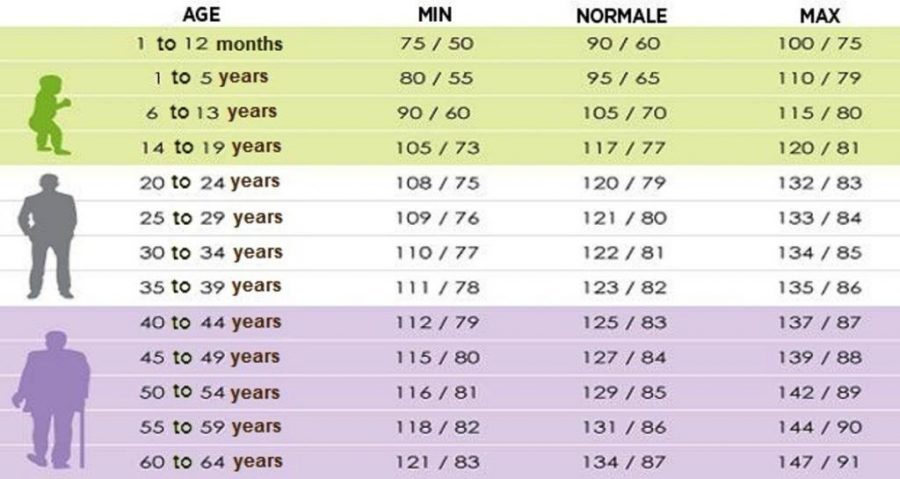 Кроме того, беременные или кормящие кошки дышат с большей частотой, чем в норме. На частоту дыхания влияют также размеры и генетические факторы: мелкие кошки дышат чаще крупных, что объясняется более высоким уровнем обмена веществ и соответственно — повышенной теплопотерей. Изменения в частоте дыхания вашей кошки могут быть вызваны страхом, болью, шоком, заболеваниями респираторной системы. Нужно учитывать также, что дыхание учащается в жаркую погоду, при физической нагрузке, при возбуждении кошки. Дыхание здорового животного после нагрузок восстанавливается за несколько минут. Затруднение дыхания может быть вызвано тепловым ударом или, в редких случаях, нехваткой кальция в крови в период лактации у самок. Животное может задыхаться при сердечной недостаточности, при воспалениях мочеполовой системы, а также при заглатывании инородного предмета.
Кроме того, беременные или кормящие кошки дышат с большей частотой, чем в норме. На частоту дыхания влияют также размеры и генетические факторы: мелкие кошки дышат чаще крупных, что объясняется более высоким уровнем обмена веществ и соответственно — повышенной теплопотерей. Изменения в частоте дыхания вашей кошки могут быть вызваны страхом, болью, шоком, заболеваниями респираторной системы. Нужно учитывать также, что дыхание учащается в жаркую погоду, при физической нагрузке, при возбуждении кошки. Дыхание здорового животного после нагрузок восстанавливается за несколько минут. Затруднение дыхания может быть вызвано тепловым ударом или, в редких случаях, нехваткой кальция в крови в период лактации у самок. Животное может задыхаться при сердечной недостаточности, при воспалениях мочеполовой системы, а также при заглатывании инородного предмета. Движения могут стать неловкими, координация их нарушается. Признаками начала заболевания служат также быстрая утомляемость, нарушение аппетита, бессонница или наоборот — повышенная сонливость.
Движения могут стать неловкими, координация их нарушается. Признаками начала заболевания служат также быстрая утомляемость, нарушение аппетита, бессонница или наоборот — повышенная сонливость. ), прищуривание и слезотечение могут отражать боль в глазу, при ряде заболеваний наблюдается желтушность слизистой оболочки, воспаление век. При конъюнктивите, отравлениях и некоторых других случаях глаза иногда оказываются полузакрыты третьим веком.
), прищуривание и слезотечение могут отражать боль в глазу, при ряде заболеваний наблюдается желтушность слизистой оболочки, воспаление век. При конъюнктивите, отравлениях и некоторых других случаях глаза иногда оказываются полузакрыты третьим веком. Осветленные фекалии служат признаком заболевания печени (недостаток желчи и др.). Пенистые фекалии — показатель бактериальной инфекции.
Осветленные фекалии служат признаком заболевания печени (недостаток желчи и др.). Пенистые фекалии — показатель бактериальной инфекции.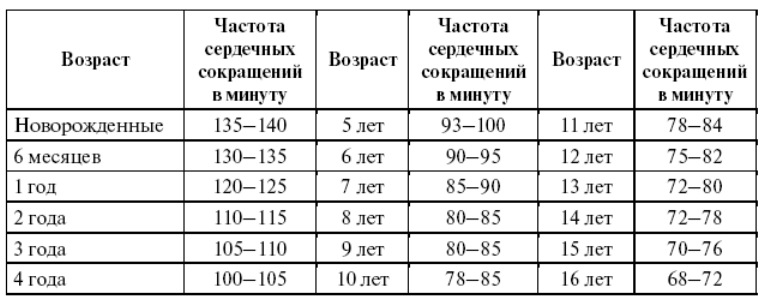 Затрудненное дыхание наблюдают при плеврите, сердечной недостаточности, анемии, сердечных глистах. У старых кошек признаком сердечной недостаточности может быть кашель.
Затрудненное дыхание наблюдают при плеврите, сердечной недостаточности, анемии, сердечных глистах. У старых кошек признаком сердечной недостаточности может быть кашель.
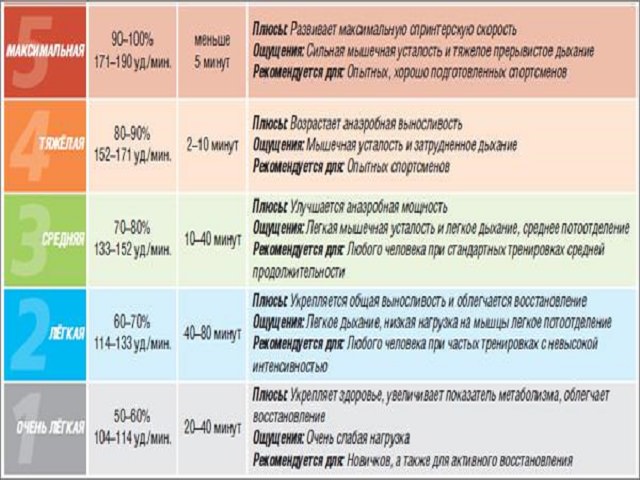 Такая преемственность позволила провести комплексное исследование не только того, как RHR может измениться после отклонений от времени отхода ко сну, но также и среднего временного окна, необходимого для возврата RHR к исходному уровню.
Такая преемственность позволила провести комплексное исследование не только того, как RHR может измениться после отклонений от времени отхода ко сну, но также и среднего временного окна, необходимого для возврата RHR к исходному уровню. Отбор производился в порядке очереди в соответствии с общим демографическим распределением университета.
Отбор производился в порядке очереди в соответствии с общим демографическим распределением университета. 3C, D), а еще 2207 сеансов сна были исключены, поскольку данные о физической активности за предыдущий день отсутствовали (рис.3E). На этом этапе для анализа оставалась когорта из 599 участников.
3C, D), а еще 2207 сеансов сна были исключены, поскольку данные о физической активности за предыдущий день отсутствовали (рис.3E). На этом этапе для анализа оставалась когорта из 599 участников. Остальные десять категорий сосредоточились на отклонениях от этого исходного уровня, произошедших раньше или позже.Интервалы для этих категорий отклонений составляли [1, 30) мин., [30, 60) мин., [1, 2) ч., [2, 3) ч. И ≥3 ч.
Остальные десять категорий сосредоточились на отклонениях от этого исходного уровня, произошедших раньше или позже.Интервалы для этих категорий отклонений составляли [1, 30) мин., [30, 60) мин., [1, 2) ч., [2, 3) ч. И ≥3 ч. Как мы видели на предыдущих этапах обработки, можно разумно ожидать, что оно будет справедливым для приблизительно нормального распределения записей сна каждого студента.Кроме того, поскольку вариационный вывод добавляет уровень регуляризации по сравнению с традиционными подходами GMM, BGMM может обеспечить более надежную оценку истинных базовых моделей сна, необходимых для устранения двусмысленного представления о дремоте из данных. Более того, чтобы избежать предположений об основной природе кластеров сна, BGMM соответствовала структурам полной ковариации, позволяя каждому идентифицированному компоненту варьироваться как по направлению, так и по форме.
Как мы видели на предыдущих этапах обработки, можно разумно ожидать, что оно будет справедливым для приблизительно нормального распределения записей сна каждого студента.Кроме того, поскольку вариационный вывод добавляет уровень регуляризации по сравнению с традиционными подходами GMM, BGMM может обеспечить более надежную оценку истинных базовых моделей сна, необходимых для устранения двусмысленного представления о дремоте из данных. Более того, чтобы избежать предположений об основной природе кластеров сна, BGMM соответствовала структурам полной ковариации, позволяя каждому идентифицированному компоненту варьироваться как по направлению, так и по форме. Учитывая, что сеансы сна в кластере 2 имели в среднем более короткую продолжительность и большие отклонения от нормального времени отхода ко сну, мы удалили сеансы сна в этом кластере из нашего анализа, поскольку они больше напоминали характеристики дневного сна (рис.3е). При этом также были удалены три участника, эти участники, вероятно, носили свое устройство только во время сна, но удаляли устройство перед сном, не сумев зафиксировать полные ночи сна. Кроме того, мы удалили несколько оставшихся сеансов сна, в которых несколько сеансов все еще происходили в один и тот же день (рис. 3g).
Учитывая, что сеансы сна в кластере 2 имели в среднем более короткую продолжительность и большие отклонения от нормального времени отхода ко сну, мы удалили сеансы сна в этом кластере из нашего анализа, поскольку они больше напоминали характеристики дневного сна (рис.3е). При этом также были удалены три участника, эти участники, вероятно, носили свое устройство только во время сна, но удаляли устройство перед сном, не сумев зафиксировать полные ночи сна. Кроме того, мы удалили несколько оставшихся сеансов сна, в которых несколько сеансов все еще происходили в один и тот же день (рис. 3g). 3H) 37 .
3H) 37 .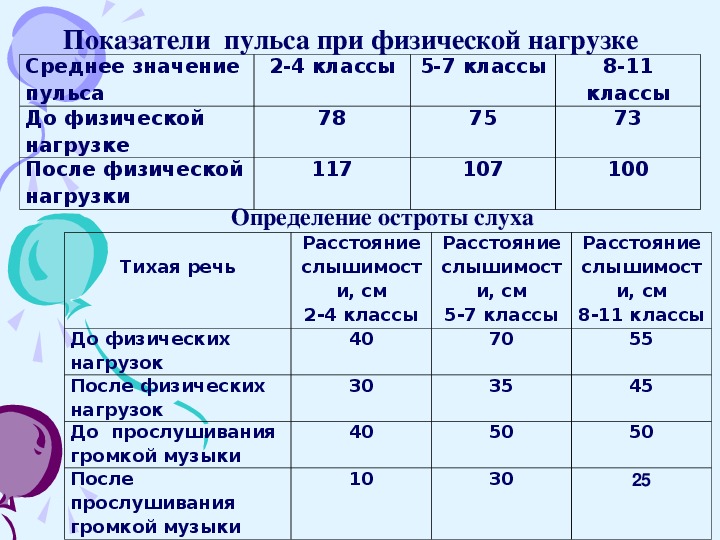 В частности, мы отслеживали RHR участников, начиная с того момента, когда они впервые ложились спать, до полуночи следующего дня. При этом необходимо было исследовать RHR в периоды, когда участники спали и бодрствовали. Учитывая, что на RHR могут влиять различные факторы в зависимости от того, когда человек спит или бодрствует, мы разделили их на два отдельных анализа, используя два разных подхода для наилучшего определения RHR для каждого состояния.
В частности, мы отслеживали RHR участников, начиная с того момента, когда они впервые ложились спать, до полуночи следующего дня. При этом необходимо было исследовать RHR в периоды, когда участники спали и бодрствовали. Учитывая, что на RHR могут влиять различные факторы в зависимости от того, когда человек спит или бодрствует, мы разделили их на два отдельных анализа, используя два разных подхода для наилучшего определения RHR для каждого состояния. Затем измеряли RHR, вычисляя медианное RHR для каждого часа сна в каждой ночной записи. Сеансы сна были обрезаны до 7 часов, чтобы избежать потери данных из-за разницы в продолжительности сеансов сна. Семь часов были выбраны специально, поскольку это была средняя продолжительность сна среди участников. Наконец, мы отмечаем, что при изучении RHR во время сна 14 877 сеансов отсутствовали данные RHR, вероятно, из-за отказа устройства, а не из-за того, что его не надевали, поскольку время отхода ко сну и продолжительность сна все еще регистрировались (обнаруживались акселерометром Fitbit).Таким образом, эти сеансы были исключены (рис. 3I).
Затем измеряли RHR, вычисляя медианное RHR для каждого часа сна в каждой ночной записи. Сеансы сна были обрезаны до 7 часов, чтобы избежать потери данных из-за разницы в продолжительности сеансов сна. Семь часов были выбраны специально, поскольку это была средняя продолжительность сна среди участников. Наконец, мы отмечаем, что при изучении RHR во время сна 14 877 сеансов отсутствовали данные RHR, вероятно, из-за отказа устройства, а не из-за того, что его не надевали, поскольку время отхода ко сну и продолжительность сна все еще регистрировались (обнаруживались акселерометром Fitbit).Таким образом, эти сеансы были исключены (рис. 3I).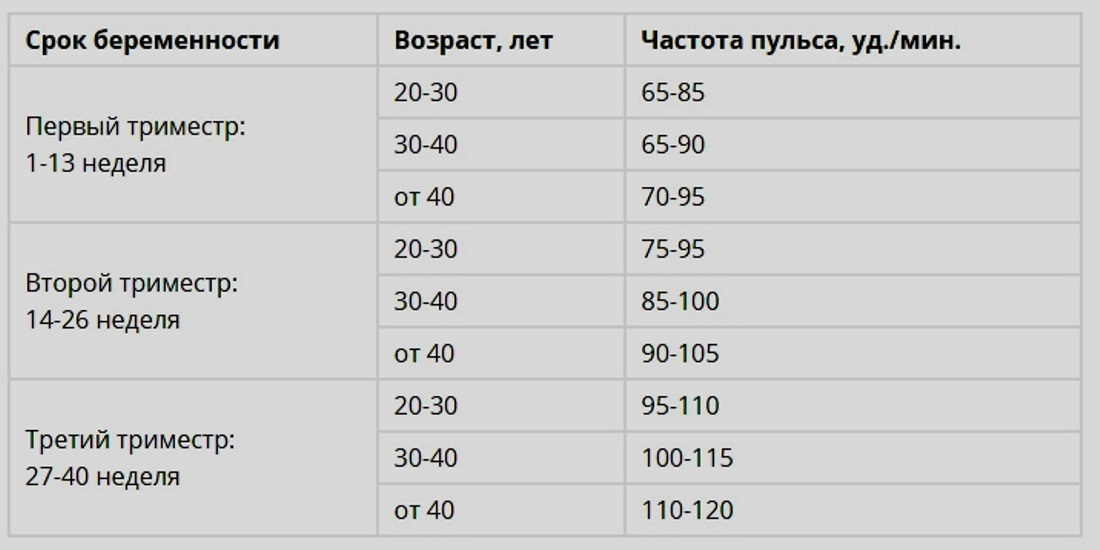 Вместо этого люди склонны придерживаться повседневного социального ритма, в котором события больше соответствуют времени суток, чем когда человек просыпается 40,41 .Например, если человек просыпается на час позже обычного, это не обязательно означает, что он также будет обедать на 1 час позже, чем обычно, поскольку время обеда определяется в большей степени временем суток. Дополнительные аспекты этих социальных ритмов могут включать соблюдение расписания занятий, уход и возвращение с работы и т. Д., Что может повлиять на RHR 40,41 . Поэтому при измерении RHR на следующий день мы вместо этого вычисляли медианное RHR для каждого часа дня (с 9:00 до 9:59, с 10:00 до 10:59 и т. Д.).), чтобы лучше сравнить RHR в этих социальных ритмах. Кроме того, чтобы зафиксировать RHR вместо HR, мы рассматривали только периоды, в которых участник был неактивен (без шагов) в течение как минимум 30 минут, в соответствии с предшествующей литературой, с измерениями, заканчивающимися, когда участник снова начал двигаться 42,43, 44 .
Вместо этого люди склонны придерживаться повседневного социального ритма, в котором события больше соответствуют времени суток, чем когда человек просыпается 40,41 .Например, если человек просыпается на час позже обычного, это не обязательно означает, что он также будет обедать на 1 час позже, чем обычно, поскольку время обеда определяется в большей степени временем суток. Дополнительные аспекты этих социальных ритмов могут включать соблюдение расписания занятий, уход и возвращение с работы и т. Д., Что может повлиять на RHR 40,41 . Поэтому при измерении RHR на следующий день мы вместо этого вычисляли медианное RHR для каждого часа дня (с 9:00 до 9:59, с 10:00 до 10:59 и т. Д.).), чтобы лучше сравнить RHR в этих социальных ритмах. Кроме того, чтобы зафиксировать RHR вместо HR, мы рассматривали только периоды, в которых участник был неактивен (без шагов) в течение как минимум 30 минут, в соответствии с предшествующей литературой, с измерениями, заканчивающимися, когда участник снова начал двигаться 42,43, 44 . Наконец, мы отмечаем, что при изучении RHR на следующий день 51 368 дней были исключены из-за отсутствия данных, так как участники, вероятно, не использовали свое устройство в течение этого дня (рис. 3J).
Наконец, мы отмечаем, что при изучении RHR на следующий день 51 368 дней были исключены из-за отсутствия данных, так как участники, вероятно, не использовали свое устройство в течение этого дня (рис. 3J).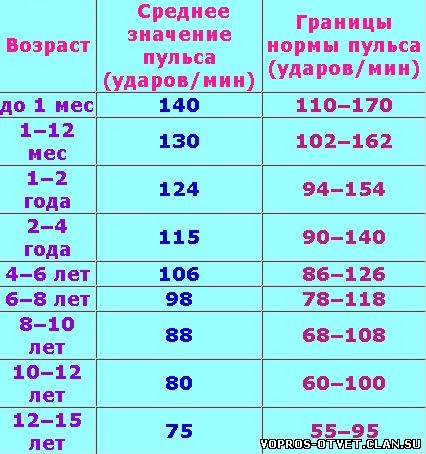 В то время как участник в основном проводил бы свое время в диапазоне сжигания жира, так как это может быть достигнуто путем ходьбы, эта зона была включена, чтобы отрегулировать связь даже с легкими уровнями физической активности, так как любая даже легкая физическая активность увеличит частоту сердечных сокращений.
В то время как участник в основном проводил бы свое время в диапазоне сжигания жира, так как это может быть достигнуто путем ходьбы, эта зона была включена, чтобы отрегулировать связь даже с легкими уровнями физической активности, так как любая даже легкая физическая активность увеличит частоту сердечных сокращений. Кроме того, независимое изучение каждого часа позволило нам зафиксировать нелинейные тенденции RHR во времени. Чтобы дополнить модели, фиксирующие эти почасовые изменения уровня, мы подобрали две дополнительные модели смешанных эффектов для среднего RHR: одна для всего сеанса сна участников, а другая — на следующий день; эти модели предоставили нам широкий обзор ассоциаций.
Кроме того, независимое изучение каждого часа позволило нам зафиксировать нелинейные тенденции RHR во времени. Чтобы дополнить модели, фиксирующие эти почасовые изменения уровня, мы подобрали две дополнительные модели смешанных эффектов для среднего RHR: одна для всего сеанса сна участников, а другая — на следующий день; эти модели предоставили нам широкий обзор ассоциаций.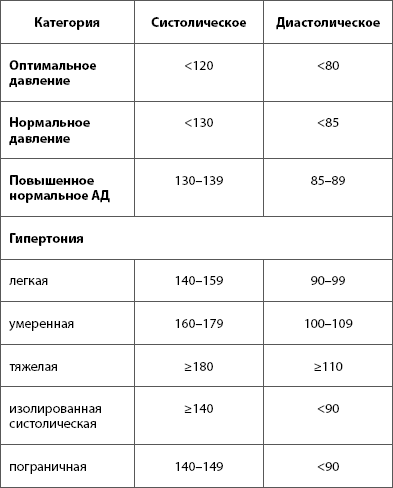 Таким образом, мы расширяем модель смешанных эффектов с повторяющимися измерениями до многоуровневой модели, в которой мы вкладываем наблюдения для каждого абсолютного времени суток под каждого человека. Принимая во внимание изменчивость RHR по каждому часу дня для конкретного человека, мы уменьшаем вероятность обнаружения различий в двух показателях RHR, потому что они просто измерялись в разных точках циркадного ритма человека.После этого мы вкладываем наблюдения внутри отдельных людей, чтобы учесть вариабельность RHR между людьми. В конечном итоге этот подход обеспечивает значительно более надежную оценку несмещенного воздействия каждой ковариаты на относительную частоту сердечных сокращений на основе отклонений времени отхода ко сну.
Таким образом, мы расширяем модель смешанных эффектов с повторяющимися измерениями до многоуровневой модели, в которой мы вкладываем наблюдения для каждого абсолютного времени суток под каждого человека. Принимая во внимание изменчивость RHR по каждому часу дня для конкретного человека, мы уменьшаем вероятность обнаружения различий в двух показателях RHR, потому что они просто измерялись в разных точках циркадного ритма человека.После этого мы вкладываем наблюдения внутри отдельных людей, чтобы учесть вариабельность RHR между людьми. В конечном итоге этот подход обеспечивает значительно более надежную оценку несмещенного воздействия каждой ковариаты на относительную частоту сердечных сокращений на основе отклонений времени отхода ко сну. В случае, если участники пропустили опрос, использовалось вменение прямого / обратного заполнения, позволяющее этим условным значениям наиболее точно отражать истинные баллы участников на данный момент и удовлетворять требованиям модели. Мы подробно описываем каждую из этих переменных ниже.
В случае, если участники пропустили опрос, использовалось вменение прямого / обратного заполнения, позволяющее этим условным значениям наиболее точно отражать истинные баллы участников на данный момент и удовлетворять требованиям модели. Мы подробно описываем каждую из этих переменных ниже.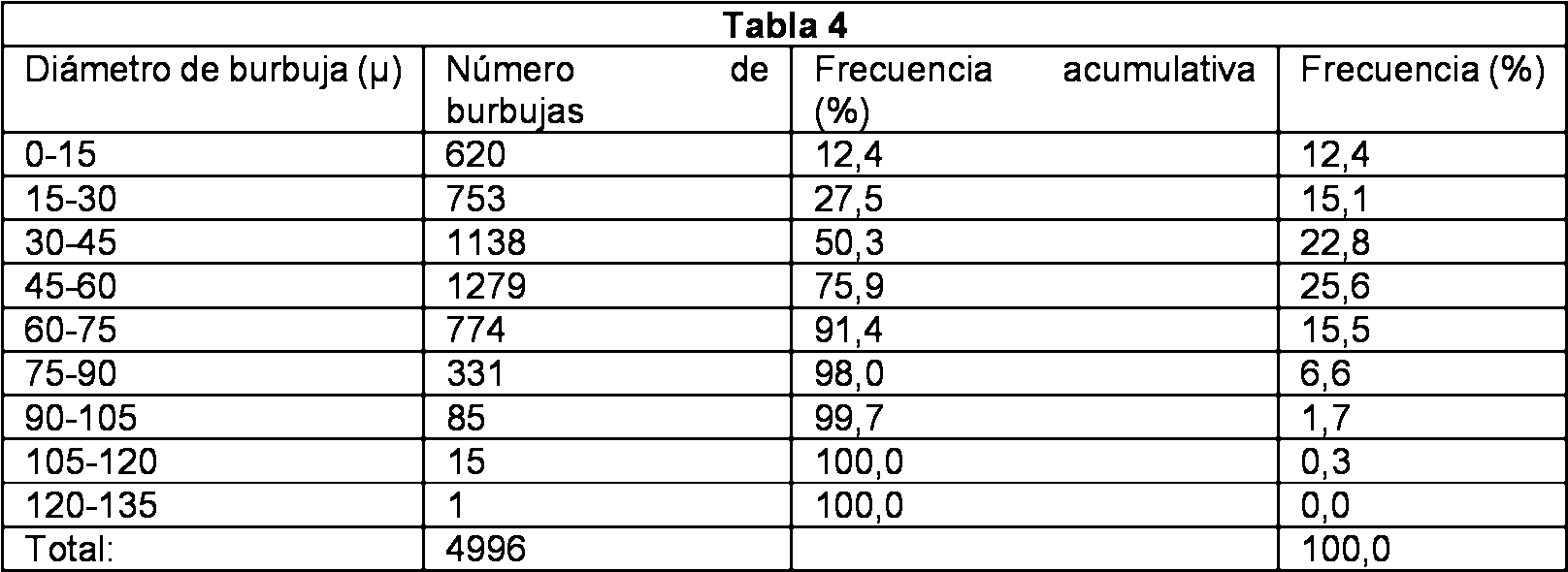
 Мы считаем, что это предположение верно для этой когорты, поскольку выполнение теста хи-квадрат на независимость частот отклонений от времени отхода ко сну, стратифицированных по будним и выходным дням, показывает статистически значимую разницу между распределениями ( P <0,001) для отдельных лиц. ложитесь спать позже, чаще по выходным.
Мы считаем, что это предположение верно для этой когорты, поскольку выполнение теста хи-квадрат на независимость частот отклонений от времени отхода ко сну, стратифицированных по будним и выходным дням, показывает статистически значимую разницу между распределениями ( P <0,001) для отдельных лиц. ложитесь спать позже, чаще по выходным. Любое отклонение от этого времени является ненормальным сердечным ритмом, также известным как аритмия . Есть разные виды аритмий. К ним относятся 1 :
Любое отклонение от этого времени является ненормальным сердечным ритмом, также известным как аритмия . Есть разные виды аритмий. К ним относятся 1 :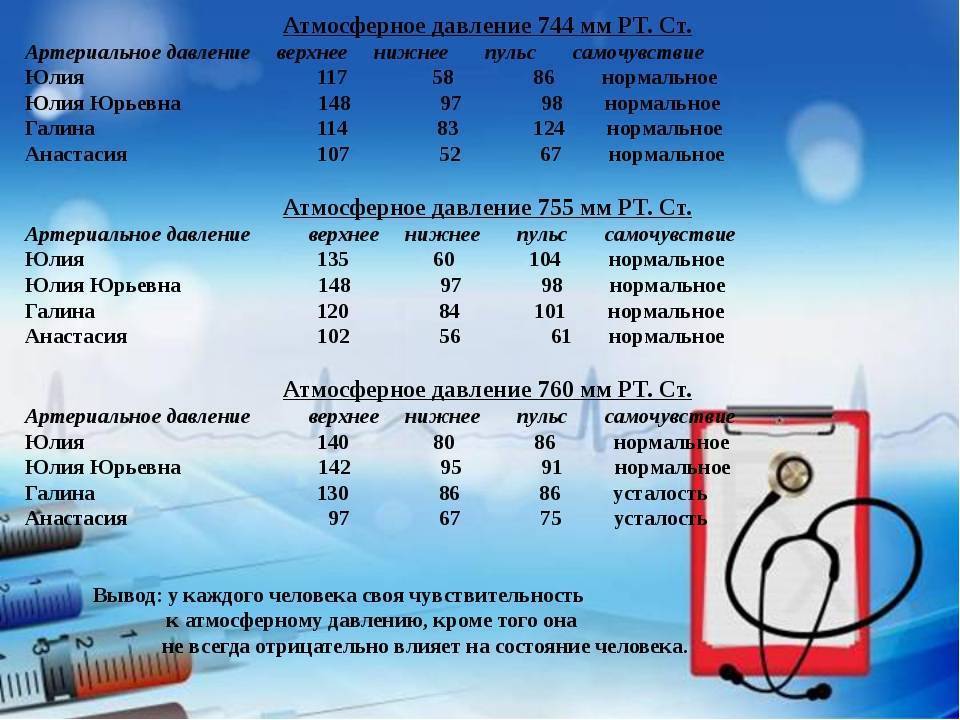 2 Нормальный процесс сердцебиения включает действие синоатриального (СА) узла, который запускает первый электрический импульс, заставляющий сокращаться две верхние камеры сердца (предсердия). 2
2 Нормальный процесс сердцебиения включает действие синоатриального (СА) узла, который запускает первый электрический импульс, заставляющий сокращаться две верхние камеры сердца (предсердия). 2  1
1  Частота сердечных сокращений обычно соответственно увеличивается при физической активности (например, при прыжках с ног в офисе) с последующим быстрым возвращением к исходному уровню во время восстановления.На противоположном конце спектра синусовая брадикардия не редкость у пожилых людей. В этом случае это может представлять дегенеративные изменения проводящей системы. Эта дегенерация может быть прогрессирующей и в тяжелой форме может потребовать имплантации кардиостимулятора. Синусовая брадикардия также может быть признаком повышенного тонуса блуждающего нерва (например, при повышенном внутричерепном давлении), побочным эффектом многих распространенных лекарств (бета-адреноблокаторы, дигоксин, литий и т. Д.) Или обнаружением у пациентов с гипотиреозом.Двумя наиболее важными сердечными причинами синусовой брадикардии являются инфаркт миокарда и первичные заболевания синусового узла (синдром слабости синусового узла) (John and Kumar, 2016). Хотя последнее встречается редко, первое требует пристального внимания, и пациента следует обследовать на предмет других результатов, предполагающих ишемию миокарда (например, боль в груди, потоотделение, гипотензию, впервые возникшую блокаду левой ножки пучка Гиса).
Частота сердечных сокращений обычно соответственно увеличивается при физической активности (например, при прыжках с ног в офисе) с последующим быстрым возвращением к исходному уровню во время восстановления.На противоположном конце спектра синусовая брадикардия не редкость у пожилых людей. В этом случае это может представлять дегенеративные изменения проводящей системы. Эта дегенерация может быть прогрессирующей и в тяжелой форме может потребовать имплантации кардиостимулятора. Синусовая брадикардия также может быть признаком повышенного тонуса блуждающего нерва (например, при повышенном внутричерепном давлении), побочным эффектом многих распространенных лекарств (бета-адреноблокаторы, дигоксин, литий и т. Д.) Или обнаружением у пациентов с гипотиреозом.Двумя наиболее важными сердечными причинами синусовой брадикардии являются инфаркт миокарда и первичные заболевания синусового узла (синдром слабости синусового узла) (John and Kumar, 2016). Хотя последнее встречается редко, первое требует пристального внимания, и пациента следует обследовать на предмет других результатов, предполагающих ишемию миокарда (например, боль в груди, потоотделение, гипотензию, впервые возникшую блокаду левой ножки пучка Гиса).
 Благодаря технологиям носимых датчиков теперь можно непрерывно измерять частоту сердечных сокращений, что позволяет точно определять «нормальную» частоту сердечных сокращений человека и потенциально важные изменения в ней с течением времени.Наша цель — описать межличностную и внутриличностную изменчивость частоты пульса в состоянии покоя (ЧСС), полученную в течение двух лет с помощью носимого устройства, изучая вариации частоты пульса в состоянии покоя в зависимости от времени года, а также отдельных лиц. такие характеристики, как возраст, пол, средняя продолжительность сна и индекс массы тела (ИМТ).
Благодаря технологиям носимых датчиков теперь можно непрерывно измерять частоту сердечных сокращений, что позволяет точно определять «нормальную» частоту сердечных сокращений человека и потенциально важные изменения в ней с течением времени.Наша цель — описать межличностную и внутриличностную изменчивость частоты пульса в состоянии покоя (ЧСС), полученную в течение двух лет с помощью носимого устройства, изучая вариации частоты пульса в состоянии покоя в зависимости от времени года, а также отдельных лиц. такие характеристики, как возраст, пол, средняя продолжительность сна и индекс массы тела (ИМТ). Индивидуальная дневная RHR была доступна в среднем для 320 дней, что дает почти 33 миллиона дневных значений RHR. Мы также исследовали диапазон суточной вариабельности RHR между людьми, а также долгосрочные и краткосрочные изменения траектории ежедневной RHR человека.
Индивидуальная дневная RHR была доступна в среднем для 320 дней, что дает почти 33 миллиона дневных значений RHR. Мы также исследовали диапазон суточной вариабельности RHR между людьми, а также долгосрочные и краткосрочные изменения траектории ежедневной RHR человека.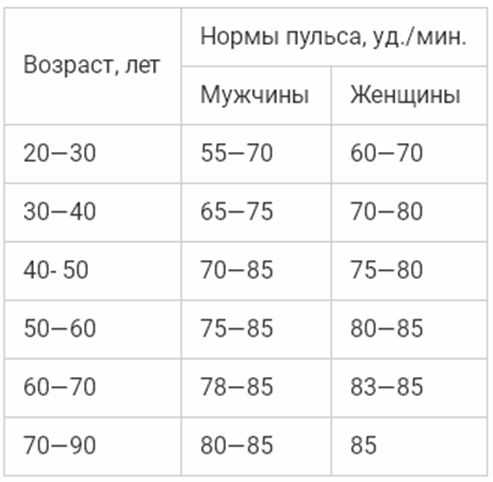 У индивидуумов RHR был намного более постоянным с течением времени с небольшим, но значимым сезонным трендом и обнаруживаемыми дискретными и редкими эпизодами, выходящими за рамки их норм.
У индивидуумов RHR был намного более постоянным с течением времени с небольшим, но значимым сезонным трендом и обнаруживаемыми дискретными и редкими эпизодами, выходящими за рамки их норм.
 Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи. В этом же исследовании значительное изменение RHR через 3 года наблюдения было связано с более высоким риском сердечно-сосудистых заболеваний.Таким образом, одно измерение частоты пульса дает очень мало полезной информации о текущем состоянии здоровья человека, если только оно не выходит за пределы ожидаемого диапазона нормы. Лонгитюдные, индивидуальные данные могут быть более ценными, поскольку несколько исследований изменений дискретных измерений сердечного ритма в течение длительных периодов времени обнаружили связь с сердечно-сосудистыми исходами [13–16]. Подробный анализ индивидуальных изменений в сердечной деятельности может предоставить полезную информацию, которая поможет уточнить существующие фенотипы здоровья и болезни, а в сочетании с другими стандартными или расширенными клиническими тестами может выявить заболевания на самых ранних стадиях [17–19].
В этом же исследовании значительное изменение RHR через 3 года наблюдения было связано с более высоким риском сердечно-сосудистых заболеваний.Таким образом, одно измерение частоты пульса дает очень мало полезной информации о текущем состоянии здоровья человека, если только оно не выходит за пределы ожидаемого диапазона нормы. Лонгитюдные, индивидуальные данные могут быть более ценными, поскольку несколько исследований изменений дискретных измерений сердечного ритма в течение длительных периодов времени обнаружили связь с сердечно-сосудистыми исходами [13–16]. Подробный анализ индивидуальных изменений в сердечной деятельности может предоставить полезную информацию, которая поможет уточнить существующие фенотипы здоровья и болезни, а в сочетании с другими стандартными или расширенными клиническими тестами может выявить заболевания на самых ранних стадиях [17–19]. Их точность в настоящее время аналогична стандартной электрокардиографии (ЭКГ), особенно в покое [20–22]. Повсеместное распространение этих датчиков дает уникальную возможность лучше понять, как RHR изменяется с течением времени для людей и между людьми в течение дней, недель, лет и, в конечном итоге, продолжительности жизни.
Их точность в настоящее время аналогична стандартной электрокардиографии (ЭКГ), особенно в покое [20–22]. Повсеместное распространение этих датчиков дает уникальную возможность лучше понять, как RHR изменяется с течением времени для людей и между людьми в течение дней, недель, лет и, в конечном итоге, продолжительности жизни.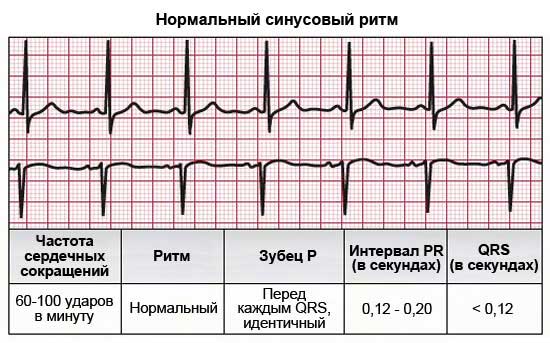 Затем мы исключили пользователей, которые не указали свой пол, чей возраст был младше 18 лет или старше 100 лет, и чей ИМТ был вне диапазона 15–50 кг / м 2 (рассчитано на основе самооценки роста и вес), предполагая, что последние более вероятно ошибочны.Кроме того, мы учитывали только измерения RHR в те дни, когда устройство носили не менее 20 часов, при этом время ношения на запястье определялось устройством на основе собранных данных. Это помогло гарантировать, что RHR рассчитывалась одинаково для всех людей во все дни. Популяция окончательного анализа включала 92 457 человек, которым проводилось как минимум два дня измерения RHR в неделю в течение как минимум 35 недель. Эффекты критериев отбора вместе с демографическими характеристиками людей в наших наборах данных (с точки зрения пола, возраста и категорий ИМТ) описаны на рисунке 1.
Затем мы исключили пользователей, которые не указали свой пол, чей возраст был младше 18 лет или старше 100 лет, и чей ИМТ был вне диапазона 15–50 кг / м 2 (рассчитано на основе самооценки роста и вес), предполагая, что последние более вероятно ошибочны.Кроме того, мы учитывали только измерения RHR в те дни, когда устройство носили не менее 20 часов, при этом время ношения на запястье определялось устройством на основе собранных данных. Это помогло гарантировать, что RHR рассчитывалась одинаково для всех людей во все дни. Популяция окончательного анализа включала 92 457 человек, которым проводилось как минимум два дня измерения RHR в неделю в течение как минимум 35 недель. Эффекты критериев отбора вместе с демографическими характеристиками людей в наших наборах данных (с точки зрения пола, возраста и категорий ИМТ) описаны на рисунке 1. Затем мы удалили пользователей, которые не использовали по крайней мере 2 дня в неделю, с устройством, которое носили 20 или более часов в день, в течение как минимум 35 недель. Показаны демографические и клинические данные полученной когорты, разделенные по полу.
Затем мы удалили пользователей, которые не использовали по крайней мере 2 дня в неделю, с устройством, которое носили 20 или более часов в день, в течение как минимум 35 недель. Показаны демографические и клинические данные полученной когорты, разделенные по полу. RHR рассчитывалась по запатентованной формуле от Fitbit, которая предоставляет каждому человеку одно значение каждый день. Ожидается, что это значение будет репрезентативным для истинного значения RHR, которое может быть получено в положении лежа на спине сразу после пробуждения, но перед тем, как встать с постели.Значение RHR, сообщаемое устройствами, использованными в этом исследовании, согласуется с данными электрокардиограммы потребителя на грудной клетке [25, 26]. В другом исследовании было показано, что определение частоты сердечных сокращений с помощью запястного устройства имеет ошибку <5% для ряда устройств и видов деятельности по сравнению с золотым стандартом и ближе к 1% в состоянии покоя [21]. Чтобы определить значимость любых различий в средней RHR между группами на основе возраста, ИМТ и часов сна, мы использовали тест Велча T для сравнения средних значений двух независимых выборок.
RHR рассчитывалась по запатентованной формуле от Fitbit, которая предоставляет каждому человеку одно значение каждый день. Ожидается, что это значение будет репрезентативным для истинного значения RHR, которое может быть получено в положении лежа на спине сразу после пробуждения, но перед тем, как встать с постели.Значение RHR, сообщаемое устройствами, использованными в этом исследовании, согласуется с данными электрокардиограммы потребителя на грудной клетке [25, 26]. В другом исследовании было показано, что определение частоты сердечных сокращений с помощью запястного устройства имеет ошибку <5% для ряда устройств и видов деятельности по сравнению с золотым стандартом и ближе к 1% в состоянии покоя [21]. Чтобы определить значимость любых различий в средней RHR между группами на основе возраста, ИМТ и часов сна, мы использовали тест Велча T для сравнения средних значений двух независимых выборок. В частности, поскольку связь между независимыми переменными (возраст, ИМТ и количество часов сна) и зависимой переменной (средняя RHR) не является линейной (как показано в результатах), мы решили рассматривать каждую независимую переменную как категориальную переменную. . Для каждой независимой переменной (возраста, ИМТ и сна) мы разделили популяцию на n = 15 групп на основе процентилей (например,g., первая группа включает всех лиц, у которых независимая переменная меньше или равна перцентилю 100 / n). Затем мы вычислили среднее значение зависимой переменной (RHR) среди всех лиц в каждой группе, и мы сохранили это значение в качестве лучшего предиктора среднего RHR для лиц в этой группе. Эти значения (по одному на группу) затем использовали для расчета суммы квадратов остатков (расстояния между прогнозируемой RHR и средней RHR для одного человека). Наконец, коэффициент детерминации равен единице минус общая сумма квадратов расстояния между прогнозируемым значением RHR и средним RHR для всех людей.
В частности, поскольку связь между независимыми переменными (возраст, ИМТ и количество часов сна) и зависимой переменной (средняя RHR) не является линейной (как показано в результатах), мы решили рассматривать каждую независимую переменную как категориальную переменную. . Для каждой независимой переменной (возраста, ИМТ и сна) мы разделили популяцию на n = 15 групп на основе процентилей (например,g., первая группа включает всех лиц, у которых независимая переменная меньше или равна перцентилю 100 / n). Затем мы вычислили среднее значение зависимой переменной (RHR) среди всех лиц в каждой группе, и мы сохранили это значение в качестве лучшего предиктора среднего RHR для лиц в этой группе. Эти значения (по одному на группу) затем использовали для расчета суммы квадратов остатков (расстояния между прогнозируемой RHR и средней RHR для одного человека). Наконец, коэффициент детерминации равен единице минус общая сумма квадратов расстояния между прогнозируемым значением RHR и средним RHR для всех людей.
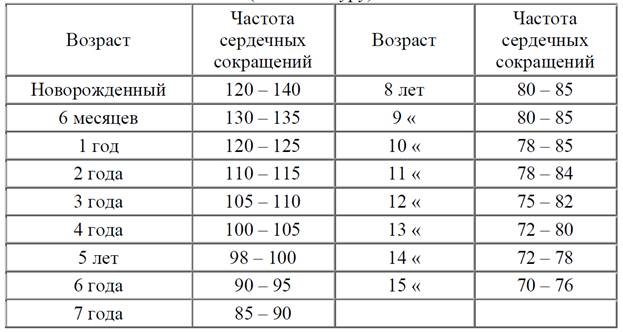 Аналогичным образом, ожидаемые изменения за неделю были рассчитаны путем вычисления Δ i w для всех недель с минимум четырьмя измерениями. Затем для каждого человека мы рассчитали ожидаемый диапазон за все доступные недели: Δ i (exp) = медиана w Δ i w .
Аналогичным образом, ожидаемые изменения за неделю были рассчитаны путем вычисления Δ i w для всех недель с минимум четырьмя измерениями. Затем для каждого человека мы рассчитали ожидаемый диапазон за все доступные недели: Δ i (exp) = медиана w Δ i w .