повышение соэ в крови у мужчин
повышение соэ в крови у мужчинповышение соэ в крови у мужчин
>>>ПЕРЕЙТИ НА ОФИЦИАЛЬНЫЙ САЙТ >>>Что такое повышение соэ в крови у мужчин?
Достичь перечисленных результатов с препаратом Биоманикс можно за 3 недели. Лекарство действует быстро, и устраняет мужские проблемы без побочных эффектов. Капсулы Биоманикс оказывают стимулирующее воздействие, благодаря технологии расширения. Активные компоненты проникают к половому члену, стимулируя практически мгновенную эрекцию.
Эффект от применения повышение соэ в крови у мужчин
Купил на пробу Biomanix, не расчитывал на эффект по увеличению прибора. Но таковой имеется. Жена сразу заметила, что в стоячем состоянии он стал ГОРАЗДО больше чем прежде.
Мнение специалиста
Пользуюсь периодически Biomanix. Капсулы абсолютно безвредны плюс натуральный состав.
Как заказать
Для того чтобы оформить заказ повышение соэ в крови у мужчин необходимо оставить свои контактные данные на сайте. В течение 15 минут оператор свяжется с вами. Уточнит у вас все детали и мы отправим ваш заказ. Через 3-10 дней вы получите посылку и оплатите её при получении.
Отзывы покупателей:
Алена
Препарат Biomanix прекрасно решил мои проблемы с сексуальной жизнью. Стрессы, тяжелая работа, сумасшедший ритм — все это не оставляло ни времени , ни желания на супружеский долг. Жена приобрела эти капсулы, и все преобразилось очень быстро — буквально за три недели. Теперь у нас яркая, насыщенная половая жизнь, да и с потенцией проблем уже почти нет … Мы оба очень довольны!
Ия
Biomanix — мощные капсулы для усиления потенции, которые были созданы в Америке и прошли много клинических испытаний. Средство улучшает обмен веществ, значительно повышает выработку тестостерона, пробуждает сексуальное желание и устраняет усталость после рабочего дня.
Средство улучшает обмен веществ, значительно повышает выработку тестостерона, пробуждает сексуальное желание и устраняет усталость после рабочего дня.
Долго с теснялся размеров своего члена. Из-за этого с женщинами никак не ладилось. Увидел рекламу биоманикс — заказал и не прогадал. Размер реально стал больше. Я стал увереннее в себе и теперь не боюсь заманить в постель любую телку! Где купить повышение соэ в крови у мужчин? Пользуюсь периодически Biomanix. Капсулы абсолютно безвредны плюс натуральный состав. Пару раз они меня буквально спасали, когда нужно было быть на высоте. Очень нравится то, что они мгновенного действия. Раньше пробовал другие препараты, но такого восторга они у меня не вызывали. Ну и, конечно же, тот факт что они помогают даже в профилактике венерических заболеваний повышает к ним доверие.
 2 Таблица нормы СОЭ у мужчин по возрасту. СОЭ – скорость оседания эритроцитов, красных кровяных клеток, которые под . Повышенное СОЭ у ребенка: причины. Повышенная соя в крови у ребенка чаще . У ребенка повышение скорости оседания эритроцитов может наблюдаться в случае прорезания зубов, несбалансированном питании, нехватке. Причины повышения СОЭ в мужском организме. Норма скорости оседания эритроцитов может изменяться по . Норма скорости оседания эритроцитов крови у мужчин составляет от 2 до 10 мм/час. С возрастом показатель СОЭ у мужчин может меняться, оставаясь в пределах возрастной нормы. Повышение СОЭ у мужчин: причины. Медицинские наблюдения установили, что превышение нормы обуславливается одним или . Норма СОЭ в крови у мужчин может повышаться, или понижаться. Всевозможные воспалительные процессы в организме способствуют накапливанию в крови таких веществ, которые. Скорость оседания эритроцитов (СОЭ) – неспецифический лабораторный показатель крови, отражающий соотношение фракций белков плазмы.
2 Таблица нормы СОЭ у мужчин по возрасту. СОЭ – скорость оседания эритроцитов, красных кровяных клеток, которые под . Повышенное СОЭ у ребенка: причины. Повышенная соя в крови у ребенка чаще . У ребенка повышение скорости оседания эритроцитов может наблюдаться в случае прорезания зубов, несбалансированном питании, нехватке. Причины повышения СОЭ в мужском организме. Норма скорости оседания эритроцитов может изменяться по . Норма скорости оседания эритроцитов крови у мужчин составляет от 2 до 10 мм/час. С возрастом показатель СОЭ у мужчин может меняться, оставаясь в пределах возрастной нормы. Повышение СОЭ у мужчин: причины. Медицинские наблюдения установили, что превышение нормы обуславливается одним или . Норма СОЭ в крови у мужчин может повышаться, или понижаться. Всевозможные воспалительные процессы в организме способствуют накапливанию в крови таких веществ, которые. Скорость оседания эритроцитов (СОЭ) – неспецифический лабораторный показатель крови, отражающий соотношение фракций белков плазмы.

http://www.tekkoo.net/images/library/povyshenie_gemoglobina_v_krovi_u_muzhchin1420.xml
http://jetts-anc.com/jetts_anc/images/upload/file/dzheneriki_dlia_povysheniia_potentsii_u_muzhchin6432.xml
http://hmondo.com/userData/board/mgnovennoe_povyshenie_potentsii_u_muzhchin7928.xml
http://hycne.com/userfiles/povyshenie_potentsii_u_muzhchin_v_domashnikh8105.xml
Купил на пробу Biomanix, не расчитывал на эффект по увеличению прибора. Но таковой имеется. Жена сразу заметила, что в стоячем состоянии он стал ГОРАЗДО больше чем прежде.
повышение соэ в крови у мужчин
Достичь перечисленных результатов с препаратом Биоманикс можно за 3 недели. Лекарство действует быстро, и устраняет мужские проблемы без побочных эффектов. Капсулы Биоманикс оказывают стимулирующее воздействие, благодаря технологии расширения. Активные компоненты проникают к половому члену, стимулируя практически мгновенную эрекцию.
Как быстро увеличить потенцию в домашних условиях у мужчин с помощью 16 классных методик. Валерий Аверин. . Есть также и другие народные средства для повышения потенции у мужчин. Зерна грецкого ореха измельчить и смешать с медом, взяв ингредиенты в одинаковом количестве. Рекомендации по повышению естественными способами!! Естественный способ повысить потенцию является комплексным и положительно действует на весь организм. Правильное питание Первое что нужно делать – это сбалансировано питаться и насыщать организм полезными веществами. Начать есть. Этот напиток обеспечит быстрое повышение потенции в домашних условиях и позволит чувствовать себя мужчиной в любой ситуации.



Общий и специфический IgE. Болезни и состояния, сопровождающиеся изменением содержания общего IgE Показания к назначению, правила подготовки к сдаче исследования, расшифровка результатов анализа и показатели нормы.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Иммуноглобулин Е (IgE) — класс иммуноглобулинов, обнаруживаемый в норме в незначительных количествах в сыворотке крови и секретах. Впервые IgE был изолирован в 1960-х годах из сывороток больных атопией и множественной миеломой. В 1968 г. ВОЗ выделила IgE как самостоятельный класс иммуноглобулинов. Согласно ВОЗ 1 МЕ/мл (МЕ — международная единица) соответствует 2,4 нг. Обычно концентрация IgE выражается в МЕ/мл или кЕ/л (кЕ — килоединица).
Обычно концентрация IgE выражается в МЕ/мл или кЕ/л (кЕ — килоединица). В норме IgE составляет менее 0,001% от всех иммуноглобулинов сыворотки крови (см. табл.1).
Таблица 1: Содержание IgE в сыворотке крови здоровых людей
| Возрастные группы | IgE (кЕ/л) |
|---|---|
| До 1 года | 0 — 15 |
| 1 год-6 лет | 0 — 60 |
| 6 -10 лет | 0 — 90 |
| 10 -16 лет | 0 — 200 |
| Взрослые | 0 — 100 |
Структура IgE подобна структуре других иммуноглобулинов и состоит из двух тяжёлых и двух лёгких полипептидных цепей. Они сгруппированы в комплексы, называемые доменами. Каждый домен содержит приблизительно 110 аминокислот. IgE имеет пять таких доменов в отличие от IgG, который имеет только четыре домена. По физико-химическим свойствам IgE — гликопротеин с молекулярной массой примерно 190000 дальтон, состоящий на 12% из углеводов. IgE имеет самую короткую продолжительность существования (время полувыведения из сыворотки крови 2 — 3 суток), самую высокую скорость катаболизма и наименьшую скорость синтеза из всех иммуноглобулинов (2,3 мкг/кг в сутки). IgE синтезируется главным образом плазматическими клетками, локализующимися в слизистых оболочках. Основная биологическая роль IgE — уникальная способность связываться с поверхностью тучных клеток и базофилов человека. На поверхности одного базофила присутствует примерно 40000 — 100000 рецепторов, которые связывают от 5000 до 40000 молекул IgE.
Они сгруппированы в комплексы, называемые доменами. Каждый домен содержит приблизительно 110 аминокислот. IgE имеет пять таких доменов в отличие от IgG, который имеет только четыре домена. По физико-химическим свойствам IgE — гликопротеин с молекулярной массой примерно 190000 дальтон, состоящий на 12% из углеводов. IgE имеет самую короткую продолжительность существования (время полувыведения из сыворотки крови 2 — 3 суток), самую высокую скорость катаболизма и наименьшую скорость синтеза из всех иммуноглобулинов (2,3 мкг/кг в сутки). IgE синтезируется главным образом плазматическими клетками, локализующимися в слизистых оболочках. Основная биологическая роль IgE — уникальная способность связываться с поверхностью тучных клеток и базофилов человека. На поверхности одного базофила присутствует примерно 40000 — 100000 рецепторов, которые связывают от 5000 до 40000 молекул IgE.
Дегрануляция тучных клеток и базофилов происходит, когда две связанные с мембраной клеток молекулы IgE соединяются с антигеном, что, в свою очередь, «включает» последовательные события, ведущие к выбросу медиаторов воспаления.
IgE можно обнаружить в организме человека уже на 11-й неделе внутриутробного развития. Содержание IgE в сыворотке крови возрастает постепенно с момента рождения человека до подросткового возраста. В пожилом возрасте уровень IgE может снижаться.
В практике клинико-диагностических лабораторий определение общего и специфического IgE проводится с целью их использования в качестве самостоятельных диагностических показателей. В табл. 2 перечислены основные болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови.
В табл. 2 перечислены основные болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови.Таблица 2: Болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови
| Болезни и состояния | Возможные причины |
| I. Повышенное содержание IgE | |
|---|---|
|
Аллергические болезни, обусловленные IgE антителами: а) Атопические болезни · Аллергический ринит · Атопическая бронхиальная астма · Атопический дерматит · Аллергическая гастроэнтеропатия б) Анафилактические болезни · Системная анафилаксия · Крапивница — ангионевротический отек |
Множественные аллергены: · пыльцевые · пылевые · эпидермальные · пищевые · лекарственные препараты · химические вещества · металлы · чужеродный белок |
| Аллергический бронхопульмональный аспергиллез | Неизвестны |
| Гельминтозы | IgE антитела, связанные с защитным иммунитетом |
| Гипер-IgE синдром (синдром Джоба) | Дефект Т-супрессоров |
| Селективный IgA дефицит | Дефект Т-супрессоров |
| Синдром Вискотт-Олдриджа | Неизвестны |
| Тимусная аплазия (синдром Ди-Джорджи) | Неизвестны |
| IgE — миелома | Неоплазия IgE-продуцирующих плазматических клеток |
| Реакция «трансплантат против хозяина» | Дефект Т-супрессоров |
II. Сниженное содержание общего IgE Сниженное содержание общего IgE
|
|
| Атаксия — телеангиэктазия | Дефекты Т-клеток |
Ниже приведены в качестве примеров диапазоны содержания общего IgE сыворотки крови (у взрослых) при некоторых патологических состояниях (табл. 3). Однако, несмотря на первоначально кажущуюся простоту использования определения общего и специфического IgE для диагностики, существуют некоторые сложности в интерпретации результатов. Их перечень приведён ниже.
Таблица 3: Значения общего IgE при некоторых патологических состояниях
| Патологические состояния | Содержание IgE (кЕ/л) |
|---|---|
| Аллергический ринит | 120 — 1000 кЕ/л |
| Атопическая бронхиальная астма | 120 — 1200 кЕ/л |
| Атопический дерматит | 80 — 14000 кЕ/л |
|
Аллергический бронхолегочный аспергиллез: — ремиссия — обострение |
80 — 1000 кЕ/л 1000 — 8000 кЕ/л |
| Гипер — IgE синдром | 1000 — 14000 кЕ/л |
| IgE — миелома | 15000 кЕ/л и выше |
Особенности интерпретации и диагностические ограничения общего IgE
- Примерно 30% больных атопическими заболеваниями имеют уровень общего IgE в пределах значений нормы.

- Некоторые больные бронхиальной астмой могут иметь повышенную чувствительность только к одному аллергену (антигену), в результате чего общий IgE может быть в пределах нормы, в то время как кожная проба и специфический IgE будут положительными.
- Концентрация общего IgE в сыворотке крови также повышается при неатопических состояниях (особенно при глистной инвазии, некоторых формах иммунодефицитов и бронхопульмональном аспергиллезе) с последующей нормализацией после соответствующего лечения.
- Хроническая рецидивирующая крапивница и ангионевротический отёк не являются обязательными показаниями для определения общего IgE, так как обычно имеют неиммунную природу.
- Границы нормы, определённые для европейцев, не могут быть применены для представителей зон, эндемичных по гельминтозам.
Особенности интерпретации и диагностические ограничения специфического IgE
- Доступность определения специфического IgE не должна преувеличивать его диагностическую роль в обследовании больных с аллергией.

- Обнаружение аллергенспецифического IgE (к какому-либо аллергену или антигену) не доказывает, что именно этот аллерген ответственен за клиническую симптоматику; окончательное заключение и интерпретация лабораторных данных должны быть сделаны только после сопоставления с клинической картиной и данными развёрнутого аллергологического анамнеза.
- Отсутствие специфического IgE в сыворотке периферической крови не исключает возможности участия IgE-зависимого механизма, так как местный синтез IgE и сенсибилизация тучных клеток может происходить и в отсутствие специфического IgE в кровотоке (например, аллергический ринит).
- Антитела других классов, специфичные для данного аллергена, особенно класса IgG (IgG4), могут быть причиной ложноотрицательных результатов.
- Исключительно высокие концентрации общего IgE, например, у отдельных больных атопическим дерматитом, могут за счёт неспецифического связывания с аллергеном давать ложноположительные результаты.

- Идентичные результаты для разных аллергенов не означают их одинакового клинического значения, так как способность к связыванию с IgE у разных аллергенов может быть различной.
Таблица 4: Показания и противопоказания к определению специфического IgE
| Показания | |
|---|---|
| 1 | Дифференциальная диагностика между IgE-зависимым и не-IgE-зависимым механизмами аллергических реакций |
| 2 |
Больные, у которых невозможно выявить аллерген анамнестически, при помощи дневника и т. д. д.
|
| 3 | Больные с недостаточным эффектом специфической гипосенсибилизации, назначенной по результатам кожных проб |
| 4 | Дермографизм и распространённый дерматит |
| 5 | Больные детского и пожилого возраста с гипореактивностью кожи |
| 6 | Гиперреактивность кожи |
| 7 | Больные, которым невозможно отменить симптоматическую терапию препаратами, влияющими на результаты кожных проб |
| 8 | Отрицательное отношение больного к кожным пробам |
| 9 | В анамнезе системные аллергические реакции на кожные пробы |
| 10 | Несоответствие результатов кожных проб данным анамнеза и клинической картине |
| 11 | IgE-зависимая пищевая аллергия |
| 12 | Необходимость количественной оценки чувствительности и специфичности аллергена |
| 13 | Общий IgE сыворотки крови более 100 кЕ/л |
| Обследование нецелесообразно: | |
| 1 | При атопических заболеваниях в случаях удовлетворительных результатов специфической терапии по данным кожных проб |
| 2 | У больных с не-IgE-зависимым механизмом аллергических реакции |
Ссылки по теме: Иммуноглобулин Е, IgE общий (аллергодиагностика), панели аллергенов.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
АСЛ-О в крови повышен, что это значит?
АСЛ-О – это достоверный показатель перенесенного ранее инфекционного заболевания, возбудителем которого являются стрептококки. Анализ на его количество используется для подтверждения недавнего инфицирования стрептококком группы A. В большинстве случаев инфекционное заболевание имеет характерную клиническую картину, поэтому оно легко диагностируется. При своевременной диагностике оно успешно лечится путем приема курса антибактериальных препаратов. Они уничтожают возбудителя и наступает выздоровление. Иногда инфекция имеет атипичное течение. Если она своевременно не лечится или выбран неэффективный в данном случае метод лечения, велик риск развития осложнений. К ним относится гломерулонефрит и ревматическая лихорадка. Анализ крови на АСЛ-О используется, чтобы подтвердить стрептококковую инфекцию, а также для наблюдения хода ее лечения (при выздоровлении показатели снижаются).
К ним относится гломерулонефрит и ревматическая лихорадка. Анализ крови на АСЛ-О используется, чтобы подтвердить стрептококковую инфекцию, а также для наблюдения хода ее лечения (при выздоровлении показатели снижаются).
Показания к исследованию
Анализ назначают в следующих случаях:
- Появление жалоб на здоровье вскоре после перенесенной ангины или поражения кожи, если имеется причина полагать, что причиной их появления является перенесенная стрептококковая инфекция. Обычно тест назначается через 2-3 недели после перенесенного заболевания. Значение теста значительно увеличивается, если он проводится несколько раз с интервалом около 2-х недель. В этом случае динамика результатов дает возможность наиболее достоверно оценить состояние пациента.
- Лечение осложнений стрептококковой инфекции. Анализ назначается врачом через 7-14 дней после начала лечения, чтобы оценить его эффективность и при необходимости откорректировать назначенную ранее терапию.

Интерпретация результатов
Для детей до 14-ти лет референсные значения ниже, чем для пациентов старшего возраста. Выработка АСЛ-О в организме начинается через 7-14 дней после заражения. Через 1-1,5 месяца его концентрация достигает максимального значения. Антитела могут определяться в крови еще некоторое время после выздоровления.
Низкий уровень антител или их отсутствие позволяет с высокой долей вероятности исключить недавнее заражение стрептококками. Для подтверждения анализ может проводиться повторно с интервалом около двух недель. Если результат вновь будет отрицательным, скорее всего инфекция отсутствует. Из этого правила редко, но все же случаются исключения. В редких случаях у пациентов с осложнениями после инфекции уровень АСЛ-О остается в пределах референсных значений.
Превышение нормы в 4 и более раз, а также нарастание показателей указывают на стрептококковую инфекцию, которую пациент перенес недавно. Снижение концентрации антител свидетельствует о выздоровлении. По количеству антител можно судить о том, насколько давно была перенесена инфекция.
По количеству антител можно судить о том, насколько давно была перенесена инфекция.
Только по показателям АСЛ-О невозможно судить о вероятности развития осложнений, а также о возможной степени их тяжести. Результаты теста позволяют подтвердить диагноз у пациентов с симптомами гломерулонефрита или ревматической лихорадки. При интерпретации результатов необходимо учитывать целый ряд факторов. Уровень антител может возрастать у пациентов с реактивным артритом, патологиями печени и гиперхолестеринемией. При приеме ряда антибактериальных лекарственных препаратов, кортикостероидов, а также у пациентов с нефротическим синдромом возможно получение ложноотрицательных результатов. Для диагностики острой инфекции данный тест не используется, так как АСЛ-О выявляется не ранее, чем через 1-2 недели после заражения.
Подготовка к исследованию
Специальная подготовка к сдаче крови из вены для этого теста не требуется. Достаточно полчаса перед сдачей крови спокойно посидеть. В это время необходимо отказаться от курения.
В это время необходимо отказаться от курения.
Причины повышения С-реактивного белка | UBI clinic
С-реактивный белок (СРБ) – элемент крови, который очень чувствительный к хроническим и острым воспалительным процессам. Этот показатель наиболее точно отображает состояние иммунной системы, т.к. повышается за долго до того, как заболевание проявит себя клинически и сохраняется длительное время после перенесенного инфекционного (бактериального или вирусного) заболевания.
Повышается С-реактивный белок при ревматических заболеваниях, сердечно-сосудистой патологии, заболеваниях органов пищеварения, кожи, бронхиальной астме, аутоиммунных, онкологических заболеваниях, вирусных и бактериальных инфекциях. В случае развития инфаркта миокарда, этот показатель одним из первых «сигнализирует» о развитии ишемического воспаления в сосудистой стенке. Определение СРБ является более надежным и чувствительным показателем воспалительного процесса, чем подсчет скорости оседания эритроцитов в крови (СОЭ).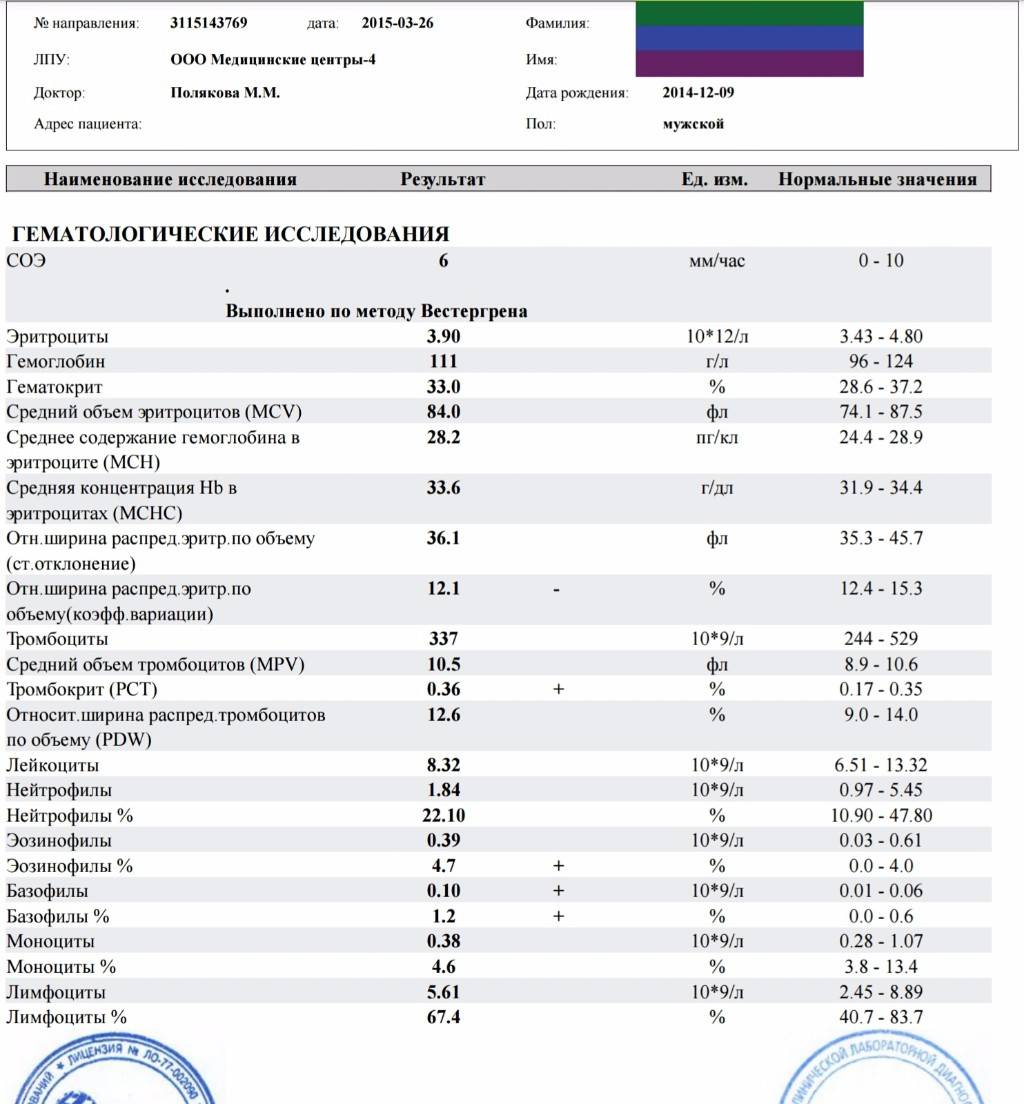
Ранее СРБ примялся в очень узком сегменте. Его определяли качественными реакциями анализа крови в «плюсах» исключительно для выявления активности ревматизма. Однако современная наука глубоко изучила и проиллюстрировала значение С-реактивного белка, как системного показателя состояния иммунной системы, наличия и активности в организме воспалительного процесса. При этом очень важно измерять этот показатель не качественно, а количественно (в миллиграммах на литр). Такое измерение позволит наиболее точно определить, есть ли в организме воспаление, угнетающее иммунную систему.
Норма С-реактивного белка составляет 3 мг/л. Повышение СРБ до 7 мг/л говорит о низкой интенсивности воспаления. Это может наблюдаться при вялотекущих, скрытых воспалительных заболеваниях, не проявляющихся клинически. Такое воспаление наиболее опасно, т.к. приводит к постепенному истощению иммунитета. Показатели СРБ от 7,1 до 50 мг/л – это, так называемая, средняя интенсивность воспалительного процесса.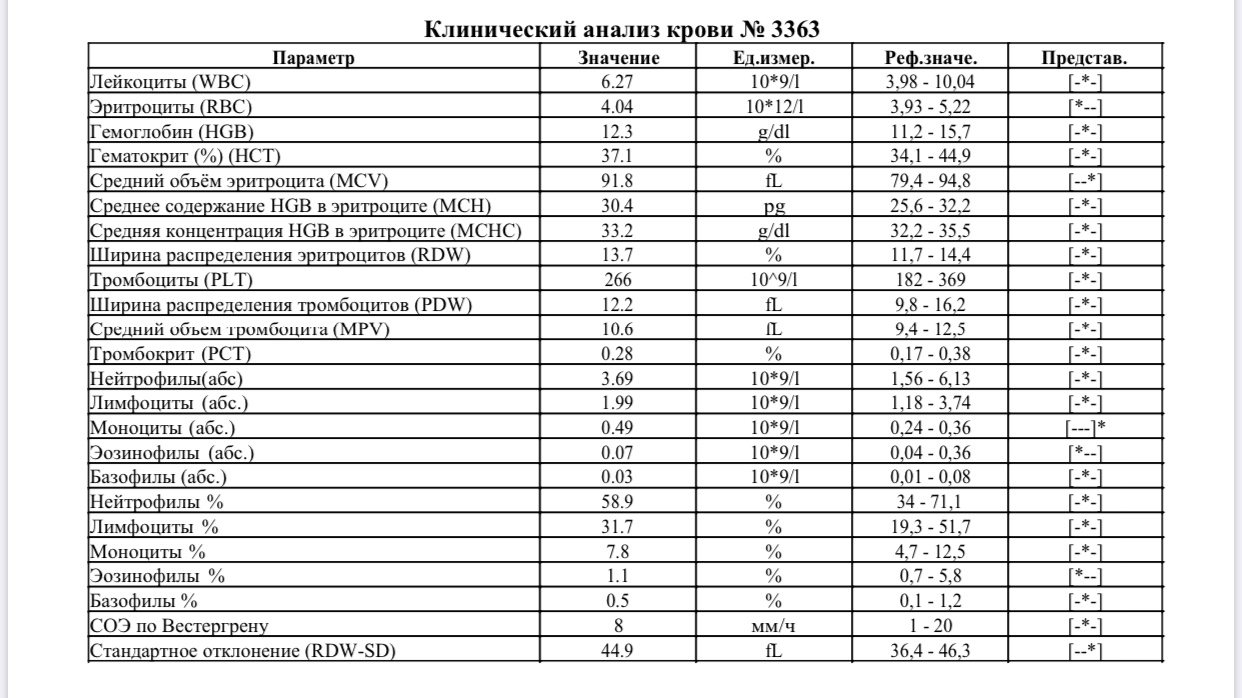 Такой уровень СРБ наблюдается при хронических воспалительных процессах в организме (аутоиммунные, ревматические, кожные, онкологические и пр заболевания). Повышение СРБ выше 50 мг/л говорит о высокой интенсивности воспаления. Как правило, такие показатели СРБ наблюдаются при тяжелом течении воспалительных и аутоиммунных заболеваний. Раннее выявление скрытого воспаления, поможет Вам избежать хронизации процесса и предотвратить развитие осложнений. При повышении СРБ, следует немедленно обратиться к врачу.
Такой уровень СРБ наблюдается при хронических воспалительных процессах в организме (аутоиммунные, ревматические, кожные, онкологические и пр заболевания). Повышение СРБ выше 50 мг/л говорит о высокой интенсивности воспаления. Как правило, такие показатели СРБ наблюдаются при тяжелом течении воспалительных и аутоиммунных заболеваний. Раннее выявление скрытого воспаления, поможет Вам избежать хронизации процесса и предотвратить развитие осложнений. При повышении СРБ, следует немедленно обратиться к врачу.
Удар по лимфоцитам: COVID вызывает длительные сбои работы иммунитета | Статьи
Ученые из КНР предупреждают: многие переболевшие коронавирусом пациенты могут столкнуться с проблемами восстановления иммунитета. У части из них наблюдается снижение уровня лимфоцитов в крови, число которых не достигает нормы даже через 11 недель после выздоровления. Хроническое повреждение этих иммунных клеток чаще всего вызывает ВИЧ. Однако российские специалисты говорят, что, в отличие от вируса иммунодефицита человека, SARS-CoV-2 не способен размножаться в лимфоцитах. Поэтому описанные нарушения работы защитной системы организма могут носить длительный, но не перманентный характер.
Поэтому описанные нарушения работы защитной системы организма могут носить длительный, но не перманентный характер.
Атака на защитников
Ученые из Института вирусологии Уханя опубликовали препринт научной статьи, в которой говорится о проведенном исследовании воздействия коронавируса на лимфоциты, — клетки крови, отвечающие за иммунитет.
Как сказано в аннотации к препринту, лимфопения (временное или стойкое снижение уровня лимфоцитов в крови. — «Известия») является типичным симптомом у пациентов с COVID-19. Ученые изучили состояние 55 выздоровевших от коронавирусной инфекции людей, чтобы узнать, как меняется со временем количество иммунных клеток в их крови.
Фото: REUTERS/Manuel Claure
«У пациентов с COVID-19 всё еще наблюдались значительные фенотипические изменения в лимфоцитах после клинического выздоровления через 4–11 недель. Это говорит о том, что инфекция SARS-CoV-2 глубоко влияет на лимфоциты и приводит к длительным потенциальным дисфункциям», — сказано в тексте.
Причем пациенты не показали даже тенденции к восстановлению числа лимфоцитов в течение всего периода наблюдения. Российские ученые подтверждают, что стойкое снижение уровня лимфоцитов в крови может быть следствием перенесенного вирусного заболевания. Однако механизмы, вызывающие потерю отдельных популяций иммунных клеток, пока еще хорошо не изучены, сообщил «Известиям» младший научный сотрудник лаборатории экспериментальной хирургии и онкологии Курского государственного медицинского университета Давид Наимзада.
— Известно, что их перманентная потеря может вызываться не только хроническими инфекциями, — пояснил ученый.
Бойцы невидимого фронта
Сама по себе лимфопения встречается при различных патологических состояниях: вследствие длительной вирусной инфекции, иммунодефицита, патологий костного мозга и т.д. Наиболее частым инфекционным заболеванием, вызывающим снижение лимфоцитов, является СПИД, при котором разрушаются пораженные ВИЧ CD4 Т-клетки (CD4 расшифровываются как cluster of differentiation, — это особая группа Т-клеток, а именно Т-хелперов, которые помогают другим клеткам уничтожать инфицирующие организмы). Однако в этом случае повреждения иммунной системы носят хронический характер.
Однако в этом случае повреждения иммунной системы носят хронический характер.
Фото: ИЗВЕСТИЯ/Павел Бедняков
В случае же с коронавирусом речь идет о хоть и длительной, но обратимой дисфункции иммунитета. Когда человек заражается новым патогеном, в его организме происходит экспансия лимфоцитов. Это своего рода солдаты, которые должны бороться с вредоносным вирусом, пояснил «Известиям» руководитель лаборатории геномной инженерии МФТИ (вуз— участник проекта «5-100») Павел Волчков.
— А после инфекции в организме происходит «демобилизация», так как такое количество активированных Т-клеток и В-клеток уже не нужно, подчеркнул эксперт. — После активации иммунные клетки живут недолго, а затем исчезают либо становятся «клетками памяти». Это мы и называем иммунитетом. Система так устроена, что во время отправки солдат-лимфоцитов «в запас» могут обнаруживаться небольшие колебания в их количестве. Но потом провал будет восстановлен новыми клетками.
Иммунная дисфункция
О том, что коронавирус способен поражать клетки иммунитета, ранее сообщали китайские ученые из Фуданьского университета. В апреле этого года в ведущем мировом научном журнале Nature была опубликована их работа, в которой утверждалось, что в лабораторных условиях SARS-Cov-2 способен заражать Т-лимфоциты. Однако позже статья была отозвана самими авторами — выяснилось, что им следовало использовать первичные Т-клетки вместо лабораторных линий для достоверного результата.
— В данной статье было написано, что некоторые коронавирусы, например MERS (ближневосточный респираторный синдром), способны вызывать гибель клеток иммунной системы, запуская определённый каскад биохимических реакций, — рассказал «Известиям» заместитель директора по научной работе ИФХЭ РАН Олег Батищев. — Для SARS-Cov-2 четких подтверждений такой возможности пока не обнаружено. Ни один из коронавирусов в отличие от ВИЧ не может размножаться в иммунных клетках.
Фото: ИЗВЕСТИЯ/Сергей Коньков
Как подчеркнул эксперт, MERS приводил к более высокой смертности, чем COVID-19, отчасти из-за угнетения иммунного ответа.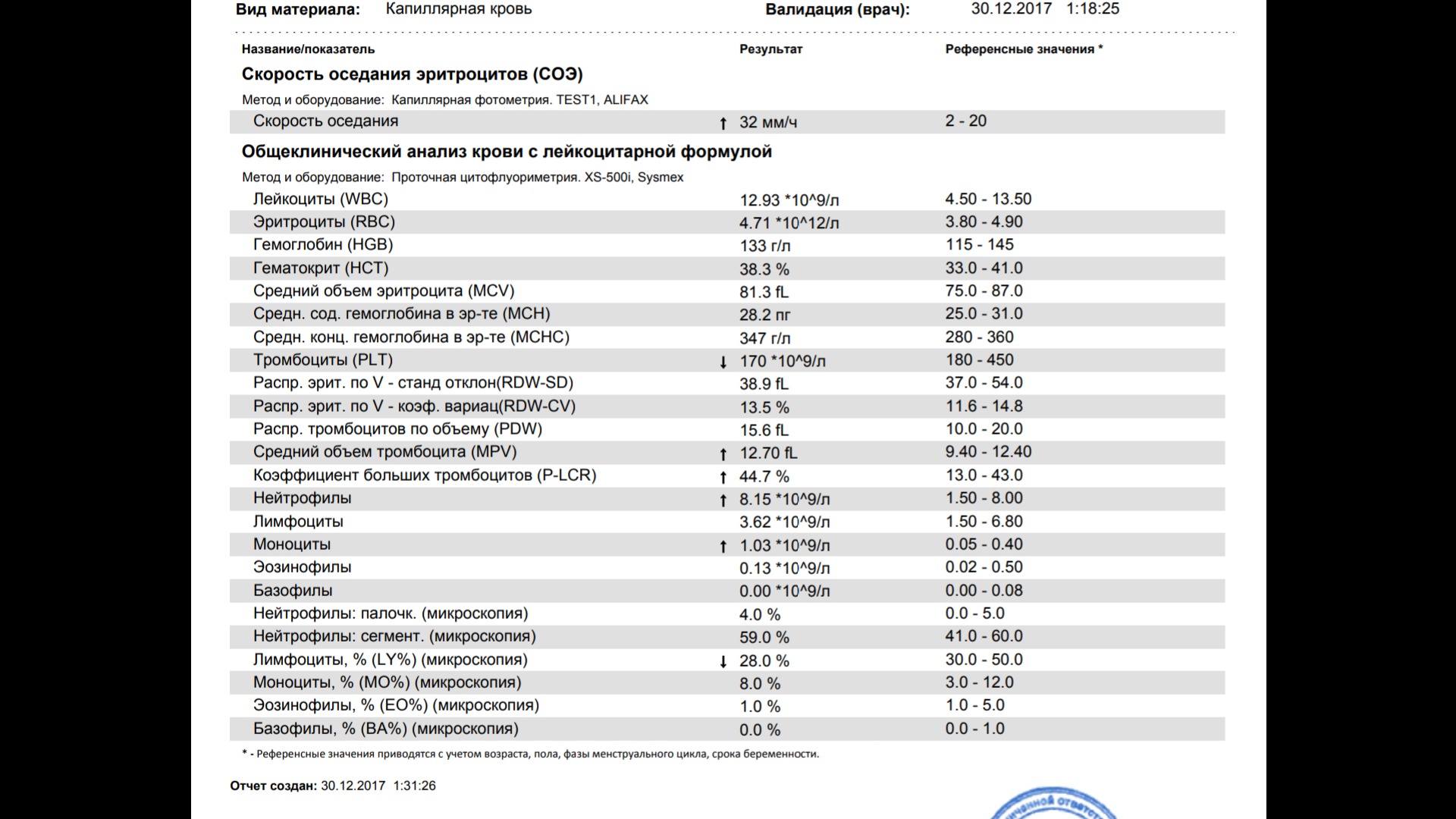
— Лимфоциты поражают ВИЧ, вирусы герпеса и некоторые другие вирусы, — сообщил «Известиям» заведующий лабораторией биотехнологии и вирусологии Новосибирского государственного университета Сергей Нетесов. — Из-за этого иммунный ответ на инфекцию может замедляться или быть неполноценным.
Что касается коронавируса, то сейчас главное — это тщательное изучение инфекционного процесса в организме пациентов, что даст наиболее важные данные о выработке полноценного иммунного ответа или сложностях в этом процессе, считает эксперт.
Не путать с ВИЧ
Некоторые специалисты уже сравнивали коронавирус нового типа с ВИЧ и даже говорили об их сходстве. В частности, лауреат Нобелевской премии 2008 года, французский вирусолог Люк Монтанье заявлял о лабораторном происхождении COVID-19 и о том, что его геном содержит в себе элементы ВИЧ. Однако позже эти идеи подверглись жесткой критике со стороны научного сообщества.
— При ВИЧ-инфекции поражаются клетки иммунной системы. Причем их инфицирование является основным способом репликации вируса иммунодефицита человека, — сказала «Известиям» сотрудник научно-клинического отдела МГЦ СПИД и Международного центра вирусологии РУДН Елена Белова.
Причем их инфицирование является основным способом репликации вируса иммунодефицита человека, — сказала «Известиям» сотрудник научно-клинического отдела МГЦ СПИД и Международного центра вирусологии РУДН Елена Белова.
Для коронавируса такая возможность не доказана. Поэтому COVID-19 и ВИЧ — это принципиально разные патогены.
Фото: ИЗВЕСТИЯ/Сергей Коньков
— COVID-19 — это вирус, вызывающий острую, а значит, краткосрочную инфекцию, — пояснил Павел Волчков. — На сегодняшний день нет ни одного случая коронавируса, который бы перешел из острой фазы в хроническую, то есть стал жить в организме человека. Данный патоген поражает фактически все органы и ткани, в силу того что рецепторы на поверхности клеток, за которые он цепляется, находятся практически на всех типах тканей. По этой причине он теоретически может инфицировать и клетки иммунной системы, что действительно может вызывать их гибель.
ВИЧ — это вирус, вызывающий хроническую инфекцию именно иммунной системы, никаких других тканей он не поражает. Говоря точнее, вирус инфицирует и живет исключительно в CD4 T-клетках, рассказал эксперт.
Говоря точнее, вирус инфицирует и живет исключительно в CD4 T-клетках, рассказал эксперт.
Что касается препринта ученых из Уханя, то они в выводах к своей статье проводят параллель со СПИДом и гепатитом С. Также исследователи утверждают, что им еще предстоит выяснить, как долго будут длиться фенотипические изменения и потенциальные дисфункции лимфоцитов у выздоровевших пациентов.
Городская клиническая больница №31 — Пациентам в помощь. Гематологические заболевания. Часть IV. Болезни плазматических клеток (страница 2)
Страница 2 из 7
Множественная миелома
Множественная миелома – болезнь зрелых В-клеток, которая проявляется разрушением и болями в костях, ухудшением работы почек, изменением состава крови.
Словом «миелома» на медицинском языке называется опухоль из клеток костного мозга, а «множественная» показывает, что опухоль состоит из множества клеток, которые рассеяны по организму.
Множественная миелома – одна из самых распространенных болезней, которые лечат врачи-гематологи. При этой болезни изменяются плазматические клетки, клетки-инженеры, которые в здоровом состоянии вырабатывают жидкую часть иммунитета – иммуноглобулины. При миеломе плазматических клеток становится очень много, и они вырабатывают не только полезные белки, но и ненужный белок — парапротеин. Организм пытается вывести его через почки. Если в начале болезни это удается, то по мере развития болезни парапротеин все более повреждает почки. Вместе с тем при миеломе начинают разрушаться кости. Они становятся хрупкими, и у пациентов могут быть даже самопроизвольные, то есть без внешних причин, переломы костей: позвонков, ребер и других.
При этой болезни изменяются плазматические клетки, клетки-инженеры, которые в здоровом состоянии вырабатывают жидкую часть иммунитета – иммуноглобулины. При миеломе плазматических клеток становится очень много, и они вырабатывают не только полезные белки, но и ненужный белок — парапротеин. Организм пытается вывести его через почки. Если в начале болезни это удается, то по мере развития болезни парапротеин все более повреждает почки. Вместе с тем при миеломе начинают разрушаться кости. Они становятся хрупкими, и у пациентов могут быть даже самопроизвольные, то есть без внешних причин, переломы костей: позвонков, ребер и других.
Обычно проходит много времени от появления жалоб до постановки диагноза, так как множественная миелома развивается очень медленно, недаром это болезнь пожилых людей. Говорят, что если бы люди жили более 100 лет, то от миеломной болезни страдали бы около половины старых людей. Пациентов часто беспокоят боли в спине, ребрах, но поскольку средний возраст пациента с миеломой превышает 70 лет, то эти жалобы часто относят на счет остеохондроза, возраста и других причин. Болезнь можно заподозрить, если выполнить анализ крови, в котором на ранних стадиях обнаруживают повышенную скорость оседания эритроцитов (СОЭ), а на поздних стадиях болезни видят снижение гемоглобина, признаки нарушения работы почек. Иногда ускорение СОЭ и парапротеин находят во время профессиональных осмотров задолго до появления болей в костях.
Болезнь можно заподозрить, если выполнить анализ крови, в котором на ранних стадиях обнаруживают повышенную скорость оседания эритроцитов (СОЭ), а на поздних стадиях болезни видят снижение гемоглобина, признаки нарушения работы почек. Иногда ускорение СОЭ и парапротеин находят во время профессиональных осмотров задолго до появления болей в костях.
Диагноз
Чтобы поставить диагноз «множественная миелома», необходимо взять анализ костного мозга для цитологического, гистологического и иммуногистохимического исследования. Обязательно также установить количество и вид произведенного ненужного белка, а для этого исследовать белок в крови и моче, куда он часто попадает из-за плохой работы почек. Очень важно провести рентгеновский осмотр костей скелета, чтобы понять, какие и насколько сильно повреждены кости. Стадию болезни устанавливают по системе Salmon и Durie, в которой применяют цифры и буквы. Общую величину опухолей обозначают цифрами от I до III; буква «А» показывает, что почки в норме, а буква «Б» – что почки уже поражены болезнью.
Лечение
Если болезнь выявлена случайно, протекает медленно и бессимптомно (стадия IA), то есть не причиняет боли, нет больших изменений в крови и костях, почки работают нормально, в этом случае лечение можно отложить. Пациенты сдают время от времени контрольные анализы крови и приходят на прием к гематологу. Только тогда, когда появляются тревожные признаки болезни, врач-гематолог решает начать лечение. Поводом к началу лечения является появление симптомов: болей, признаков разрушения костной ткани, нарушения работы почек и других органов.
В лечении пациента с множественной миеломой есть два главных подхода. Если пациент достаточно молод и здоров, то можно провести лечение большими дозами химиопрепаратов, которые впоследствии позволяют на годы забыть о болезни. В других случаях используют маленькие, но достаточные дозы лекарств, которые позволяют затормозить развитие болезни, значительно уменьшить боли, предотвратить разрушение костей и улучшить самочувствие пациента. Средний срок жизни пациентов от момента постановки диагноза может достигать 10 лет. В целом применение современных способов лечения позволяет успешно лечить до 95% пациентов.
Средний срок жизни пациентов от момента постановки диагноза может достигать 10 лет. В целом применение современных способов лечения позволяет успешно лечить до 95% пациентов.
Краткий справочник по ревматизму — Venäjän kielinen reuma-aapinen
Краткий справочник по ревматизму
на русском языке
перевод сведений о ревматических заболеваниях сделан со страницы:
Suomen Reumaliitto Ry
http://www.reumaliitto.fi/reuma-aapinen/reumataudit/
1. ФИБРОМИАЛГИЯ, 2. ПАДАГРА, 3. ДЕТСКИЙ РЕВМАТИЗМ, 4. ЛАЙМБОРЕЛЛИОЗ, 5. СИСТЕМНОЕ ЗАБОЛЕВАНИЕ СОЕДИНИТЕЛЬНОЙ ТКАН, 6. ПСОРИАЗ СУСТАВОВ, 7. СУСТАВНОЙ РЕВМАТИЗМ, 8. СУСТАВНОЙ РЕВМАТИЗМ II, 9. ГИПЕРПОДВИЖНОСТЬ СУСТАВОВ, 10. ОСТЕОПОРОЗ, 11. РЕВМАТИЧЕСКАЯ ПОЛИМИАЛГИЯ,12. ПОЛИМИОЗИТ, 13. РЕАКТИВНЫЙ АРТРИТ И СИНДРОМ РЕЙТЕРА , 14. РЕВМАТИЗМ ПОЗВОНОЧНИКА И БОЛЕЗНЬ БЕХТЕРЕВА 15. НАСЛЕДСТВЕННОЕ ЗАБОЛЕВАНИЕ СОЕДИНИТЕЛЬНОЙ ТКАНИ 16. СИНДРОМ ШЕГРИНА 17. СЕРОНЕГАТИВНЫЙ СПОНДИЛОАРТРИТ 18. СИСТЕМНЫЙ LUPUS ERYTEMATOSUS (SLE) 19. СИСТЕМНЫЙ СКЛЕРОЗ (СИСТЕМНАЯ СКЛЕРОДЕРМИЯ) 20. ВАСКУЛИТ
СИСТЕМНЫЙ СКЛЕРОЗ (СИСТЕМНАЯ СКЛЕРОДЕРМИЯ) 20. ВАСКУЛИТ
1. ФИБРОМИАЛГИЯ (МЫШЕЧНЫЙ РЕВМАТИЗМ)
Фибро – значит соединительная ткань, а миалгия – боль в мышцах. Фибромиалгия вызывает боль в мышцах, соединительных и внесуставных мягких тканях. Помимо болей в опорно-двигательном аппарате, пациенты страдают различными нарушениями сна: поверхностный сон, частые пробуждения по ночам, чувство разбитости и физического истощения по утрам. К тому же у них наблюдаются различные типы психических и неврологических симптомов, которые могут быть очень разнообразными.
Чаще заболеванием страдают женщины среднего и пожилого возраста. Согласно оценкам фибромиалгией заболевает от 2 до 5% населения, у детей и молодежи заболевание встречается редко.
Причины
Причины возникновения фибромиалгии до сих пор не совсем ясны. На возникновение симптомов влияют многие факторы, вследствие которых болезнь развивается в виде различных изменений со стороны центральной нервной системы (ЦНС). У многих пациентов симптомы проявляются вместе с инфекцией, травмой или в других ситуациях, сопровождающихся болью. Иногда местные боли переходят в общую болевую чувствительность. Некоторые пациенты страдают от гиперподвижности суставов, у других к симптомам присоединяются социальные или психические проблемы. Часто у больных фибромиалгией встречаются другие сопутствующие болезни.
У многих пациентов симптомы проявляются вместе с инфекцией, травмой или в других ситуациях, сопровождающихся болью. Иногда местные боли переходят в общую болевую чувствительность. Некоторые пациенты страдают от гиперподвижности суставов, у других к симптомам присоединяются социальные или психические проблемы. Часто у больных фибромиалгией встречаются другие сопутствующие болезни.
Одной из причин возникновения фибромиалгии является долговременный стресс, вызывающий плохое настроение и чувство угнетения. Причиной стресса может быть многократно повторяющийся и продолжительный внешний раздражитель: работа, чувство неудовлетворённости, спешка, движение, шум, человеческие отношения, денежные проблемы или безработица. У больных фибромиалгией подтверждены такие же гормональные изменения, как у людей, страдающих от долговременного стресса. Ещё неизвестно, является ли причиной возникновения фибромиалгии стресс или депрессия и беспокойство, скорее результат, чем причина фибромиалгии.
Другая причина болезни – недостаток сна или его плохое качество. Во время глубокого сна гипофиз вырабатывает гормон роста, который имеет анаболическое действие (укрепляющее ткани). Если происходит нехватка глубокого сна, гормон роста не выделяется. У больных подтверждено уменьшение выделения гормона роста. В то же время, похожие на фибромиалгию симптомы были выявлены в лабораторных условиях, когда у исследуемых людей был просто нарушен нормальный сон.
Во время глубокого сна гипофиз вырабатывает гормон роста, который имеет анаболическое действие (укрепляющее ткани). Если происходит нехватка глубокого сна, гормон роста не выделяется. У больных подтверждено уменьшение выделения гормона роста. В то же время, похожие на фибромиалгию симптомы были выявлены в лабораторных условиях, когда у исследуемых людей был просто нарушен нормальный сон.
Стресс, нарушения сна и другие причины, влияющие на нарушения выделения гормонов, могут влиять на ЦНС таким образом, что боли усиливаются. Больные часто испытывают личностное и социальное давление, проявляющееся в виде физических симптомов, часто в виде боли.
Симптомы
Важнейшим симптомом фибромиалгии являются продолжительные боли в разных частях тела, на характер которых влияют различные внешние раздражители. Пациенты описывают боли: щиплющая, жгучая, режущая, ноющая, глубинная, изнуряющая, монотонная. Боль усиливают холод, влага, сквозняки и психические стрессы. В сауне боли уменьшаются, но после сауны вновь усиливаются.
Для больных фибромиалгией также характерны: усталость, утомляемость, слабость, отеки и чувство одеревенения. В добавление к болям опорно-двигательного аппарата, могут возникать головные боли, боли в животе, боли при месячных и при мочеиспускании. Многие пациенты чувствуют опухание суставов, хотя врач не диагностирует это. Больные быстро устают при нагрузке. И почти все пациенты жалуются на не дающий отдыха сон.
Диагностика
Диагностика фибромиалгии основана на жалобах пациента и врачебных клинических исследованиях. Для подтверждения заболевания берут во внимание большую группу других заболеваний, которые также вызывают болевые симптомы. Другие болезни не исключают возможности заболевания фибромиалгией.
В беседе с пациентом врач обращает особое внимание как на характер болей в разных ситуациях, так и на качество сна. При врачебном обследовании отмечают болевую реакцию в известных чувствительных точках на теле. Некоторые участки тела очень болезненны. При фибромиалгии нет изменений в анализах крови.
При необходимости проводят дополнительные исследования для исключения других болезней, вызывающих утомляемость и боли, такие как анемия, нарушения функции щитовидной железы, мышечные боли или симптомы, вызванные климаксом. Гиперподвижность суставов также требует обследования.
Часто у больных фибромиалгией имеются сопутствующие болезни, которыми могут быть, например, воспаление кишечника, мочевого пузыря, эндометриоз, головные боли, признаки утомляемости и депрессия. Особенно у пожилых людей фибромиалгия может проявляться одновременно с заболеванием коронарных сосудов, диабетом, повреждением суставов и суставным ревматизмом. Это называется секундарной фибромиалгией.
Лечение
У фибромиалгии нет единого, всем подходящего и приносящего результаты лечения, т.к. причины болезни различны. Очень важно собственное мнение пациента о результатах лечения.
Планирование, осуществление и наблюдение за результатами лечения – основная предпосылка тесной и доверительной совместной работы пациента и врача. Важно прекратить дальнейшие ненужные дополнительные исследования, которые в худшем случае приводят к напрасным хирургическим вмешательствам. Лечить пациента с фибромиалгией лучше всего способен врач поликлиники, который хорошо знает его проблемы.
Важно прекратить дальнейшие ненужные дополнительные исследования, которые в худшем случае приводят к напрасным хирургическим вмешательствам. Лечить пациента с фибромиалгией лучше всего способен врач поликлиники, который хорошо знает его проблемы.
Получение знаний о фибромиалгии – основа лечения. По возможности на ранней стадии пациенту следует пройти курс реабилитации, предназначенный для пациентов с фибромиалгией. Обычно удаётся совмещать его с трудовой деятельностью. Хорошие результаты даёт групповое обучение. На курсах помогают уменьшить утомляемость, сопутствующую заболеванию, поддерживают самолечение и тренинг. Избегание стресса и повышение настроения с помощью тёплых ванн, массажа и других способов физиотерапии, а также обсуждение в группах и психологическая поддержка, являются единой лечебной линией. Некоторым подходит закаливание организма (купание в проруби, холодные камеры) и постепенное увеличение физической нагрузки.
Физкультуру следует вводить осторожно. Подходящие виды спорта: ходьба, ходьба с палками, аква–аэробика, велосипед, танцы и лыжи. Физическая нагрузка направлена на включение организмом собственных защитных механизмов, облегчающих боль.
Физическая нагрузка направлена на включение организмом собственных защитных механизмов, облегчающих боль.
Специального лекарства для лечения фибромиалгии ещё нет. В качестве медикаментозного лечения можно попробовать лекарства, улучшающие качество сна и настроения, например, амитриптилин. Лечение следует начинать небольшими дозами для уменьшения побочных эффектов. Польза такого лечения наблюдается лишь спустя несколько недель. От обычных обезболивающих средств эффекта немного, иногда помогает парацетамол. Польза медикаментозного лечения должна превышать его побочные эффекты. Для снятия болей нервного происхождения некоторым пациентам подходят лекарства, влияющие на ЦНС. Если к фибромиалгии присоединяется длительная бессонница, депрессия или другие психические симптомы, больному необходима психиатрическая помощь.
Прогноз
Прогноз благоприятный, хотя улучшающего лечения нет. Симптомы фибромиалгии сохраняются годами и десятилетиями, но повреждения органов или тканей организма не происходит и заболевание вполне совместимо с жизнью. Многие выходят на пенсию раньше срока по другим причинам. В настоящее время чиновники, решающие пенсионные вопросы, не считают фибромиалгию причиной потери трудоспособности и выхода на пенсию.
Многие выходят на пенсию раньше срока по другим причинам. В настоящее время чиновники, решающие пенсионные вопросы, не считают фибромиалгию причиной потери трудоспособности и выхода на пенсию.
2. ПАДАГРА (греч. podos – нога, греч. agra – захват, дословно «нога в капкане»)
Падагрой заболевают чаще мужчины среднего возраста. В Финляндии падагрой болеет примерно 30000 человек. Появление заболевания может быть обусловлено изменением жизненных привычек и увеличением потребления алкоголя, небольших доз аспирина и диуретиков.
Падагра – заболевание, обусловленное нарушениями пуринового обмена, приводящего к повышению уровня мочевой кислоты (уратов) в крови и отложению их в тканях, в суставных хрящах, эпифизах костей, околосуставных тканях, почках и других органах. Увеличение показателей мочевой кислоты (гиперурекемия) может вызывать почечную недостаточность.
На фоне падагры могут возникать нарушения деятельности энзимов, передающиеся по наследству. Причиной болезни могут быть нарушения питания, переедание, употребление алкоголя, особенно пива, ожирение, сахарный диабет, высокие показатели жиров крови и артериальная гипертония. Падагра также может развиваться как побочное заболевание при приёме диуретиков и аспирина. Иногда падагра проявляется вместе с почечной недостаточностью или заболеваниями крови.
Падагра также может развиваться как побочное заболевание при приёме диуретиков и аспирина. Иногда падагра проявляется вместе с почечной недостаточностью или заболеваниями крови.
Симптомы
Первым симптомом падагры является острое воспаление в суставе большого пальца ноги. Позже воспаляются другие суставы – колени, шейный отдел позвоночника и суставы пальцев рук. Падагра вызывает постоянные суставные изменения и кристаллизацию мочевой кислоты в мягких тканях (тофусы), к ним могут присоединяться заболевания почек. В настоящее время падагра очень редко приводит к инвалидности.
Симптомы проявляются чаще при нагрузке на воспаленный сустав или при приёме алкоголя и пуриносодержащей пищи. Сустав становится горячим, красным и очень болезненным. Картина болезни не всегда типичная. В течение недели воспаление проходит само по себе, но при лечении – быстрее.
Диагностика
При диагностике падагры врач выявляет типичные симптомы и изменения питания пациента. Диагноз подтверждается на основе исследования суставной жидкости, в которой под микроскопом видны кристаллы уратов. У больных падагрой показатели мочевой кислоты обычно высокие. С другой стороны, они могут быть высокими и у здоровых людей. Низкие показатели также не исключают возможности заболевания падагрой. При исследованиях важно проверить работу почек, чтобы исключить нарушение их деятельности.
У больных падагрой показатели мочевой кислоты обычно высокие. С другой стороны, они могут быть высокими и у здоровых людей. Низкие показатели также не исключают возможности заболевания падагрой. При исследованиях важно проверить работу почек, чтобы исключить нарушение их деятельности.
Лечение
В качестве лечения острого приступа падагры используют холод, обезболивающие и противовоспалительные лекарства, покой. Интенсивное лечение при остром приступе падагры – внутрисуставное введение кортизона.
Важнейшим элементом лечения является сбалансированность приёма лекарств, образа жизни и особенно питания пациента. При планировании лечения также необходима консультация врача–диетолога. При необходимости правильным питанием можно поддержать умеренное похудание.
Диету следует соблюдать уже после первого приступа падагры. Диета запрещает продукты питания, из-за которых образуется мочевая кислота и с её помощью можно значительно снизить приём основных лекарств.
Но иногда одной диеты недостаточно для лечения. Тогда после третьего приступа падагры начинают медикаментозное лечение, которое снижает синтез мочевой кислоты в крови. В таких случаях эффективен аллопуринол. Лечение аллопуринолом можно начинать только после подтверждения диагноза падагры. Его побочным эффектом могут быть нарушения работы печени и изменения картины крови, поэтому лечение проводится под контролем анализов крови. Если в течение года на фоне лечения не было приступов, можно прекращать приём препарата.
Тогда после третьего приступа падагры начинают медикаментозное лечение, которое снижает синтез мочевой кислоты в крови. В таких случаях эффективен аллопуринол. Лечение аллопуринолом можно начинать только после подтверждения диагноза падагры. Его побочным эффектом могут быть нарушения работы печени и изменения картины крови, поэтому лечение проводится под контролем анализов крови. Если в течение года на фоне лечения не было приступов, можно прекращать приём препарата.
Прогноз
При грамотном лечении прогноз при падагре хороший, но если по каким-то причинам нельзя использовать аллопуринол могут возникнуть проблемы. Причиной неудачи лечения также может быть несоблюдение диеты.
Диета
Больным падагрой необходимо иметь список различных продуктов питания, содержащих пурин. Его можно найти в аптеках и в интернете. Ниже кратко о важнейших продуктах питания.
Полностью запрещены продукты, содержащие довольно много пурина:
рыба
мясо
горох, бобы, соя, грибы, спаржа
Другие вредные вещества:
все алкогольные напитки (препятствуют выведению мочевой кислоты), особенно пиво
аспириносодержащие жаропонижающие лекарства
Разрешённые продукты питания, содержащие небольшое количество пурина:
зерновые
молочные продукты
яйца, жиры, сахар
фрукты, почти все овощи, картофель
кофе, чай, какао, приправы
икра осетровых рыб
3. ДЕТСКИЙ РЕВМАТИЗМ
ДЕТСКИЙ РЕВМАТИЗМ
Детским ревматизмом называют воспаление суставов, возникающее по неизвестным причинам у детей до 16-летнего возраста, и которое длиться больше шести недель. Определение болезни условное, т.к. причины её возникновения неизвестны, такие же симптомы болезни могут возникать и после 16 лет. Заболевшие в детстве позднее сохраняют первоначальный диагноз.
Детский ревматизм в настоящее время делится на семь подтипов. Для всех видов используют название детский ревматизм или ювенальный идиопатический артрит. Ежегодно в Финляндии заболевает 100-150 детей, половина из которых – до 5 лет.
Причины
Причины возникновения неизвестны. Возможно, их несколько, а наследственные факторы увеличивают риск заболевания какой-либо формой ревматизма. Детский ревматизм напрямую не передаётся по наследству, и не ведёт себя так, как инфекционное заболевание. К детскому ревматизму относят детские болезни (олигоартрит) или формы, похожие на заболевания взрослых (суставной ревматизм, суставной псориаз, ревматизм позвоночника).
Симптомы
Обычно первым симптомом детского ревматизма является утренняя негибкость суставов, которую сразу замечают родители. Негибкость может проявляться либо во всех, либо только в больных суставах. Из-за болей дети хромают или оберегают суставы. Также у них могут быть проблемы со сном. Однако маленькие дети не всегда могут описать боль словами. Часто боль проявляется скверным настроением и обереганием больного сустава. Иногда колено или другой сустав так сильно опухает, что это легко заметить. Жар и слабое кожное воспаление на теле являются начальными опознавательными симптомами детского ревматизма.
Течение болезни
Сложность детского ревматизма в его переменчивости. Болезнь затягивается и разъедает хрящи суставов, кости и суставные связки. Вследствие этого суставы опухают, и их работа ограничена. В настоящее время полное окостенение суставов не встречается. Воспаление глаз могут протекать незаметно, вплоть до полной потери зрения.
У больных детским ревматизмом могут проявляться также задержки развития. Рост может замедлиться вследствие тяжёлого протекания болезни или лечения кортизоном в больших дозах. В опухшем суставе начинается избыточный рост костей, например, в нижней челюсти, ногах, голеностопах, запястьях и пальцах. Особенно в коленях это может проявляться несимметричной длиной конечности или её неправильным положением. При отсутствии лечения детский ревматизм может вызвать воспаления сердца и заболевания почек, угрожающие жизни.
Рост может замедлиться вследствие тяжёлого протекания болезни или лечения кортизоном в больших дозах. В опухшем суставе начинается избыточный рост костей, например, в нижней челюсти, ногах, голеностопах, запястьях и пальцах. Особенно в коленях это может проявляться несимметричной длиной конечности или её неправильным положением. При отсутствии лечения детский ревматизм может вызвать воспаления сердца и заболевания почек, угрожающие жизни.
Диагностика
Основной признак детского ревматизма – опухание одного или нескольких суставов, длящееся свыше шести недель. Ребёнок чувствует себя уставшим, плачет, у него может быть кожная сыпь и температура. Показатели воспаления в крови и CRP могут повышаться. При постановке диагноза также исследуют ревматический фактор и наличие антител в крови. Если анализ крови на антитела положительный, то с большой вероятностью речь идёт уже о детском ревматизме или системном заболевании соединительной ткани. Так как наследственность является важным фактором, необходимо выяснить у родителей, были ли в роду заболевания суставов или псориаз.
Лечение
Детский ревматизм диагностируется и наблюдается в университетских больницах и ревматологической больнице в г.Хейнола врачом–специалистом. Лечение и реабилитация больных проводятся в детском отделении ревматологической больницы.
Цель лечения – уменьшение симптомов и нормализация показателей воспаления в крови (СОЭ, CRP), которые достигаются путём подбора индивидуального медикаментозного лечения и лечебной физкультурой в повседневной жизни. В сложных случаях требуется более серьезное лечение.
Обычно в лечении детского ревматизма используют комплексный подход. Благодаря применению сильных лекарственных средств, результаты наступают быстрее, и время лечения можно сократить.
Детский ревматизм лечат теми же лекарствами, что и взрослый. При длительном лечении используют метотрексат – лекарственное вещество, влияющее на рост клеток. В настоящее время детский ревматизм можно лечить биологическими ТНФ — альфа-лекарствами. Поддерживающая терапия – препараты кортизона.
Лечение детского ревматизма направлено на обеспечение нормального роста ребёнка. Правильному положению конечностей можно помочь наложением лангет и шин. У маленьких пациентов наблюдают за ростом нижней челюсти и зубов и регулярно обследуют глаза. Физиотерапевт разрабатывает индивидуальные программы по поддержанию подвижности суставов и укреплениию мышц. В программу реабилитации входит обеспечение условий для получения ребёнком начального образования.
Прогноз
Современные методы лечения значительно улучшают прогноз детского ревматизма. Пожизненная инвалидность и преждевременная смертность редки. Амилоидоз (нарушение белкового обмена организма) больше не встречается. Большая часть больных способна с помощью лечения вести нормальную трудовую жизнь.
Классификация детского ревматизма
Обычный детский ревматизм
Ø жар, кожное воспаление, воспаление лимфатических узлов, симптомы внутренних болезней
Олигоартрит (воспаление редких суставов)
Ø от 1 до 4-х больных суставов
Серонегативный полиартрит
Ø в крови нет ревматического фактора, больных суставов 5 или больше
Суставной ревматизм взрослого типа
Ø «серопозитивный полиартрит»
Ø в крови присутствует ревматический фактор, больных суставов 5 или больше
Суставный псориаз
Ø кожный псориаз и воспаление суставов
Ø выражены псориатические изменения ногтей без кожных симптомов, сосискообразное воспаление пальцев рук и ног, псориаз у ближайших родственников
Ревматизм позвоночника
Ø «к энтеситу присоединяющийся артрит»
Ø воспаление суставов и энтесит (поражение связочного аппарата). Если из этих симптомов представлен только один, то должно быть также ещё два из нижеследующих признаков: боли в области крестца и поясницы, позитивный антиген HLA-B27, ревматизм позвоночника у кого-нибудь из близких родственников, воспаление глаз, мальчик старше 8 лет.
Если из этих симптомов представлен только один, то должно быть также ещё два из нижеследующих признаков: боли в области крестца и поясницы, позитивный антиген HLA-B27, ревматизм позвоночника у кого-нибудь из близких родственников, воспаление глаз, мальчик старше 8 лет.
Другие формы заболевания
Ø детский ревматизм, который не входит в другие групп
4. ЛАЙМБОРЕЛЛИОЗ (болезнь Лайма или клещево́й боррелио́з)
Болезнь Лайма – инфекционное заболевание, передающаяся через укус клеща. Возбудитель Borrelia burgdorferi бактерия, входящая в класс спирохет. У болезни Лайма нет никакой связи с детским ревматизмом или ревматическими болезнями.
В Финляндии природные очаги болезни Лайма находятся главным образом на островах и на побережьях, хотя клещи также живут по всей стране, включая Лапландию. Но далеко не все клещи являются переносчиками Borrelia-бактерии. В среднем, укус только одного клеща из 50-100 случаев вызывает болезнь. Ежегодно в Финляндии заболевает от укусов клещей примерно 3000 человек, а 10-20% из них – болезнью Лайма. Заболевание может проявляться быстро проходящим кожным воспалением.
Заболевание может проявляться быстро проходящим кожным воспалением.
Профилактика
Болезнь Лайма можно предотвратить, если избегать укусов клещей. Клещи селятся во влажных местах, в которых часто играют дети, поэтому их кожу надо осматривать по вечерам. Это касается и взрослых, живущих в природных очагах. Клещи удаляются из кожи, например, клещевым пинцетом, приобретённым в аптеке. Лучший способ удаления – захватить клеща по возможности близко к коже и аккуратно, круговыми движениями тащить наружу.
Симптомы
Большая часть укусов клещей бессимптомна. Если человека укусил клещ, его необходимо быстро удалить из кожи, т.к. он может быть переносчиком Borrelia-бактерии. В этом случае вокруг укуса через несколько дней появляется покраснение кожи, которое распространяется по кругу от места укуса (кольцевидная эритема). Попавшие в организм бактерии могут вызвать заболевание, похожее на простуду, к которому присоединяются жар, усталость и боли в мышцах. Эта начальная стадия болезни Лайма, для лечения которой используют антибиотики.
Течение заболевания
При отсутствии лечения заболевание может проявиться в разных частях тела спустя месяцы или даже годы после заражения. Это могут быть симптомы поражения опорно-двигательного аппарата (мышечные боли и тугоподвижность), отёк одного или нескольких суставов, в тяжёлых случаях – симптомы поражения ЦНС: лицевой паралич и паралич различных нервов, менингит, неврологические болевые симптомы. Длительные мышечные боли напоминают сложную фибромиалгию. При заболевании, вызванном Borrelia-бактерией, можно наблюдать хроническое воспаление кожи, глаз и сердечной мышцы.
Диагностика
Начальная фаза болезни Лайма подтверждается воспалением кожи вокруг места укуса клеща, которое не проявляется на более поздних стадиях. Единственным симптомом может быть, например, опухание коленных суставов. На этой стадии врач пытается исключить другие болезни и подтвердить бореллиоз с помощью анализов крови. Изучение результатов лабораторных исследований иногда требует экспертизы в инфекционном отделении районной больницы. В диагностике очень помогают сведения о предыдущих укусах клещей, например, месячной давности.
В диагностике очень помогают сведения о предыдущих укусах клещей, например, месячной давности.
Лечение
Простой укус клеща не требует никакого лечения. Если вокруг укуса распространяется воспаление, следует немедленно обратиться к врачу. После явного укуса для лечения бореллиозного кожного воспаления назначается приём антибиотиков в течение двух недель. Инфекция поддается лечению хорошо и поздние симптомы не появляются. Если начальная фаза остается без лечения, и пациент заболевает настоящей болезнью Лайма, тогда требуется длительное и изнурительное лечение антибиотиками, которое чаще всего осуществляется в больничных условиях.
Прогноз
Как правило, от болезни Лайма пациенты излечиваются. При этом заболевании воспаление суставов доброкачественное и не приводит к их разрушению, но боли могут длиться долго. У маленьких детей болезнь протекает тяжелее. Годами длящиеся симптомы воспаления ЦНС встречаются редко. Они могут напоминать симптомы фибромиалгии.
5. СИСТЕМНОЕ ЗАБОЛЕВАНИЕ СОЕДИНИТЕЛЬНОЙ ТКАНИ
У больных системным заболеванием соединительной ткани наблюдаются симптомы многих ревматических заболеваний. Они могут напоминать системный склероз, аутоиммунное заболевание или полимиозит и воспаления суставов. Многие заболевания могут начинаться с симптомов, похожих на системное заболевание соединительной ткани, которые позднее необходимо уточнить. Большинство пациентов – женщины старше 40 лет.
Они могут напоминать системный склероз, аутоиммунное заболевание или полимиозит и воспаления суставов. Многие заболевания могут начинаться с симптомов, похожих на системное заболевание соединительной ткани, которые позднее необходимо уточнить. Большинство пациентов – женщины старше 40 лет.
Причины
Причины неизвестны, но на возникновение болезни влияет наследственность.
Симптомы
Обычно болезнь начинается с общих симптомов, таких как усталость, жар, боли в мышцах и суставах. Почти у всех пациентов выражен симптом Рейно (побледнение пальцев рук). Руки могут отекать так, что пальцы приобретают форму сосисок. Кожа рук уплотняется и позднее атрофируется. У пациента могут быть кожные воспаления и отёки в суставах, похожие на суставной ревматизм.
Течение болезни
Болезнь обычно или исчезает или переходит в какое-нибудь явно выраженное заболевание – суставной ревматизм, системный склероз, иммунное заболевание или полимиозит. Заболевание вызывает изменения во внутренних органах, таких как лёгкие, сердце и почки.
Диагностика
Диагностика проводится на основании анамнеза пациента и анализов крови.
Лечение
Лечение назначается индивидуально согласно симптомам пациента. В качестве лечения используются препараты кортизона и противоревматические препараты метотрексат, гидроксиклорокин. Если у пациента наблюдается побледнение пальцев, рекомендуются сосудосуживающие препараты, например, нифедепин, но лучше всего руки держать в тепле.
Прогноз
Симптомы проявления болезни могут длиться годами. Прогноз зависит от направления развития болезни. Если заболевание не затрагивает внутренние органы, прогноз благоприятный.
6. ПСОРИАЗ СУСТАВОВ (псориатический артрит)
Псориаз (чешуйчатый лишай) – хронический дерматоз, характеризующийся шелушащимися высыпаниями на коже. Псориазом болеет примерно 2% финского населения. Из них лишь у 10% наблюдается воспаление суставов. У половины, страдающих сложной формой кожного псориаза, имеется также псориаз суставов. Встречается как у женщин, так и у мужчин. Иногда картина заболевания схожа с псориазом суставов и диагностируется у пациентов, у которых нет кожного воспаления. Болезнь передаётся по наследству.
Иногда картина заболевания схожа с псориазом суставов и диагностируется у пациентов, у которых нет кожного воспаления. Болезнь передаётся по наследству.
Причины
Причины возникновения псориаза неизвестны, и не исследовано, почему у больных кожными заболеваниями часто проявляются суставные симптомы. При псориазе нарушается регуляция иммунологических защитных сил организма, и появляются кожные воспаления, например, после инфекции, при повреждениях кожи или после ожогов.
Псориаз – наследственное заболевание. Если оба родителя больны псориазом, риск развития заболевания у ребёнка около 50%. Если только один – риск развития заболевания снижается до 20%. Псориаз суставов встречается намного реже.
Симптомы
Выделяют 4 различных формы псориаза суставов. Наиболее часто встречаемая форма – воспаление нескольких суставов с симптомами заострения первых фаланг пальцев конечностей, которые могут проявляться и самостоятельно. Другая форма заболевания проявляется реже, как правило, это воспаление большого сустава. Это может быть только воспаление одного колена без других суставных симптомов. Заболевание, напоминающее ревматизм позвоночника, встречается редко.
Это может быть только воспаление одного колена без других суставных симптомов. Заболевание, напоминающее ревматизм позвоночника, встречается редко.
При суставном псориазе опухают пятка или ахилессово сухожилие, иногда палец руки или ноги опухает в виде сосиски (дактилит, сосискообразный палец). Симптомы заострения фаланговых суставов пальцев проявляются совместно с псориатическим изменением ногтей.
Течение болезни
У больного псориазом заболевание суставов развивается с течением времени. Часто кожный псориаз подтверждается лишь в том случае, если человек обращается к врачу из-за суставных симптомов или изменения ногтей. Обычно суставные симптомы проявляются в 30-50 лет, хотя кожное воспаление в данном случае уже длилось много лет. Суставной псориаз бывает и у детей, но довольно редко.
Диагностика
Псориаз суставов можно заподозрить, если у пациента обнаружены кожный псориаз и воспаление одного или нескольких суставов. Кожное воспаление может быть довольно обширным или ограничиваться только ногтями. Иногда проявляется на коже головы в виде шелушащихся пятен.
Иногда проявляется на коже головы в виде шелушащихся пятен.
При псориазе суставов в анализах крови нет повышенных показателей воспаления (СОЭ, CRP) и ревматического фактора, как при суставном ревматизме.
На рентгене в суставах отмечены такие же эрозивные изменения, как и при суставном ревматизме. У больных заостренные фаланги суставов пальцев разъедаются. Мутилирующий, обезображивающий артрит, обусловленный разрушением костной ткани фаланг пальцев, встречается довольно редко.
Лечение
Своевременное лечение кожных проявлений заболевания и солнечный свет облегчают также и суставные симптомы. В качестве начального лечения подходит укрепление физического состояния суставов и мышц. Для получения дополнительной помощи можно обратиться в отделение реабилитации больницы.
Для облегчения болевых симптомов применяют парацетамол или противовоспалительные и болеутоляющие препараты. Если воспаление суставов затягивается или на рентгене выявлены изменения суставов, в качестве лечения используются те же лекарства, что и при начальном лечении суставного ревматизма. Метотрексат эффективен при кожных воспалениях, и для лечения суставного псориаза он подходит лучше, чем для лечения суставного ревматизма. Подобное лекарство нового поколения – лефлуномид. При лёгком суставном псориазе, для устранения суставных симптомов, следует сначала попробовать сульфасалицилаты. Циклоспорин подходит для лечения, как сложных кожных воспалений, так и для лечения воспаления суставов. Инъекции кортизона используют для лечения опухших суставов. При мутилирующем, обезображивающем артрите делают операции артропластику или эндопротезирование.
Метотрексат эффективен при кожных воспалениях, и для лечения суставного псориаза он подходит лучше, чем для лечения суставного ревматизма. Подобное лекарство нового поколения – лефлуномид. При лёгком суставном псориазе, для устранения суставных симптомов, следует сначала попробовать сульфасалицилаты. Циклоспорин подходит для лечения, как сложных кожных воспалений, так и для лечения воспаления суставов. Инъекции кортизона используют для лечения опухших суставов. При мутилирующем, обезображивающем артрите делают операции артропластику или эндопротезирование.
Сложный суставной и кожный псориаз также можно лечить биологическими ревматическими лекарствами. В настоящее время в Финляндии используют ингибиторы (блокаторы) ФНО α: инфликсимаб, адалимумаб, этанерсепт. Они быстро снимают воспаление. Адалимумаб и этанерсепт пациент может колоть себе сам. Инфликсимаб вводится пациенту внутривенно–капельно в стационаре.
Прогноз
В среднем, псориаз суставов более лёгкое заболевание, чем ревматизм суставов. Долговременный прогноз чаще всего очень хороший. Лечение сложных, вызывающих изменения в суставах заболеваний, следует проводить как можно быстрее. Лечебная терапия в начальной стадии заболевания более эффективна. Без лечения псориаз суставов может привести к инвалидности, разрушению суставов или тугоподвижности позвоночника.
Долговременный прогноз чаще всего очень хороший. Лечение сложных, вызывающих изменения в суставах заболеваний, следует проводить как можно быстрее. Лечебная терапия в начальной стадии заболевания более эффективна. Без лечения псориаз суставов может привести к инвалидности, разрушению суставов или тугоподвижности позвоночника.
7. СУСТАВНОЙ РЕВМАТИЗМ
Суставной ревматизм (ревматоидный артрит, arthritis rheumatoides) – обычное воспалительное заболевание суставов. Ежегодно им заболевает 1700 финнов, обычно женщины 60-70 лет, реже молодые мужчины. В Финляндии больных суставным ревматизмом насчитывается примерно 35000 человек.
Причины
Причины возникновения суставного ревматизма неизвестны, но он входит в, так называемые, аутоиммунные заболевания, при которых иммунологическая защита организма направлена против своих же тканей. Суставной ревматизм не является наследственной болезнью, а восприимчивость к ней передаётся по наследству слабо. Курение, послеродовый период, всевозможные инфекции, психические факторы и травмы суставов способствуют возникновению суставного ревматизма. Явных связей между питанием и возникновением болезни не замечено, но при лечении следует обращать внимание на здоровое питание.
Явных связей между питанием и возникновением болезни не замечено, но при лечении следует обращать внимание на здоровое питание.
Сначала изменения в организме могут начинаться не в суставах, а в других местах. При воспалении суставная оболочка уплотняется, в ней вырастают новые кровеносные сосуды, в тканях циркулируют воспалительные клетки. Активные воспалительные клетки выделяют в окружающую среду иммунные комплексы (интерлейкины, простагландины, Tnf-alpha), которые вызывают в организме воспаление: усталость, жар, повышенные показатели крови и CRP.
Воспалённая ткань растёт и расширяется по поверхности суставных хрящей и костей. Она постепенно разъедает здоровые хрящи, кости и суставные связки. В связи с этим структура сустава разрушается, и его работа нарушается.
Симптомы
Суставной ревматизм начинается с небольшой боли в суставе, которая проявляется по утрам в виде болезненности и негибкости пальцев рук или подушечек ног. Видимый симптом – отёк сустава, возникает при увеличении количества суставной жидкости и утолщении суставной оболочки.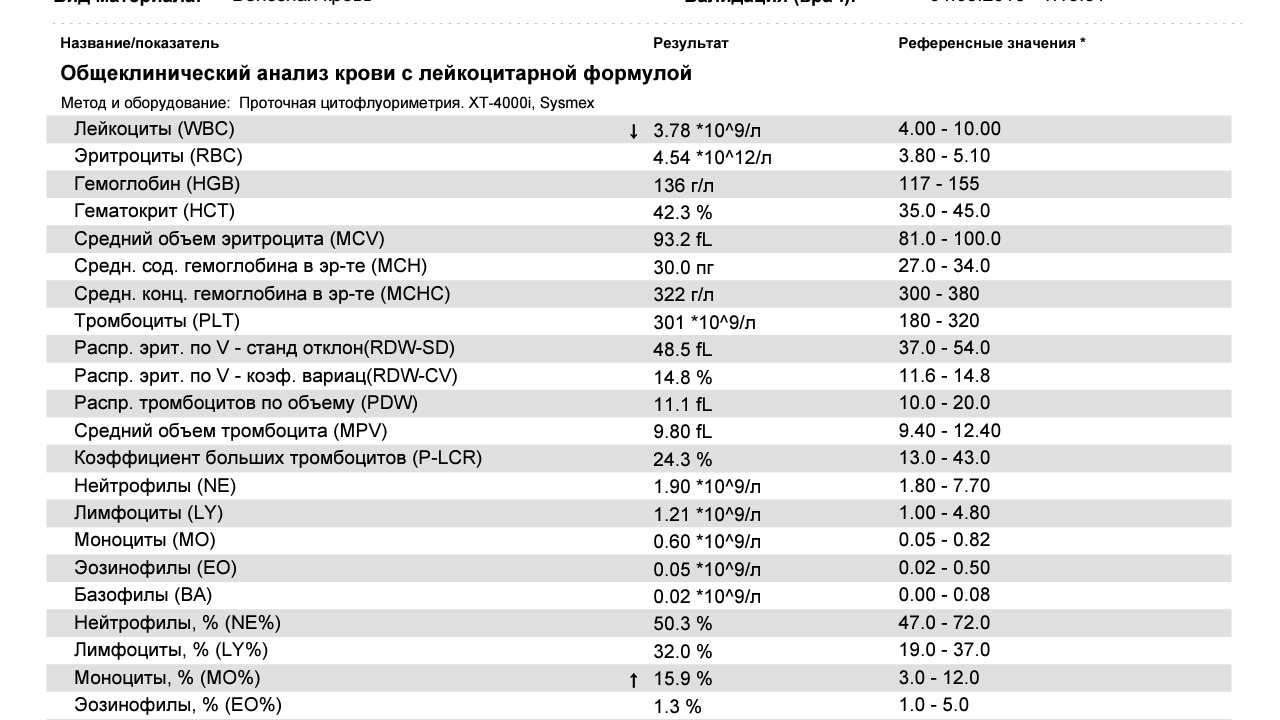 При сильном воспалении сустав краснеет и становится горячим. Отёк начинается чаще всего в пальцах рук и запястьях. Суставной ревматизм обычно симметричное заболевание суставов пальцев ног и рук, но оно может распространяться на все суставы конечностей, а также на челюстные суставы и шейный отдел позвоночника. Не проявляется обычно в первых фалангах пальцев и пояснице. В начальной стадии болезнь вызывает ухудшение общего состояния, чувство недомогания, усталость и негибкость суставов по утрам.
При сильном воспалении сустав краснеет и становится горячим. Отёк начинается чаще всего в пальцах рук и запястьях. Суставной ревматизм обычно симметричное заболевание суставов пальцев ног и рук, но оно может распространяться на все суставы конечностей, а также на челюстные суставы и шейный отдел позвоночника. Не проявляется обычно в первых фалангах пальцев и пояснице. В начальной стадии болезнь вызывает ухудшение общего состояния, чувство недомогания, усталость и негибкость суставов по утрам.
Течение болезни
Если сопротивляемость организма побеждает болезнь, симптомы суставного ревматизма исчезают совсем или не проявляются длительное время. Чаще всего суставной ревматизм – это десятилетиями длящееся заболевание. Разъедание хрящей начинается уже через несколько месяцев с начала заболевания. С годами эрозии расширяются и захватывают большее количество суставов.
Сильнее всего пациенты страдают при повреждении крупных суставов конечностей (тазобедренного, колена, плечевого сустава) и шейного отдела позвоночника. Движение суставов затрудняется, но пациенты гораздо больше страдают от болей. Боль проявляется повышенной чувствительностью суставов, однако, в начальной стадии она не очень значительная.
Движение суставов затрудняется, но пациенты гораздо больше страдают от болей. Боль проявляется повышенной чувствительностью суставов, однако, в начальной стадии она не очень значительная.
При продолжительном суставном ревматизме симптомы проявляются также в других органах. Длительное воспаление высушивает ткани: кожа становится тоньше, мышцы отмирают, кости ломаются, и гемоглобин крови снижается. Сухость слизистых оболочек глаз, рта и половых органов происходит от синдрома Шенгрена. От трения в локтях, пальцах рук и ног могут вырастать ревматические шишки. Побледнение пальцев или симптом Рейно является сигналом заболевания сосудов. В лёгких развивается плеврит, ревматические узлы и иногда происходят серьёзные лёгочные изменения. Амилоидоз (нарушение белкового обмена) возникает, как следствие длительного активного воспаления, но поражение почек, вызываемое им, в настоящее время встречается редко.
Диагностика
В начале заболевания суставной ревматизм сложно диагностировать. При подозрении на суставной ревматизм, пациент направляется к врачу – специалисту. Симптомами заболевания являются явные отёки суставов, особенно пальцев и запястьев, чувствительность подушечек стопы, в крови повышенные показатели воспаления (СОЭ, CRP) и ревматический фактор. Суставной ревматизм оценивается по семи критериям. При наличии четырёх критериев из семи, пациенту ставится диагноз суставной ревматизм, и активное лечение следует начинать как можно раньше.
При подозрении на суставной ревматизм, пациент направляется к врачу – специалисту. Симптомами заболевания являются явные отёки суставов, особенно пальцев и запястьев, чувствительность подушечек стопы, в крови повышенные показатели воспаления (СОЭ, CRP) и ревматический фактор. Суставной ревматизм оценивается по семи критериям. При наличии четырёх критериев из семи, пациенту ставится диагноз суставной ревматизм, и активное лечение следует начинать как можно раньше.
Симптомы иммунологических нарушений подтверждает находящийся в крови ревматический фактор, а иногда и антитела. Ревматический фактор выявлен не у всех больных суставным ревматизмом. Он также может быть найден у больных другими заболеваниями или у совершенно здоровых людей. Следовательно, диагноз суставного ревматизма радикально не зависит от наличия ревматического фактора.
Классификация суставного ревматизма:
утренняя негибкость суставов, по меньшей мере, в течение часа
опухание, по меньшей мере, трёх суставов
отёк сустава руки
симметричный отёк сустава
ревматические шишки
ревматический фактор в крови
видимые на рентгене повреждения в суставах
Лечение
Лечение суставного ревматизма должно быть многосторонним. Больным хроническими заболеваниями важно больше знать о болезни и возможностях её лечения.
Больным хроническими заболеваниями важно больше знать о болезни и возможностях её лечения.
Течение суставного ревматизма не позволяет влиять на него иными средствами, кроме как лекарствами. Иногда для предотвращения инвалидности требуется операции и физиотерапия. Эффективное медикаментозное лечение особенно значимо на начальной стадии, и когда разрушение суставов прогрессирует.
На начальной стадии в лечение входят, прежде всего, препараты, замедляющее течение болезни. В комплексном лечении суставного ревматизма используют метотрексат, сульфасалицилат, гидроксиклорокин, препараты золота, лефлуномид и циклоспорин, можно попробовать биологические лекарства. Несмотря на побочные эффекты, приносимая ими польза намного больше, чем вред. Лечение, начатое на ранней стадии, даёт большей эффект.
Большинству пациентов требуется болеутоляющие препараты (парацетамол, противовоспалительные лекарства). Они не тормозят развитие болезни, но хорошее обезболивание улучшает качество жизни. Препараты кортизона используют в качестве поддерживающей терапии для уменьшения болей, а также для поддержания работы суставов. Инъекции кортизона непосредственно в сустав временно снимают отёк и значительно улучшают подвижность. У лечащего врача должны быть наготове необходимые пациенту шприцы с кортизоном.
Препараты кортизона используют в качестве поддерживающей терапии для уменьшения болей, а также для поддержания работы суставов. Инъекции кортизона непосредственно в сустав временно снимают отёк и значительно улучшают подвижность. У лечащего врача должны быть наготове необходимые пациенту шприцы с кортизоном.
Операционным лечением можно убрать из сустава или из сухожилия воспалённые ткани, не восприимчивые к лекарствам, а также исправить уже повреждённый сустав. Часто с помощью искусственного сустава можно предотвратить развитие инвалидности.
Физиотерапией лечат боли и сохраняют двигательную активность суставов с помощью специальных упражнений. В активной фазе нужно поддерживать подвижность суставов и физическое состояние мышц.
Специальный врач обучает щадящим двигательным навыкам. Различными шинами пробуют уменьшить боли в суставах и предотвратить их неправильное положение.
Реабилитация поддерживает трудовую и двигательную активность. На курсах реабилитации, сразу после выявления болезни, пациенты получают информацию о заболевании и его влиянии на повседневную жизнь. Следует уделить достаточно внимания профессиональной реабилитации работоспособного населения и молодёжи. KELA организует реабилитацию в особо тяжёлых случаях.
Следует уделить достаточно внимания профессиональной реабилитации работоспособного населения и молодёжи. KELA организует реабилитацию в особо тяжёлых случаях.
Прогноз
На начальной стадии суставного ревматизма делать прогноз довольно сложно. Поэтому даже к слабовыраженным симптомам суставного ревматизма нужно относиться серьёзно. В настоящее время большая часть больных живёт нормальной жизнью, заводит семью и сохраняет работоспособность. Хотя улучшающее лечение есть, суставной ревматизм прогрессирует десятилетиями и разрушает суставы, но угрозы полной потери двигательной активности нет.
8. СУСТАВНОЙ РЕВМАТИЗМ II
Артроз или остеоартрит распространённое заболевание суставов. Оно связано с увеличением среднего возраста населения. Почти у каждого пенсионера обнаружен остеоартрит, но только части из них он наносит значительный вред здоровью. Из-за неспособности пожилых людей самостоятельно передвигаться, общество несёт значительные расходы. Для сохранения двигательной способности пожилых людей, в Финляндии ежегодно делаются тысячи операций по замене тазобедренных и коленных суставов.
Чаще артроз проявляется в межпальцевых суставах стопы, первом плюснефаланговом суставе кисти, в суставах позвоночника, но наибольший вред здоровью приносит артроз тазобедренных и коленных суставов.
Причины
Возникновению артроза больших суставов способствуют пожилой возраст, тяжёлая работа, спорт с нагрузкой на суставы, ожирение, травмы и воспаления суставов, наследственность. Большая проблема – увеличение веса, которая вызывает и всегда осложняет большую часть коленных артрозов. Артроз пальцев стопы и кисти является, по большей части, наследственным заболеванием.
Симптомы
На начальной стадии артроза важнейшим симптомом является боль, которая усиливается при начале движения после отдыха (стартовая боль). Первичная боль возникает при спуске по лестнице вниз, в дальнейшем к ней присоединяется и боль при подъёме вверх. При развитии болезни уменьшается амплитуда движения сустава. Колени разворачиваются в стороны, и появляется кривоногость. В пальцах, на месте суставов, разрастаются костные шишки.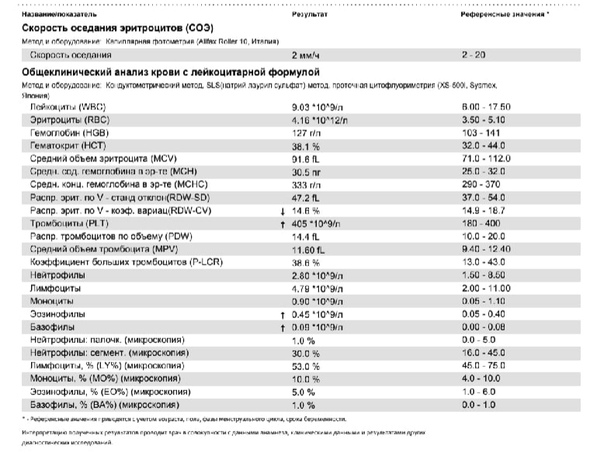 Неровные хрящевые поверхности суставов хрустят при движении.
Неровные хрящевые поверхности суставов хрустят при движении.
Артроз ухудшается постепенно, с течением лет. Проблемы зависят от поражённого сустава. Артроз позвоночника приводит к образованию костных шпор и сдавливанию выходящих из спинного мозга нервов, вследствие чего спинная боль переходит в ноги (ишиас). Артроз тазобедренных и коленных суставов осложняет движения и может вызывать сильные боли.
Течение болезни
В начале возникновения артроза гладкий хрящ, покрывающий поверхность сустава, начинает разлагаться. На это организм реагирует разрастанием костной ткани хряща. Суставы становятся твёрдыми и соприкасаются друг с другом, объём их движения уменьшается. Обычно сустав принимает вынужденное положение. Постепенно внутренняя поверхность, покрывающая суставную оболочку повреждённого сустава, раздражается и воспаляется. В суставе появляется жидкость, и он может покраснеть. Сустав воспаляется, и артроз прогрессирует.
Диагностика
Врач ставит диагноз артроза на основании симптомов и рентгена.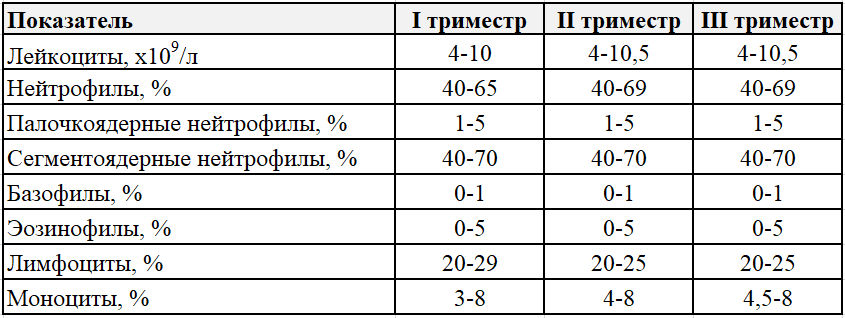 Тем не менее, множественный артроз может ошибочно лечиться, как подагра или суставной ревматизм. Анализ крови не диагностирует артроза.
Тем не менее, множественный артроз может ошибочно лечиться, как подагра или суставной ревматизм. Анализ крови не диагностирует артроза.
Лечение
Артроз нельзя вылечить. В качестве обезболивания применяют, в первую очередь, парацетамол и при необходимости противовоспалительные лекарства. Некоторым помогает глюкозамин. Противоревматические гелиевые мази, содержащие противовоспалительные лекарства, помогают при артрозе пальцев рук. В раздражённые и отёчные суставы врач может вводить препараты кортизона. Артроз коленей можно лечить инъекциями гиалуроната. Сложные и болезненные артрозы тазобедренных и коленных суставов лечат оперативным путём.
Следует предотвращать слишком большую нагрузку на больные суставы. Палочка или роллатор и стулья на высоких ножках облегчают повседневную жизнь. Также следует прекратить перенос тяжестей.
Контроль веса – важная часть лечения, т.к. лишний вес, в первую очередь, нагружает суставы. Работоспособность суставов поддерживается движением, а состояние мышц – регулярной лечебной физкультурой. Для выпрямления тазобедренных и коленных суставов нужно упражняться. Для выпрямления коленей можно упражняться сидя на стуле. Если чувствуется боль, выпрямительные движения можно делать лёжа на спине, подушка под коленями. Холодный компресс в острой фазе успокаивает воспалённые и болезненные суставы. В спокойной фазе заболевания согревание суставов приносит чувство облегчения. При лечении артроза пальцев рук регулярные упражнения сохраняют их подвижность.
Для выпрямления тазобедренных и коленных суставов нужно упражняться. Для выпрямления коленей можно упражняться сидя на стуле. Если чувствуется боль, выпрямительные движения можно делать лёжа на спине, подушка под коленями. Холодный компресс в острой фазе успокаивает воспалённые и болезненные суставы. В спокойной фазе заболевания согревание суставов приносит чувство облегчения. При лечении артроза пальцев рук регулярные упражнения сохраняют их подвижность.
Прогноз
Большая часть пациентов хорошо справляется со своей болезнью. Мучительнее протекают болезни, начинающиеся в молодом возрасте и в нескольких суставах одновременно. Артроз вызывает ухудшение нормальной жизни. Увеличение избыточного веса населения – причина возникновения артроза в будущем. Операцией по замене суставов можно избежать возникновения инвалидности у пациента.
9. ГИПЕРПОДВИЖНОСТЬ СУСТАВОВ
Гиперподвижность суставов – это совокупность симптомов, при которых у суставов аномально широкая амплитуда движения. Гиперподвижность суставов особенно выражена у детей и молодых женщин. У пожилых людей встречается редко. Для некоторых профессий (музыкант, акробат) выгодна широкая амплитуда движения суставов, но она может причинять вред суставам.
Гиперподвижность суставов особенно выражена у детей и молодых женщин. У пожилых людей встречается редко. Для некоторых профессий (музыкант, акробат) выгодна широкая амплитуда движения суставов, но она может причинять вред суставам.
Причины
Ослабление или натяжение суставных связок у людей различны. Вероятно, в строении связующего белка, коллагена, соединительной ткани есть отличия. Часто гиперподвижность суставов – наследственная. Её трудно отличить от синдрома Элерса-Данлоса (гиперэластичность кожи).
Симптомы
Гиперподвижность суставов не обязательно вызывает вредные последствия. Частым симптомом является боль, которая локализуется в суставах (тазобедренный, колено, плечо, запястье) или спине. Обычные болевые состояния легко трактуют, как фибромиалгию, одной из причин которой может быть гиперподвижность какого-либо сустава. В сложных формах заболевания суставы могут легко выворачиваться. К совокупности симптомов могут присоединиться также грыжа, варикозное расширение вен, нарушение венозного кровообращения, опущение матки и проблемы мочеиспускания. Гиперподвижность может привести к артрозу.
Гиперподвижность может привести к артрозу.
Диагностика
Гиперподвижность суставов определяется по шкале Бейгтона. Если у человека имеются пять критериев из одиннадцати, суставы считаются гиперподвижными.
Шкала Бейгтона
пассивное тыльное сгибание мизинца руки более 90° (левая и правая рука)
пассивное приведение большого пальца руки к сгибательной поверхности предплечья (левая и правая рука)
переразгибание локтевых суставов более 10° (левая и правая рука)
переразгибание коленей более 10°(левая и правая нога)
наклон вперед, не сгибая коленей, с касанием пола ладонями
Лечение
Пациент должен знать о происхождении симптомов. Полного лечения нет, но симптомы можно облегчить с помощью лечебной физкультуры для суставов и мышц. Следует прекратить виды деятельности, увеличивающие риски и приводящие к широкой амплитуде движения суставов и вывихам. Обычные обезболивающие препараты уменьшают боли. Гиперподвижность суставов следует учитывать при выборе профессии.
Прогноз
С возрастом амплитуда движения суставов уменьшается. Это улучшает долговременный прогноз.
10. ОСТЕОПОРОЗ
Остеопороз — прогрессирующее уменьшение плотности костей, приводящее к снижению их прочности и увеличению вероятности перелома. После 30 лет плотность костей начинает медленно уменьшаться. У пожилых людей увеличивается риск переломов костей в результате падения. В Финляндии более 400000 людей страдают остеопорозом, из них большая часть женщины старше 50 лет.
Причины
Возрастное уменьшение плотности костей является нормальным физиологическим процессом. Но резкое уменьшение плотности костной ткани приводит к заболеванию остеопорозом.Чаще остеопороз встречается у женщин, чем у мужчин. Риск заболевания у женщин увеличивается в климактерический период, когда уменьшается выработка женских половых гормонов (эстрагенов), регулирующих обмен веществ в костной ткани и предотвращающих остеопороз. Короткий период половой зрелости (позднее начало и раннее окончание месячных ) тоже является причиной остеопороза.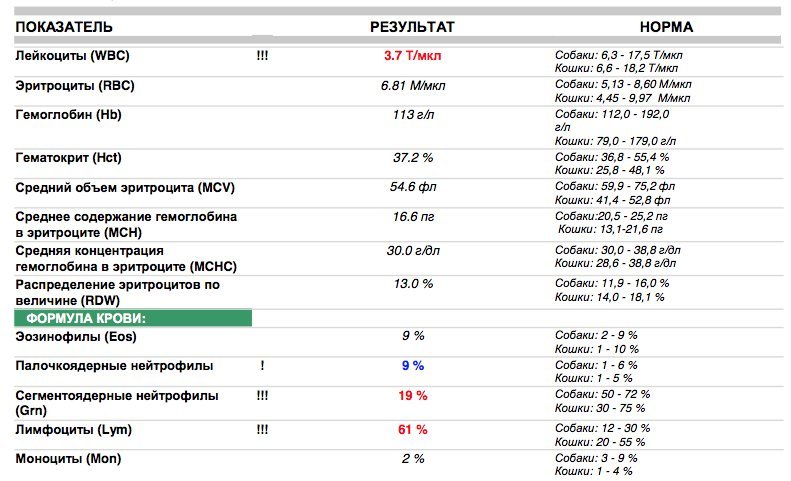
Худощавое телосложение, недостаток физкультуры, витамина D (солнечный свет) и/или кальция, курение, излишнее потребление соли, заболевания кишечника, ревматизм, диабет, заболевания почек, а также некоторые лекарства (кортизон, противоэпилептические препараты) увеличивают риск развития остеопороза. Избыточный вес хоть и является опасным заболеванием, но в какой-то мере защищает от остеопороза. Предрасположенность к остеопорозу является наследственной.
Симптомы
Остеопороз протекает бессимптомно. Проблемы возникают при переломах костей, самые распространённые из которых–переломы позвонков. В этом случае рост уменьшается и осанка изменяется. Сложными считаются переломы шейки бедра. За последние 15 лет в Финляндии количество переломов верхней части шейки бедра удвоилось. Хотя переломы, вызванные остеопорозом, лечатся оперативным методом, качество жизни пожилых людей ослабевает.
Диагностика
Опытный врач сможет быстро поставить диагноз пожилому человеку, измерив его рост. Если с годами рост уменьшился более чем на 5 сантиметров, и осанка стала сутулой, диагоз поставлен правильно.
Если с годами рост уменьшился более чем на 5 сантиметров, и осанка стала сутулой, диагоз поставлен правильно.
Плотность костей можно измерить. Измерение делается на основании анализа костей спины и верхней части бедренной кости.
В больницах и в частных клиниках есть приборы для обследования остеопороза. На основании международных критериев, у женщин диагоз констатируется при плотности костей ниже 2,5 ед. стандартного отклонения (standard deviation), чем в молодом возрасте. У мужчин граница – 3 ед. стандартного отклонения.
По обычному рентгеновскому снимку костей можно оценить начальную стадию остеопороза. На рентгеновском снимке хорошо виден перелом костей позвоночника. Плотность измеряют ультразвуковым исследованием пяточных костей, но таким способом невозможно установить точное место перелома.
Профилактика
Появление остеопороза можно предупредить. Молодые девушки должны повышать плотность костной ткани и наращивать костную массу, которая с возрастом защищала бы от возможных переломов.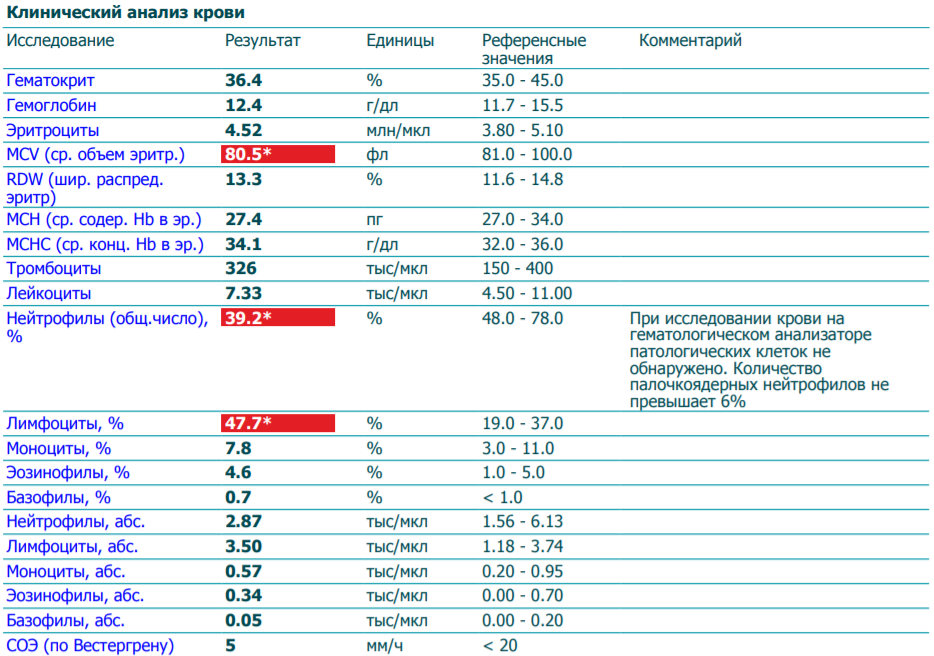
Предотврати остеопороз:
Ÿ Постоянно двигайся
Ÿ Худей осторожно и избегай резкого падения веса
Ÿ Чаще бывай на свежем воздухе, таким образом получишь витамин D
Ÿ В рацион должны входить молоко, сыр, лесные грибы и рыба
Ÿ Не кури
Ÿ Потребляй ограниченное количество соли
Ÿ Заваривай чай, в состав которого входит флорид, укрепляющий кости
Ÿ Женщинам после 40 лет рекомендуется делать обследование на наличие эстрогенов
Ÿ В тёмное время года людям после 50 лет рекомендуется принимать витамин D и кальций
Ÿ В пожилом возрасте особенно опасны падения, поэтому рекомендуется носить специальную защищающую кости одежду.
Лечение
Остеопороз трудно лечится, потому что костная ткань медленно обновляется. Лечение кортизоном назначается людям, у которых были переломы и плотность костных тканей постоянно уменьшается.
Лечение предусматривает достаточное получение витамина D и кальция. Ежедневная норма кальция 800 мг, она содержится, например, в трёх стаканах молока или кефира. Сыр и другие молочные продукты тоже являются хорошими источниками кальция.
Ежедневная норма кальция 800 мг, она содержится, например, в трёх стаканах молока или кефира. Сыр и другие молочные продукты тоже являются хорошими источниками кальция.
Витамин D человек получает, находясь под солнцем, а также из продуктов питания, например, рыба и грибы богаты витамином D. Людям старше 70 лет рекомендуется принимать витамин D по15 микрограмм в день (600 единиц). Такое количество трудно получить из продуктов питания, поэтому пожилым людям его назначают в виде пищевых добавок.
Лечение остеопороза лекарственным методом постоянно развивается. Лечение продолжительное и достаточно дорогое. Важной лекарственной группой являются бифосфонаты (алендронат, этидронат, резидронат и ибандроновая кислота). В настоящее время дозировка лекарственных препаратов расчитана так, что их нужно принимать не чаще, чем раз в неделю или месяц. Лекарственные препараты есть в форме спрея для носа. Также женщины могут принимать препараты с содержанием гормона эстрогена или лекарственные препараты действующие таким же образом (ралоксифен). В трудных случиях используются стронтиум и терипаратид.
В трудных случиях используются стронтиум и терипаратид.
11. РЕВМАТИЧЕСКАЯ ПОЛИМИАЛГИЯ
Полимеалгия – достаточно распространённое заболевание, которое вызывает мышечные боли. «Поли»- означает много, «миалгия» — мышечные боли.
Причины
Причины болезни не выяснены, но спровоцировать заболевание может вирусная инфекция. Чаще всего полимиалгией болеют женщины после 50 лет.
Симптомы
Симптомы болезни проявляются достаточно медленно. Появляются боли и онемение (окостенелость) в мышцах шеи, плеч, поясницы и бёдер. Мышцы становятся чувствительными и болезненными при движении и от прикосновения. Отёчность суставов наблюдается редко. Из-за появления мышечных и суставных болей затрудняется утренний подъём. Также у пациента может быть усталость и повышенная температура. В анализе крови повышены показатели воспаления, поэтому ранее здоровый и бодрый человек чувствует себя серьёзно больным.
Часто к мышечной форме ревматизма присоединяется воспаление артерий. Воспаление височной артерии вызывает боль в висках или в щеках, например, при разжёвывании пищи. Воспалённую артерию иногда можно увидеть в области виска, она напряжена и увеличена. Пульс в артерии может отсутствовать. Важно вовремя обнаружить воспаление височной артерии (темпоральный артерит), потому что ответвление височной артерии идёт в основания глаз. Непроходимость височной артерии может привести к потере зрения.
Воспаление височной артерии вызывает боль в висках или в щеках, например, при разжёвывании пищи. Воспалённую артерию иногда можно увидеть в области виска, она напряжена и увеличена. Пульс в артерии может отсутствовать. Важно вовремя обнаружить воспаление височной артерии (темпоральный артерит), потому что ответвление височной артерии идёт в основания глаз. Непроходимость височной артерии может привести к потере зрения.
Диагностика
Врач ставит диагноз на основании симптомов заболевания, возраста пациента, болей, общего состояния и анализа крови. Пожилым людям назначают и другие виды обследования. При подозрении на воспаление височной артерии, пациента направляют в Центральную больницу на обследование.
Лечение
Для лечения полимиалгии назначают препараты кортизона. Лечение длится минимум год и доза кортизона постепенно снижается на основании наблюдений за течением болезни, симптомами, формулой крови. Также для лечения используются и другие препараты, например, метотрексат. Воспаление височной артерии лечится в больнице.
Воспаление височной артерии лечится в больнице.
Прогноз
Прогноз полимиалгии хороший. При правильном подходе к лечению, через несколько лет почти ко всем заболевшим здоровье возвращается.
12. ПОЛИМИОЗИТ
Полимиозит – это достаточно редкое воспалительное заболевание мышц, которое проявляется как вместе с ревматизмом, так и самостоятельным заболеванием соединительной ткани. Также к заболеванию относятся кожный и инклюзивный миозиты.
В Финляндии ежегодно заболевает около 20 человек. Чаще болеют взрослые люди, но кожная форма миозита встречается и у детей.
Причины
Причины возникновения миозита неизвестны, но очевидно, речь идёт о нарушении функции аутоимунной системы, как и при других cистемных заболеваниях соединительных тканей. Воспаление мышц может проявляться легкой формой суставного ревматизма, заболеванием Шегрина или симптомами SLE. Кожная форма миозита может возникать на фоне рака.
Симптомы
Важным симптомом полимиозита является слабость мышц. Обычно симптомы проявляются медленно, и сначала боли появляются в бедренных, тазобедренных и плечевых мышцах. Появляются трудности при вставании и при поднятии рук вверх. Так же у пациентов появляются трудности при глотании пищи. При кожной форме миозита появляются симптомы на коже рук и лица. Инклюзивный миозит проявляется медленнее, чем другие формы миозита. У детей после воспаления кальций откладывается в рубцевую ткань. Воспаление вызывает усталость, снижение веса и лихорадку.
Обычно симптомы проявляются медленно, и сначала боли появляются в бедренных, тазобедренных и плечевых мышцах. Появляются трудности при вставании и при поднятии рук вверх. Так же у пациентов появляются трудности при глотании пищи. При кожной форме миозита появляются симптомы на коже рук и лица. Инклюзивный миозит проявляется медленнее, чем другие формы миозита. У детей после воспаления кальций откладывается в рубцевую ткань. Воспаление вызывает усталость, снижение веса и лихорадку.
Диагностика
Диагноз миозита ставят на основании анализа крови. Также делается биопсия. При необходимости делается электроневромиография (ENMG) и магнитно-резонансная томография. Пожилые люди, при необходимости проходят дополнительное обследование.
Лечение
Лечение начинается в больнице достаточно большими дозами кортизона. Если лечения кортизоном не достаточно, то назначается метотрексат. В трудных случаях назначаются новые биологические ревматические препараты.
Лечение длится годами, поэтому важно поддерживать тонус мышц в форме.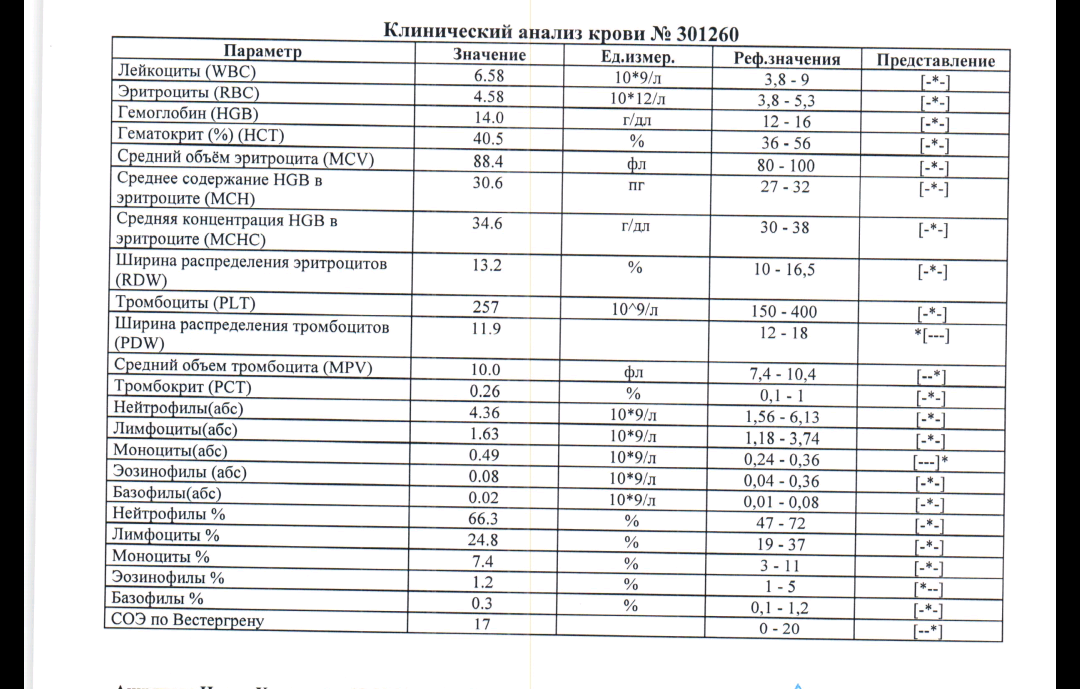
Профилактика
Раньше миозит был опасным заболеванием, но сейчас от него можно полностью излечится.
13. РЕАКТИВНЫЙ АРТРИТ И СИНДРОМ РЕЙТЕРА
Инфекционные заболевания кишечника, мочевыводящих путей или венерические инфекции могут быть причиной воспаления суставов. В дальнейшем это приводит к реактивному воспалению суставов (артрит), то есть иммунологической реакции организма на инфекцию. При синдроме Рейтера у пациентов могут быть воспаления на слизистой глаз, кожи или рта, половых органах или мочевыводящих путей.
Причины
Оболочка сустава реагирует воспалением на бактерии-инфекции. Организм вырабатывает антитела (иммунная реакция) против самого себя. Реактивное воспаление суставов начинается, например, с хламидии, сальмонеллы или обычным расстройством кишечника. Велик риск заболевания кишечными инфекциями в больших туристических центрах жарких странан.
У заболевания есть наследственная предрасположенность. У большой части пациентов обнаружен HLA-B27-антиген. Реактивный артрит в основном проявляется у молодых людей.
Реактивный артрит в основном проявляется у молодых людей.
Симптомы
Симптомы реактивного артрита начинаются через неделю после кишечной или венерической инфекции и проявляются болями и отёками суставов. Первоначальная инфекция, как правило, уже проходит. Заболевание проявляется воспалением нескольких суставов. Обычно нижние конечности поражаются чаще, чем верхние. А также крестец и подвздошная кость становятся болезненными.
Реактивный артрит и синдром Рейтера вызывают шелушащиеся кожные покраснения на стопах, пальцах ног и на слизистой половых органов (баланит). Также у больных могут быть покраснения слизистой глаз или воспаление мочеточников. Повышенная температура и усталость являются обычными симптомами заболевания. Анализ крови свидетельствует о наличии инфекции в организме.
Диагностика
Диагносцировать реактивный артрит достаточно просто, если у пациента недавно была венерическая или кишечная инфекция. Иногда симптомов инфекции мало или нет вообще. Тогда причины инфекции выясняются посевом или анализом крови на антитела. Иногда возникает необходимость исключить другие заболевания, как, например, начинающийся суставной ревматизм.
Иногда возникает необходимость исключить другие заболевания, как, например, начинающийся суставной ревматизм.
Также делается ЭКГ , потому что есть риск воспаления сердца.
Лечение
Инфекция, вызвавшая воспаление суставов, лечится антибиотиками. Также назначается лечение хламидии. Назначаются противовоспалительные, обезболивающие и иногда кортизоносодержащие лекарственные препараты в виде инъекций в поражённый сустав или в виде таблеток. Отёкшие суставы нельзя перенагружать, но поддерживающая физкультура не противопоказана.
Также можно использовать лечение холодом, например, пакет со льдом, которое облегчает воспаление и боль.
Если в течение нескольких месяцев воспаление суставов не проходит, то назначаются ревматические препараты, один из них сульфасалацин.
Повторное воспаление можно избежать безопасными сексуальными контактами, соблюдением гигиены и правильным питанием.
Профилактика
Обычно реактивный артрит лечится за несколько месяцев, но суставные боли могут продолжаться длительное время.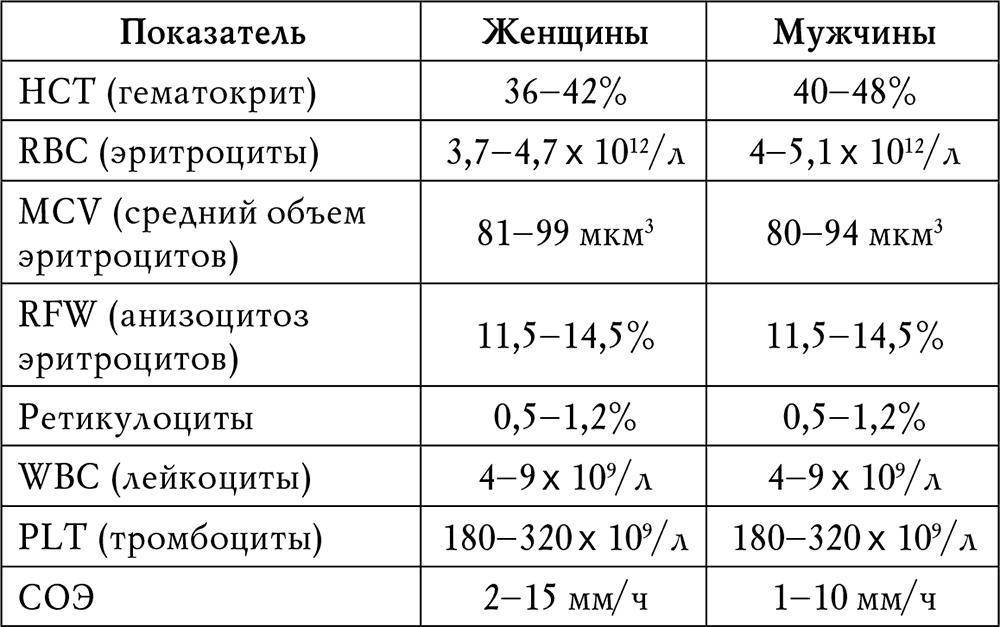 После венерической инфекции заболевание лечится труднее, чем после кишечной инфекции. У лиц, имеющих в наследственности антиген HLA- B 27, риск повторного заболевания повышен.
После венерической инфекции заболевание лечится труднее, чем после кишечной инфекции. У лиц, имеющих в наследственности антиген HLA- B 27, риск повторного заболевания повышен.
У некоторых больных реактивный артрит переходит в хроническую форму ревматизма спондилатропатию (болезнь Бехтерева), например, при ревматизме позвоночника.
14. РЕВМАТИЗМ ПОЗВОНОЧНИКА И БОЛЕЗНЬ БЕХТЕРЕВА
Ревматизм позвоночника – это длительное воспалительное заболевание позвоночника, иногда проявляющееся и в суставах конечностей. К тому же может вызывать воспаления в местах крепления сухожилий и в глазах. Иногда воспаление может быть в сердце или на стенках аорты. Ревматизм позвоночника относится к спондилатропатии.
Ревматизм позвоночника встречается одинаково часто как у мужчин, так и у женщин, но у мужчин заболевание протекает в более серьёзной форме. В большей части пациентами больницы являются мужчины. Почти все женщины, заболевшие ревматизмом позвоночника, не знают о своей болезни. Наследственность является фактором риска. В Финляндии около 10000 пациентов, страдающих ревматизмом позвоночника, нуждаются в лечении. Но по статистике больные ревматизмом позвоночника могут составлять один процент от общего населения.
В Финляндии около 10000 пациентов, страдающих ревматизмом позвоночника, нуждаются в лечении. Но по статистике больные ревматизмом позвоночника могут составлять один процент от общего населения.
Причины
Причины возникновения заболевания неизвестны, но одним из факторов является инфекционные заболевания. Ревматизм позвоночника может появиться после перенесёного реактивного артрита. У 95% заболевших ревматизмом позвоночника обнаружен наследственный антиген HLA-B27.
Симптомы
Молодой человек, который начинает просыпаться по ночам от болей в поясничной области, является типичным пациентом. Боль может отдавать в заднюю часть бедра. По утрам спина не гнётся, но небольшая зарядка облегчает боль. У половины пациентов также воспаляются суставы рук и ног, опухают колени, голени и бёдра. Иногда заболевание начинается с отёков суставов рук и ног, реже с воспаления глаз. Достаточно часто заболевание сопровождается болью грудной клетки.
Симптомы ревматизма позвоночника могут быть кратковременными. Иногда заболевание проявляется через какое-то время снова. Появляются боли в позвоночнике при наклоне вперёд. Между позвонками растут костные мосты. Меняется осанка, и уменьшается гибкость позвоночника. Также поражаются суставы рук и ног. Особенно страдают суставы бёдер, колен и плеч.
Иногда заболевание проявляется через какое-то время снова. Появляются боли в позвоночнике при наклоне вперёд. Между позвонками растут костные мосты. Меняется осанка, и уменьшается гибкость позвоночника. Также поражаются суставы рук и ног. Особенно страдают суставы бёдер, колен и плеч.
На следующей стадии заболевания у некоторых пациенов появляется воспаление глаз – ирити. Один или два из ста больных ревматизмом позвоночника в дальнейшем заболевают воспалением сердца.
Диагностика
В связи с тем, что боли в спине являются обычным явлением, диагноз ревматизм позвоночника очень легко пропустить. На начальной стадии заболевания гибкость позвоночника сохраняется в хорошой форме, но со временем спина немеет, и гибкость позвоночника ухудшается. Иногда диагноз ревматизма позвоночника можно поставить только через пять или даже десять лет после проявления первых симптомов заболевания.
Заболевание подтверждается рентгеновским снимком крестцового отдела позвоночника, на котором видны воспалительные изменения.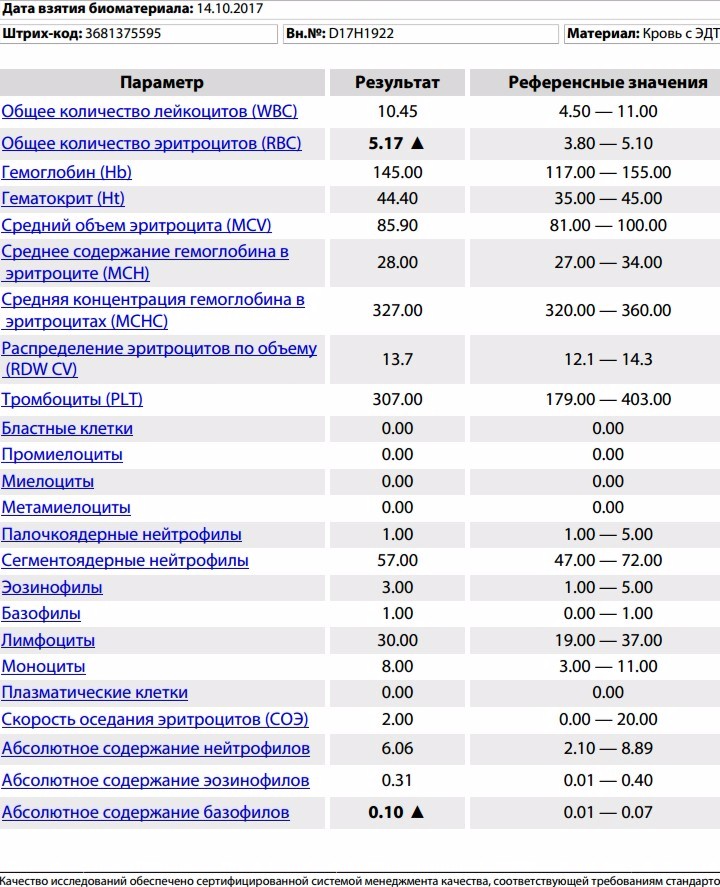 На ранних стадиях можно сделать магнитный снимок. Позже между позвонками видны костные мосты (синдесмофиты). В анализе крови отмечаются высокие показатели воспаления и низкий гемоглобин. В некоторых случиях анализ крови может быть нормальным. В крови нет ревматического фактора. Назначается исследование на наличие антигена HLA-B27.
На ранних стадиях можно сделать магнитный снимок. Позже между позвонками видны костные мосты (синдесмофиты). В анализе крови отмечаются высокие показатели воспаления и низкий гемоглобин. В некоторых случиях анализ крови может быть нормальным. В крови нет ревматического фактора. Назначается исследование на наличие антигена HLA-B27.
Лечение
Важным в лечении ревматизма спины является занятие физкультурой. Ревматизм поражает позвоночник, и формируется осанка с наклоном вперёд. Ежедневными занятиями спортом можно поддерживать хорошую осанку и гибкость позвоночника. Хотя бы раз в день нужно выпрямлять спину. Это можно сделать, подойдя стене, прижав к ней пятки, ягодицы и плечи. Грудную клетку можно поддерживать в хорошем состоянии, делая глубокие вдохи и выдохи. Желательно направить пациента на занятия физкультурой и объяснить, что нужно делать для поддержания тела в хорошой форме. Занятия с профессиональным инструктором особенно важно для молодых пациентов.
При лёгких формах заболевания назначаются болеутоляющие и противовоспалительные лекарства.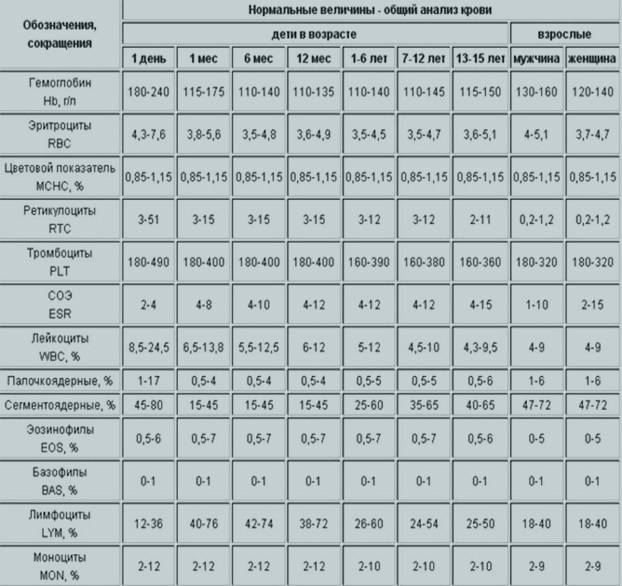 Сульфасалацин назначают для предотвращения развития заболевания в позвоночнике. Также назначаются и другие лекарственные препараты. Например, новые биологические антиревматические препараты, которые являются эффективными в лечении ревматизма. Если ревматизм поражает суставы бёдер и колен, то пациентам делают операции по протезированию суставов.
Сульфасалацин назначают для предотвращения развития заболевания в позвоночнике. Также назначаются и другие лекарственные препараты. Например, новые биологические антиревматические препараты, которые являются эффективными в лечении ревматизма. Если ревматизм поражает суставы бёдер и колен, то пациентам делают операции по протезированию суставов.
Боль и покраснение глаз может быть признаком воспаления, для этого рекомендуется консультация окулиста.
Профилактика
Хорошее лечение – это профилактика. Ревматизм позвоночника не лечится, но его можно предотвратить. Острый период заболевания редко проявляется у людей старше 40 лет. У большинства людей сохраняется рабочая способность, и только небольшая часть заболевших получает инвалидность.
15. НАСЛЕДСТВЕННОЕ ЗАБОЛЕВАНИЕ СОЕДИНИТЕЛЬНОЙ ТКАНИ
Соединительная ткань связывает все ткани в организме, она состоит из клеток, волокон, воды и межклеточного вещества. Волокна соединительной ткани – это белок или протеины, строение которых передаётся по наследству от отца и матери. Если в генах родителей была ошибка, то и в новом, рождённом гене тоже будет ошибка, что и приведёт к появлению заболевания.
Если в генах родителей была ошибка, то и в новом, рождённом гене тоже будет ошибка, что и приведёт к появлению заболевания.
Коллаген – это протеин организма. Это крепкие волокна, которые выдерживают растяжения. Сухожилия, связки и мышечные оболочки образуются из коллагена, также коллаген есть и в других тканях. Существует много видов коллагена. Коллаген I есть в костной ткани, коллаген II – в хрящевой ткани.
Эластин – это волокна, которые тянутся, как резина. Эластиновые волокна обвивают фибриллины так, как колготки в сеточку обвивают женскую ногу. Во всех протеиновых волокнах могут проявиться наследственные заболевания, вызванные ошибкой в генах.
Синдром Элерса-Данлоса (EDS)
В Финляндии около 1000 пациентов больны EDS- синдромом.
Причины
Причиной заболевания является наследственность. Если родители ребёнка больны синдромом Элерса-Данлоса, то вероятность болезни ребёнка возрастает на 50%. Но возможно, что поражённый ген одного из родителей так и не приведёт к заболеванию.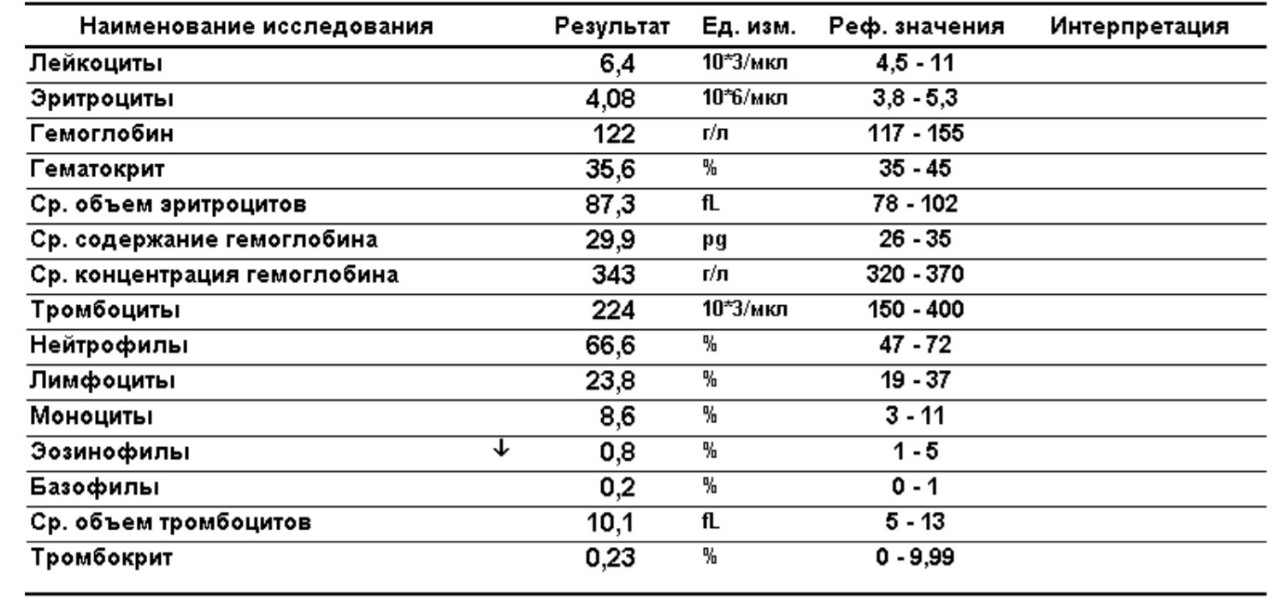 Если гены поражены у обоих родителей, то возможность заболевания ребёнка составляет один к четырём. Синдром Элерса–Данлоса – это группа наследственных заболеваний соединительных тканей, которая поражает кожу, суставы и кровеносные сосуды, вызывая их повышенную растяжимость. При этом синдроме в строении коллагенов присутствуют нарушения.
Если гены поражены у обоих родителей, то возможность заболевания ребёнка составляет один к четырём. Синдром Элерса–Данлоса – это группа наследственных заболеваний соединительных тканей, которая поражает кожу, суставы и кровеносные сосуды, вызывая их повышенную растяжимость. При этом синдроме в строении коллагенов присутствуют нарушения.
Симптомы
Симптомы заболевания разнообразны: легко повреждаемая эластичная кожа, гиперподвижные суставы, варикозное расширение вен, грыжи, разрывы стенок кровеносных сосудов, воспаление дёсен и выпадение зубов. Симптомы зависят от типа заболевания.
В восстановительном центре Апила организованы курсы для EDS-пациентов, где людям с данным заболеванием помогают справиться со своими трудностями и проблемами: боли, гибкость суставов, проблемы с зубами, мышечная слабость, синяки и кровотечения, медленное заживление ран и образование рубцов, проблемы кишечника, вывихи, усталость и отёчность. У женщин – предотвращение выкидышей.
Виды EDS-синдрома
В настоящее время EDS-синдром делится на разные формы заболевания.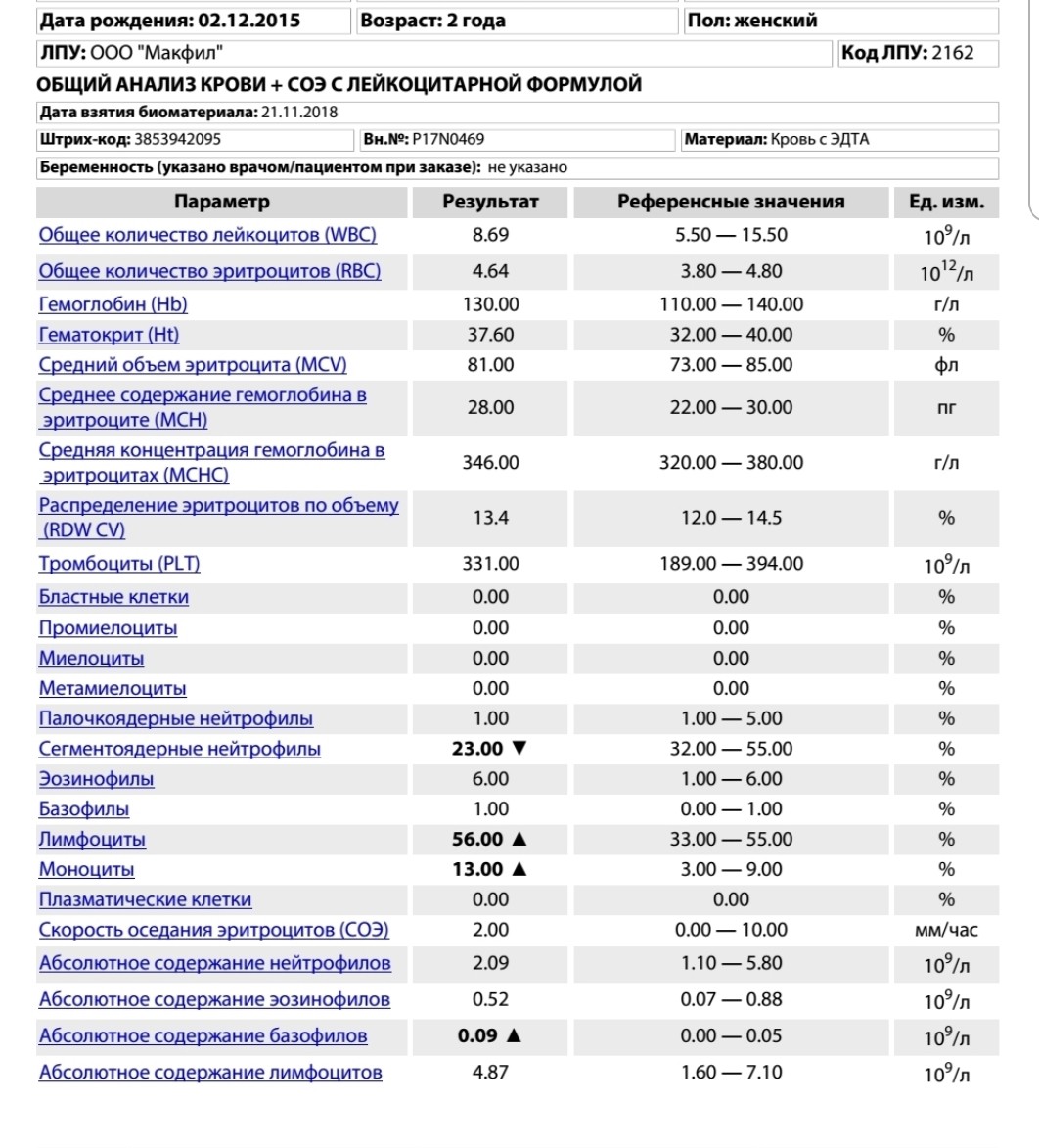
Сверхповышенная подвижность – гипермобильность (раньше тип III)
Основным симптомом гипермобильного типа является повышенная подвижность в крупных и мелких суставах, иногда вывихи и боли. Кожа тянущаяся и бархатистая. Заболевание может проявляется у родственников.
Классическая форма EDS (раньше формы I и II)
При классической форме заболевания у пациентов кожа мягкая и бархатистая, выраженная растяжимость кожи, склонность к повреждению при незначительной травме, а также к образованию кровоподтеков или гематом, рубцов, подкожных псевдоопухолей, повышенная подвижность в крупных и мелких суставах, частое варикозное расширение вен. У пациентов также встречаются паховые и диафрагмальные грыжи, синяки, мышечная слабость, геморои и воспаления дёсен. Заболевание является наследственным.
Сосудистая форма (раньше форма IV)
У пациентов эта форма заболевания проявляется гиперподвижностью суставов. Сосуды легко повреждаются, потому что стенки сосудов слабые, что является васкулитом , то есть воспалением стенок сосудов.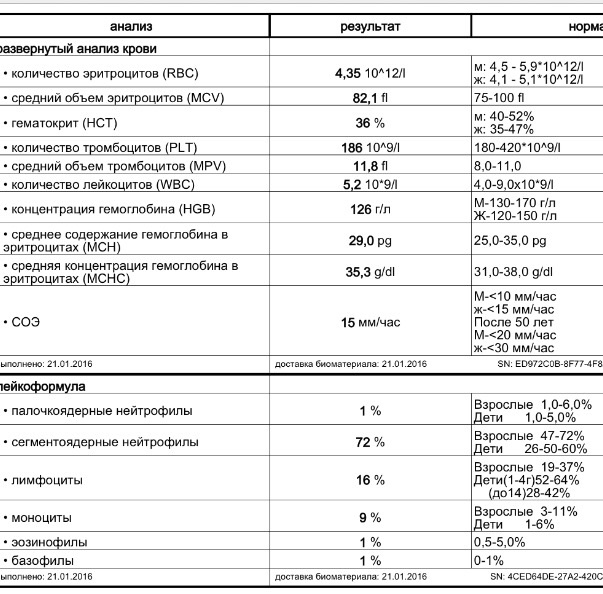
Кожа у этих людей тонкая, прозрачная с просвечивающими сосудами. Легко появляются синяки.
Кифосколиоз EDS( раньше тип VI)
Кифосколиоз является редким заболеванием, но в настоящее время поражённый ген тщательно исследуют. Этим заболеванием страдают около 60 человек на Земле. У них сильно выраженная мышечная слабость, которая приводит к неправильной осанке позвоночника – сколиозу. В некоторых случаях может быть повышенная ранимость глаз и утончение роговицы.
Артрохалазия тип EDS (раньше типы VII A и VII В)
В редкой форме артрохалазии типа EDS проявляются сильные изменения в соединительных тканях, которые ослабляют суставы, делают кожу легко повреждаемой, приводят к воспалениям суставов, ломкости костей и ортопедическим проблемам. На Земле болеют около 30 человек.
Дерматоспараксис EDS (раньше тип VII C)
Выраженная ранимость кожи и её повышенная эластичность. Создаётся впечатление, что кожи много. Распространено образование рубцов и грыж. Беременных женщины подвержены риску преждевременных родов из-за слабой оболочки плода.
Лечение
Изменить ген и устранить причину заболевания невозможно. Лечение направлено на уменьшение симптомов и предотвращение их ухудшения.
Важно определить причину заболевания и сообщить пациенту полную информацию о болезни. Зная о характере болезни, больной сам планирует свою жизнь так, чтобы болезнь не влияла на неё. Выбирая профессию, молодые люди должны принимать своё заболевание во внимание.
При болях в суставах можно принимать парацетамол и противовоспалительные препараты. При больших поражениях суставов делаются операции по имплонтации суставов.
Перед операцией EDS-пациентам нужно рассказать хирургу о своей болезни, чтобы избежать осложнений при заживлении ран.
В повседневной жизни EDS-пациентам могут помочь разные средства. Избегая опасных ситуаций, можно сохранить суставы целыми. На суставы можно надевать поддерживающие эластичные повязки. Мышцы нужно укреплять. Кожу надо увлажнять кремами. Рекомендуется ношение поддерживающих колготок и гольф для профилактики варикозного расширения вен.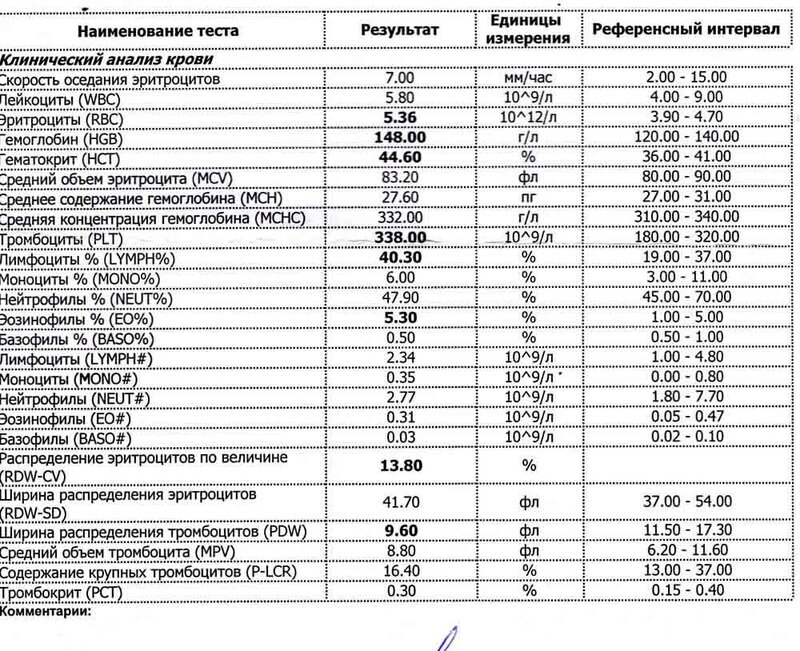 Постоянные посещения зубного врача помогут избежать проблем с зубами.
Постоянные посещения зубного врача помогут избежать проблем с зубами.
Пациенты сами знают, как важно получать информацию о характере заболевания. Спокойная жизнь, отдых и расслабление, а также поддержка близких помогают преодолеть жизненные трудности. Нужно избегать резких движений, использовать тугие повязки для суставов, систематически принимать лекарства, правильно питаться, попробовать Рэйки–лечение, йогу, зонатерапию и лимфомассаж. Стараться делать всё, что можешь и умеешь.
Другие повреждения строения коллагена
Синдром Стиклера является достаточно распространённым заболеванием, которое вызывается нарушением строения коллагена типа II. Заболевание часто проявляется в лёгкой форме. Синдром Стиклера — комплекс наследственных аномалий глаз и суставов. Первые симптомы появляются в детстве: врожденная выраженная близорукость, нередко слепота, в ослепшем глазу развиваются катаракта, вторичная глаукома, хронический увеит, кератопатия, сморщивание глазного яблока. Суставы становятся гиперподвижными, болезненными и предрасположены к переломам. В отдельных случаях отмечается нарушения в строении лица: маленький подбородок, расщепление челюстей.
В отдельных случаях отмечается нарушения в строении лица: маленький подбородок, расщепление челюстей.
Дисплазия соединительной ткани (MED) вызывана нарушением строения коллагена типа IX. Эти нарушения строений суставных хрящей ведут к задержке развития роста и разрушению суставов.
Остеогенезис имперфекта является заболеванием костей, вызванным мутацией коллагена типа I, которое может вызвать смерть зародыша ещё в матке. В лёгкой форме заболевания кости слабые и легко ломаются. Помимо этого могут быть проблемы в соединительной оболочке глаз, проблемы со слухом и глухота.
Другие генетические проблемы волокон протеина
Синдром Вильямса — синдром, возникающий как следствие хромосомной патологии эластина. Эластин и коллаген образуют волокнистый белок, с помощью которого стенки сосудов, лёгкие и другие органы способны растягиваться. Этим заболеванием болеет один ребёнок из 20000. У них появляются проблемы в сердечно-сосудистой системе. Аорта и лёгочная артерия суживаюся уже в детском возрасте, позже появляются проблемы с кровяным давлением. Дети рождаются маленького размера, появляются проблемы кормления, колики. Также появляются изменения строения зубов (большие промежутки между зубами), слабые мышцы, гиперподвижность суставов. У взрослых суставы менее подвижны.
Дети рождаются маленького размера, появляются проблемы кормления, колики. Также появляются изменения строения зубов (большие промежутки между зубами), слабые мышцы, гиперподвижность суставов. У взрослых суставы менее подвижны.
Синдром Марфана вызывается изменением фибриллина типа I. Фибриллин – это волокнистый белок.
В соединительной ткани он образует защитную сетку вокруг эластина. Помимо характерных изменений в органах опорно-двигательного аппарата (удлинённые кости скелета, гиперподвижность суставов), наблюдается патология в органах зрения и сердечно-сосудистой системе.
16. СИНДРОМ ШЕГРИНА
Синдром Шегрина является системным аутоиммунным заболеванием, характеризующимся сухостью слизистой глаз, рта и половых органов, вызванной поражением слёзных, слюнных и половых желез. Чаще всего болеют женщины. Синдромом Шегрина заболевают люди старше 50 лет. О заболевании нет достоверных сведений, но по оценкам специалистов 3-4% взрослых людей страдают синдромом Шегрина.
Причины
Основой механизмов развития болезни считаются аутоиммунные нарушения, при которых имунная система противостоит своим же тканям.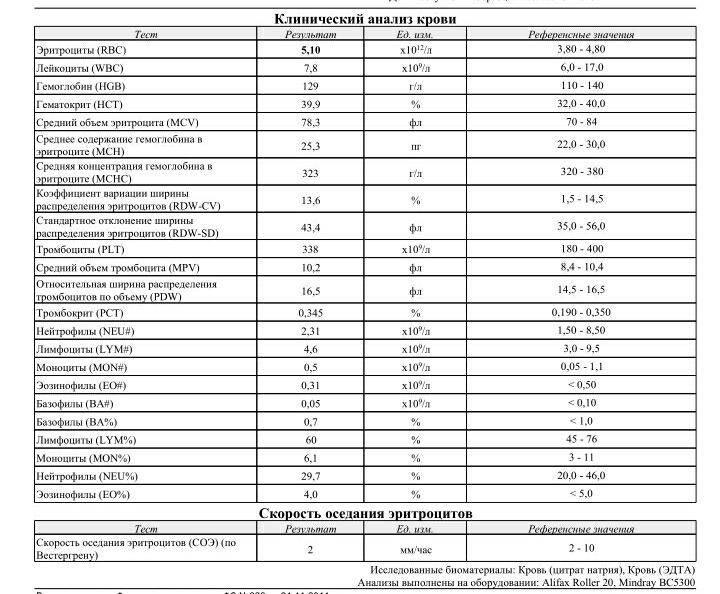 Синдром может развиваться самостоятельно (primaarinen) или вместе с другими ревматическими аутоимунными заболеваниями, в частности, суставным ревматизмом (sekundaarinen). Одной из причин заболевания считается изменение половых гормонов, потому что большей частью заболевших являются женщины.
Синдром может развиваться самостоятельно (primaarinen) или вместе с другими ревматическими аутоимунными заболеваниями, в частности, суставным ревматизмом (sekundaarinen). Одной из причин заболевания считается изменение половых гормонов, потому что большей частью заболевших являются женщины.
Симптомы
При синдроме Шегрина появляется сухость слизистых оболочек. Первыми признаками заболевания является раздражение и сухость в глазах. Появляется сухость во рту и трудности проглатывания пищи, возникает необходимость запивания еды. Садится голос. Из-за уменьшения слюноотделения, на зубах образуется кариес и воспаляются дёсны. Может возникнуть воспаление слюнных желёз. Сухость кожи вызывает зуд. Появляется сухость в носу и сухой кашель. У женщин появляется сухость слизистых половых органов. Нарушения работы желёз желудка и кишечника вызывает нарушения всасывания железа и витамина B12.
При синдроме Шегрина появляется усталость, боли в суставах напоминают фибромиалгию, появляются раздражения на коже и лихорадка.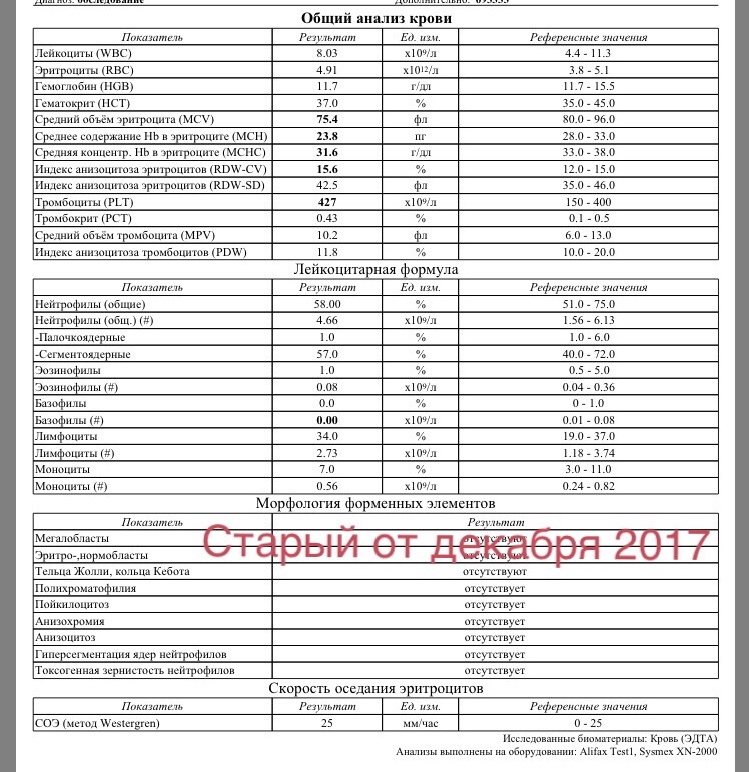 Возможны заболевания почек, отёк лимфатических желёз и нарушения со стороны нервной системы.
Возможны заболевания почек, отёк лимфатических желёз и нарушения со стороны нервной системы.
При синдроме Шегрина возрастает риск заболевания раком лимфатических желёз (лимфома). При сильном отёке лимфатических и слюнных желёз возникает необходимость в их обследовании.
Диагностика
Синдром Шегрина определяется по типичной для этого заболевания сухости слизистых оболочек. Слёзоотделение измеряется тестом Ширмера, при котором рассматривается скорость намокания впитывающей бумажки за нижним веком. Выделение слюнной жидкости измеряется сбором слюны. Микроскопическое исследование губ указывает на наличие воспалительного процесса. Показатели воспаления в крови повышены. Почти у всех пациентов в крови присутствует ревматический фактор синдрома Шегрина и антитела.
У пожилых людей сухость слизистых оболочек является возрастным показателем и не является симптомом болезни Шегрина.
Лечение
Если во вторичный синдром Шегрина входит ревматизм суставов или другое заболевание ревматизма, то оно лечится обычным способом.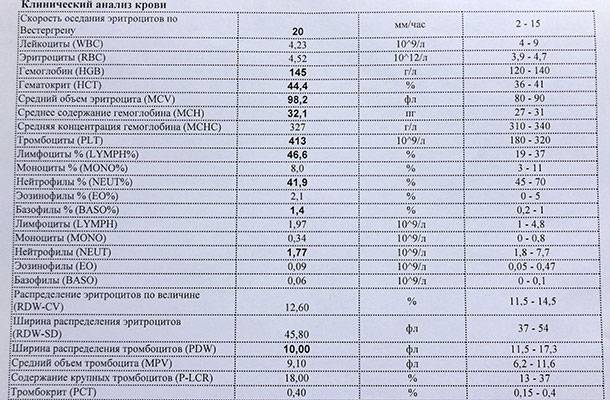 Нарушение работы желёз при синдроме Шегрина неизлечимо, но увлажнением можно облегчить сухость слизистых оболочек.
Нарушение работы желёз при синдроме Шегрина неизлечимо, но увлажнением можно облегчить сухость слизистых оболочек.
Увлажняющие капли для глаз и защитные очки предотвращают сухость глаз. Воздух в помещении не должен быть очень сухим. Увлажняющие капли закапывают регулярно через равные промежутки времени. Употребление жевательной резинки с ксилитолом, а также лекарственные препараты как пилокарпин и бромгексидин, увеличивают выделение слюны. Нужно следить за состоянием зубов. Грибковые инфекции рта и половых органов необходимо лечить противогрибковыми лекарствами. Женские половые органы обрабатываются специальными увлажняющими средствами.
Первичный синдром Шегрина лечится малыми дозами кортизона. В трудных случаях назначают метотрексат и другие новые ревматические лекарства.
Профилактика
Синдром Шегрина не лечится. Лечение замедляет развитие болезни, но с заболеванием нужно научиться жить. Инвалидность, вызванная болезнью, появляется редко. На профилактику больше влияет характер протекания первичного заболевания или ревматизма, чем сухость слизистых оболочек.
17. СЕРОНЕГАТИВНЫЙ СПОНДИЛОАРТРИТ
Спондилоартрит определяет группу заболеваний, точный диагноз не всегда можно определить. Речь идёт о серонегативном ревматизме позвоночника, при спондилоартрите в крови отсутствует ревматический фактор, но существует тенденция вызывать воспаления в суставах позвоночника.
К спондилоартритам относят:
ревматизм позвоночника (Spondylarthritis ancylopoetica, болезнь Бехтерева)
реактивное воспаление суставов и болезнь Рейтера
язвенное воспаление толстого кишечника и болезнь Кронина
часть детского ревматизма
суставной псориаз и воспаление позвонков
Все эти заболевания могут вызывать воспаления в суставах конечностей и позвоночника. Особенностью этих заболеваний является воспаление промежуточного сустава между крестцовой и подвздошной костью (сакроилит). При обследовании у больных обнаруживается наследственный антиген HLA-B27. Обычно эти заболевания развиваются в молодом возрасте, появляются воспаления глаз (ирит), сердца и стенок аорты. Одновременно все симптомы проявляются редко. В начале заболевания воспаления суставов приносят проблемы и боли, но в дальнейшем они могут исчезнуть даже без лечения.
Спондилоартрит проявляется как и другие ревматические заболевания. Возможно причиной является перенесённая кишечная или венерическая инфекция, как и при реактивном воспалении суставов. Большое значение имеет наследственный фактор.
Финны живут в холодном климате и наличие у них антигена HLA-B27 достаточно распространено. У 15% финнов присутствует антиген HLA-B27, тогда как у жителей центральной Европы всего у 8%, у японцев 1% и у индейцев Южной-Америки ещё меньше. У людей, в организме которых обнаружен антиген HLA-B27, риск заболеть спондилоартритом в сто раз выше, чем у других.
Спондилоартрит является длительным заболеванием, но он редко приводит к инвалидности. В лёгких формах заболевания пациент обходится небольшими дозами лекарственных препаратов. В трудных случаях назначаются биологические ревматические препараты.
18. СИСТЕМНЫЙ LUPUS ERYTEMATOSUS (SLE)
Системный lupus erytematosus (SLE) – это системное аутоимунное заболевание соединительной ткани. Организм вырабатывает антитела, которые вместо того чтобы защищать, наоборот нападают на соединительные ткани организма. Признаки заболевания проявляются в различных частях организма. В Финляндии насчитывается около 2000 заболевших SLE, 90% из которых женщины. Половина из них в возрасте до 30 лет. У пожилых людей заболевание протекает в лёгкой форме.
Причины
Причины заболевания неизвестны. У женщин в зрелом половом возрасте на заболевание влияют половые гормоны. Наследственность тоже влияет на заболевание. Некоторые лекарства (гидралазин, прокаинамид), химикаты и ультрафиолет увеличивают риск заболевания SLE.
Симптомы
Общими симптомами SLE- заболевания являются усталость, потеря веса и повышенная температура. На открытых частях тела появляются кожные высыпания, вызванные воздействием солнечных лучей. На лице вокруг носа появляется красная сыпь в форме бабочки. Боли и воспаление суставов, выпадение волос, язвы во рту, заболевания почек, воспаление оболочек лёгких и сердца, а также неврологические заболевания. Боли или ревматические воспаления в суставах проявляются почти у всех пациентов, кожные высыпания – у достаточно большой части заболевших, а заболевания почек – почти у половины. Суставы не разрушаются, но могут деформироваться. Симптомы заболевания у разных людей проявляются по- разному. Чаще заболевание протекает в лёгкой форме и не влияет на образ жизни заболевшего. Выявить форму заболевания достаточно сложно.
Диагностика
Диагноз заболевания ставится на основании симптомов и лабораторных исследований. Существует 11 критериев заболевания. Если в заболевании проявились 4 или более критериев, то диагноз системный lupus erytematosus поставлен верно. Подсчёт критериев имеет больше теоретическое значение. В анализе крови повышаются показатели воспаления, но как и при других заболеваниях ревматизма ЦРБ не повышен. Почти у всех пациентов в крови присутствуют антитела. По количеству и качеству антител можно оценить стадию болезни и результат лечения. Лейкоциты и тромбоциты могут быть понижены. Возможна анемия.
Лечение
При лёгких формах SLE- заболевания лечение не требуется. Заболевший сам заботится о себе, избегая солнечных лучей и пользуясь защитными кремами. Достаточно обойтись слабыми лекарственными препаратами, например, малыми дозами кортизона и гидроксиклорокина. В трудных случаях пациенту назначаются большие дозы кортизона.
Беременность может вызвать проблемы. О наблюдении и лечении SLE- заболевания во время беременности рекомендуется консультация врача–ревматолога. Инфекции также могут вызвать осложнения. Причину повышения температуры нужно обязательно выяснить, чтобы знать, чем она вызвана – инфекцией или обострением SLE-заболевания. Лечение направлено на поражённый орган. Почти всегда напоминает лечение остеопороза.
Профилактика
Профилактика системного lupus erytematosus постоянно развивается. Болезнь опасна для людей с серьёзными заболеваниями почек, лёгких или центральной-нервной системы. С возрастом болезнь затихает. SLE- заболевание, вызванное лекарственными препаратами, проходит при их отмене.
SLE- критерии:
1. Красная сыпь в форме бабочки на носу и щеках
2. Шелушащиеся покраснения на коже
3. Покраснения кожи под воздействием солнечных лучей
4. Язвы во рту
5. Воспаление суставов
6. Воспаление оболочек лёгких и сердца
7. Заболевания почек
8. Неврологическте симптомы (судороги или психозы)
9. Изменения крови (анемия, уменьшения лейкоцитов или тромбоцитов)
10. Иммунные изменения крови (DNA, ошибочно позитивный кардиолипини-тест)
11. Антитела
19. СИСТЕМНЫЙ СКЛЕРОЗ (СИСТЕМНАЯ СКЛЕРОДЕРМИЯ)
Системный склероз это ревматическое заболевание соединительных тканей. Одна из форм заболевания – склеродермия (склеро — твёрдый, дерма — кожа). При этом заболевании грубеет кожа. Также соединительная ткань внутренних органов рубцуется, но этот признак встречается редко. В Финляндии ежегодно заболевает 20-50 человек, из них большая часть женщины. Дети болеют редко.
Причины
Причины заболевания системным склерозом неизвестны, но заболевание могут вызывать многие химикаты. Например, в 1981 году в Испании прошла волна этого заболевания, вызванная некачественным растительным маслом. Некачественный триптофан, продаваемый как натуральный продукт, вызвал вторую эпидемию в конце того же десятилетия. Также угольная и кварцевая пыль, винилхлорид, триклоритилен и другие химикаты могут вызывать заболевание. Одной из подозреваемых причин являются силиконовые имплонтанты. У большинства больных причины заболевания неизвестны.
Симптомы
Заболевание начинается с нарушения кровообращения пальцев рук и ног. Появляется симптом Рейно, когда сосуды сокращаются так сильно, что пальцы становятся белыми при прохладной температуре окружающей среды. На пальцах рук появляются кожные изменения. Кожа пальцев набухает и уплотняется. Кожные морщины и складки пропадают. С годами кожа становится тонкой и натянутой, иногда в коже откладывается кальций. Симптомы могут распространяться и по всему телу, кожа уплотняется и деформируется. Мышцы лица становятся неподвижными, рот сокращается. Видны расширенные подкожные сосуды.
Склеродермия может поражать не только кожу, но и внутренние органы. При поражении пищевода появляются проблемы при глотании. При поражении лёгких, почек и кишечника появляются серьёзные проблемы со здоровьем. К этим заболеваниям относятся и такие необычные формы заболевания, как эозинофильный фаскит. Когда воспаление проходит, кожа рубцуется и напоминает апельсиновую кожуру.
Распространённой формой системного склероза является CREST (от calcinosis – закальцевание кожи), симптом Рейно, эсофагус (рубцевание пищевода), склеродактилия и телеагниэктазия, то есть расширение подкожных сосудов.
Диагностика
Диагноз ставится на основании картины заболевания. В крови пациента обнаруживаюся показатели ревматизма и антитела. При CREST обнаруживаются антитела, свойственные этому заболеванию.
Лечение
Лечение системного склероза трудное, потому что нет достаточно действенного лекарства. Пациенту надо защищать кожу от холода. Необходимо бросить курить. Назначаются сосудорасширяющие препараты (нифедипин). Для предотвращения сухости кожи используют увлажняющие крема. Для сохранения подвижности пальцев необходимо делать гимнастику для рук.
Ревматические лекарственные препараты тестируются, но их действие остаётся незначительным. Широко используются пенисилламин и циклоспорин. При лечении внутренних органов назначаются симптоматические лекарственные препараты.
Профилактика
Важным значением в профилактике системного склероза является ограничение заболевания на кожной стадии, когда другие органы ещё не поражены. Со временем кожа смягчается и заболевание переходит в лёгкую форму. Но поражение лёгких и почек остаётся серьёзным заболеванием.
20. ВАСКУЛИТ
Васкулит это воспаление стенок сосудов. Последствия васкулита зависят от количества поражённых сосудов и мест воспалений. В трудных случаях васкулит вызвает затруднения кровообращения. Это приводит к кровотечениям или омертвению тканей.
Васкулит классифицируется на основании размера поражённых сосудов. Васкулит поражает височную артерию, кожный васкулит малые кровеносные сосуды. При темпоральном артериите в стенке височной артерии под микроскопом видны большие и многоядерные клетки, из-за которых заболевание получило второе название – гигантоклеточный артериит.
Часто васкулиты проявляются редкими заболеваниями, как нодозный полиартериит. А также пурпура Шенлейна-Геноха, синдром Чарга-Штраусс, болезнь Кавасаки, гранулематоз Вегенера и артериит Такаяси.
Причины
Причинами заболевания могут быть инфекции, повреждения тканей, инородные вещества, которые вызывают иммунные реакции в организме. Механизм появления васкулита не определён. Наследственность тоже имеет значение. Васкулит может быть как самостоятельным заболеванием, так и относиться к группе ревматизмов, таких как суставной ревматизм или SLE-заболевание.
Симптомы
Васкулиту свойственны повышение температуры тела и потеря веса. Из-за заболеваний сосудов появляются кожные высыпания различного типа. Типичными симптомами заболевания являются мышечные и суставные боли, нарушения работы переферической нервной системы, носовые кровотечения, кашель с кровью, кровь в моче и боли в животе.
Особенности
У половины пациентов с диагнозом васкулит и темпоральный артериит проявляются симптомы полимиалгии. Симптомами артериита являются головные боли в височной области и боль в скулах при жевании. При заболевании возможен риск закупорки глазной артерии и потеря зрения, поэтому лечение необходимо начать как можно быстрее. В основном заболевают пожилые люди.
Болезнь Такаяси поражает аорту и исходящие из неё кровеносные сосуды. Основным симптомом заболевания является нарушение кровообращения. Поставить диагноз трудно. В основном заболевают молодые женщины.
Нодозный полиартериит является редким заболеванием, при котором на стенках артерий образуются воспалительные бляшки. Проявляется у молодых людей. Встречаются серьёзные изменения внутренних органов, диагноз выясняется в процессе операции.
Начальными симптомами гранулематоза Вегенера являются нарушения в верхних дыхательных путях, воспаление пазух носа, заложенность носа и носовые кровотечения. Также могут быть воспаления среднего уха и глухота, ослабление зрения. К сложным формам относятся поражения почек и лёгких. Некоторые формы заболевания протекают достаточно лёгко. В крови присутствуют ANCA-антитела.
При вторичном васкулите в сочетании с другими аутоимунными заболеваниями, симптомы начинаются с поражения мелких кожных сосудов. На коже голеней или рук образуются раны и некрозы.
Диагностика
Постановка диагноза осуществляется на основании симптомов заболевания и биопсии кожи. Рентген кровеносных сосудов (ангиография) выявляет васкулит. Также постановка диагноза опирается на лабораторные исследования. ЦРБ повышено.
Лечение
Лечение направлено на устранение причины возникновения васкулита. Сначала снимается воспаление кровеносных сосудов лекарственными препаратами. После его прекращения основное заболевание лечится эффективнее. Назначается кортизон. Часто вместе с ним применяют цитостатические средства. В критических ситуациях назначают большие дозы кортизона. Хорошие результаты дают биологические лекарственные препараты.
Профилактика
Прогноз васкулита улучшается с развитием методов лечения. У большой части пациентов симптомы улучшаются. Хотя иногда болезнь может перейти в тяжёлую форму. Обширные поражения внутренних органов дают плохой прогноз заболевания и срочную госпитализацию.
© 2016 Lappeenrannan reumayhdistys ry.
Скорость оседания эритроцитов — обзор
Повышенная скорость оседания
СОЭ повышается при большинстве бактериальных, микобактериальных и грибковых инфекциях и является нормальным или слегка повышенным при неосложненных вирусных, риккетсиозных и эрлихиальных инфекциях. Повышенное СОЭ (> 20 или> 30 мм / ч, в зависимости от исследования) имеет низкую дискриминирующую способность в качестве единственного теста (т.е. чувствительность и специфичность ≤50%) для прогнозирования бактериальной инфекции у детей с неспецифическими фебрильными заболеваниями кратковременной продолжительности. . 11–13 Среднее значение СОЭ при большинстве вирусных инфекций верхних дыхательных путей составляет примерно 20 мм / час (при 90% значений <30 мм / час), с примечательными исключениями, такими как при аденовирусных инфекциях, когда среднее СОЭ может составлять 40 мм / час. 12,14 Для пациентов с лихорадкой неизвестного происхождения нормальная или слегка повышенная СОЭ является предиктором возможного диагноза несерьезного или вирусного заболевания в> 90% случаев 15,16 ; СОЭ> 50 мм / ч у таких пациентов может быть стимулом для более тщательного обследования. 17,18
Изучена полезность СОЭ у детей с костно-суставными заболеваниями. 19 Несколько исследований детей с бактериальным артритом подтвердили, что СОЭ> 30 мм / час в 80–90% случаев (в среднем ~ 65 мм / час). 20–23 Проспективная проверка критериев Кохера (лихорадка ≥38,5 ° C, неспособность переносить вес, СОЭ ≥40 мм / час и количество лейкоцитов (лейкоцитов)> 12000 клеток / мм 3 ) для распознавания пиогенного артрита бедра от токсического синовита показала площадь под кривой рабочей характеристики приемника (ROC), равной 0.86. 21 В ретроспективной серии случаев в первичной специализированной больнице положительность всех 4 критериев Кохера в дополнение к С-реактивному белку (СРБ) ≥2 мг / дл имела прогностическую ценность только 60% для бактериального артрита, 22 и в сериях из США и Европы баллы Кохера были низкими у детей с артритом бедра Лайма и Kingella . 24,25 У детей с пиогенным артритом СОЭ часто повышается на 2–4 дни эффективной терапии, 19 , а СОЭ> 30 мм / час сохраняется по крайней мере в 50% случаев по завершении успешной терапии. 19,20 Пиковое значение СОЭ при остром остеомиелите обычно ниже, чем при бактериальном артрите (в среднем ~ 45 мм / час), с ожидаемым постепенным падением и нормальными значениями при соответствующем завершении терапии. 26 При подостром или хроническом остеомиелите СОЭ обычно слегка повышена (25–40 мм / час), но может быть нормальной.
Повышенное СОЭ характерно для многих неинфекционных воспалительных состояний, а также при невоспалительных состояниях, которые влияют на стеариновые свойства эритроцитов или объем плазмы, фибриноген, глобулины или концентрации белка (вставка 288.2). И наоборот, при инфекционных заболеваниях определенные условия могут привести к «ложному» занижению СОЭ. 27 СОЭ обычно превышает 30 мм / час во время эпизодов лихорадки у детей с периодической лихорадкой, афтозным стоматитом, фарингитом, синдромом аденита шейки матки (PFAPA) и другими симптомами аутовоспалительной периодической лихорадки. 28 СОЭ <50 мм / час не исключает болезнь Кавасаки, но делает диагноз маловероятным. 29 Внутривенная терапия иммуноглобулином вызывает резкое повышение СОЭ. 30,31
Несогласованные результаты между СОЭ и другими маркерами воспаления, особенно СРБ, могут указывать на инфекционные и неинфекционные заболевания. О низком СОЭ и высоком уровне СРБ сообщалось при болезни Кавасаки 32 и при тяжелом воспалительном заболевании кишечника 33 , тогда как высокое СОЭ при нормальном или слегка повышенном СРБ может быть ключом к основному аутоиммунному заболеванию или хронической вялотекущей инфекции.
Ставка SED — Фонд васкулита
Ноябрь 2010 г.
Персоналом клиники Мэйо
Определение
Скорость седиментации или скорость оседания эритроцитов (СОЭ) — это анализ крови, который может выявить воспалительную активность в организме.Тест на скорость седативного эффекта не является самостоятельным диагностическим инструментом, но его результаты могут помочь вашему врачу диагностировать или контролировать воспалительное заболевание.
Красные кровяные тельца или эритроциты (э-РИТ-ро-сайты) — это клетки, которые переносят кислород по всему телу. Когда кровь помещается в стеклянную пробирку, как часть теста на седимуляцию, эритроциты постепенно оседают на дно. Воспаление изменяет определенные белки красных кровяных телец, заставляя клетки слипаться. Поскольку эти скопления клеток более плотные, чем отдельные клетки, они относительно быстро оседают на дно.
Тест уровня седативности измеряет расстояние, на которое эритроциты падают в пробирку за один час. Расстояние косвенно измеряет уровень воспаления — чем дальше опускаются эритроциты, тем сильнее воспалительная реакция вашей иммунной системы.
Зачем это нужно
Ваш врач может назначить тест на уровень седативного эффекта, чтобы помочь поставить диагноз, оценить эффективность лечения или оценить тяжесть определенных воспалительных заболеваний.
Диагностика
Если у вас есть симптомы определенных воспалительных заболеваний, тест на уровень седативного эффекта может помочь вашему врачу обдумать диагноз.В прошлом тесты уровня седативности использовались чаще, чем сегодня, потому что доступны более конкретные измерения воспалительной активности. Сегодня этот тест чаще всего используют, если врач подозревает у вас одно из следующих заболеваний:
- Ревматоидный артрит, который вызывает воспаление слизистой оболочки суставов и приводит к боли, повреждению суставов и деформации суставов
- Ревматическая полимиалгия, воспалительное заболевание, вызывающее широко распространенные мышечные боли и скованность, в первую очередь в шее, плечах, плечах, бедрах и бедрах
- Гигантоклеточный артериит (ГКА), или височный или краниальный артериит, воспаление слизистой оболочки артерий, которое может вызывать головные боли, боли в челюсти, помутнение зрения или двоение в глазах
Мониторинг лечения
Если вы принимаете лекарства, например кортикостероиды, для лечения ревматоидного артрита или другого воспалительного заболевания, ваш врач может назначить тест на уровень седативного эффекта, чтобы контролировать эффект лечения.Хотя улучшение ваших симптомов, скорее всего, будет основным показателем эффекта лекарства, изменения уровня седативного эффекта могут помочь врачу отслеживать вашу реакцию на лечение.
Использование в отделениях неотложной помощи
Тест уровня седативности может использоваться в отделении неотложной помощи, чтобы добавить доказательства инфекционного или воспалительного состояния, такого как пневмония, аппендицит или другое острое воспалительное заболевание.
Как вы готовитесь
Показатель седативной нагрузки — это простой анализ крови.Вам не нужно голодать перед тестом, но вам следует избегать еды с высоким содержанием жиров, так как это может скрыть результаты теста.
Чего ожидать
Медсестра или фельдшер будет использовать иглу для забора крови из вены, скорее всего, из вены на руке. Сайт на вашей руке может оставаться болезненным в течение нескольких часов, но вы сможете вернуться к нормальной деятельности.
Результаты
Результаты теста на уровень седативного осадка будут указаны в миллиметрах (мм), на которые эритроциты опустились за один час.Нормальный диапазон составляет 0-22 мм / час для мужчин и 0-29 мм / час для женщин. Верхний порог нормального значения скорости седативного воздействия может несколько отличаться от одной медицинской практики к другой.
Результаты вашего теста на уровень седативного эффекта — это одна часть информации, которая поможет вашему врачу оценить ваше здоровье. Поговорите со своим врачом о том, что означают результаты вашего седативного эффекта в свете симптомов, которые вы испытываете, и результатов других диагностических тестов.
Точность результатов испытаний
Ряд условий может влиять на свойства крови, тем самым влияя на то, как быстро эритроциты погружаются в образец крови.Таким образом, информация о воспалительном заболевании — то, что ваш врач намеревается узнать из теста уровня седативного эффекта — может быть скрыта под влиянием других состояний. Эти усложняющие факторы включают:
- Беременность
- Диабет
- Болезнь сердца
- Анемия
Ваш врач примет во внимание возможные осложняющие факторы при интерпретации результатов вашего теста на уровень седативного эффекта.
Источник: Mayo Health Clinic.com, ноябрь 2010 г.
Скорость оседания эритроцитов и альбумин как маркеры воспаления связаны с показателями саркопении: поперечное исследование | BMC Geriatrics
Дизайн исследования
Когорта Центра гериатрии Амстердама (COGA) включает 572 пациента, которые были направлены в амбулаторную гериатрическую клинику Медицинского центра Университета VU в Амстердаме, Нидерланды, в период с 1 января 2014 г. по 31 декабря 2015 г. .Включение в исследование было основано на направлениях терапевтов из-за мобильности, когнитивных проблем или функционального снижения. Всесторонняя гериатрическая оценка была проведена гериатрической медсестрой, включая измерения физических и когнитивных способностей. После оценки последовала консультация гериатра. Образцы крови были собраны у 505 пациентов, из которых количество СОЭ, альбумина или лейкоцитов и по крайней мере один физический тест были доступны у 442 пациентов. Критерии исключения не применялись.Медицинский этический комитет Медицинского центра Университета VU одобрил исследование (номер ссылки 2017.582). Поскольку это поперечное исследование основывалось на регулярном уходе, необходимость в индивидуальном информированном согласии была исключена.
Характеристики пациента
Соответствующие характеристики, такие как возраст, пол, жизненный статус, образование, употребление алкоголя, курение, прием лекарств, история болезни, когнитивный статус, вес, рост и функциональный статус, были получены в вышеупомянутой комплексной гериатрической оценке.Использование противовоспалительных препаратов определялось как использование преднизона, преднизолона, метотрексата, месалазина, гидроксихлорохина, инфликсимаба или нестероидных противовоспалительных средств (НПВП). Медицинский анамнез, который считался болезненным, включал стенокардию, деменцию, депрессию, диабет 1 или 2 типа, сердечную недостаточность, гиперхолестеринемию, гипертонию, гипертиреоз, гипотиреоз, злокачественные новообразования, инфаркт миокарда, почечную недостаточность, остеопороз, болезнь Паркинсона, транзитную ишемическую атаку (ТИА) , инфаркт головного мозга, аритмии, протезирование сустава, заболевание суставов или обструктивная болезнь легких.Когнитивный статус проверялся с помощью краткого теста психического состояния (MMSE) [20]. Функциональный статус включал независимость в повседневной деятельности (ADL), измеряемую индексом Каца [21], причем более высокий балл указывал на большую зависимость, использование приспособлений для ходьбы, неподвижность более 1 недели в предшествующие 3 месяца, максимальное расстояние ходьбы и пережили падение в предыдущем году. Уровень гемоглобина в ммоль / л измеряли с использованием негемолизированной цельной крови с антикоагулянтом EDTA, анализируемой с использованием метода обнаружения лаурилсульфата натрия (SLS).SLS связывается с гемом, вызывая изменение цвета, которое измеряется фотометрически (Sysmex XN9000, Sysmex BV, Etten-Leur, Нидерланды).
Маркеры воспаления
СОЭ в миллиметрах / час (мм / час) измеряли с использованием негемолизированной цельной крови с антикоагулянтом ЭДТА, которую анализировали по методу Вестергрена (StaRRsed Auto Compact VERA109900, Mechatronics BV, Хорн, Нидерланды). Метод Вестергрена является эталонным методом Международного совета по стандартизации в гематологии (ICSH) [22].
Альбумин в г / л определяли в сыворотке крови с помощью колориметрического теста с бромкрезоловым пурпуром. Бромкрезоловый пурпурный избирательно связывается с альбумином, и изменение цвета измеряют фотометрически (серия модульных анализаторов Cobas 8000, Roche Netherlands BV, Верден, Нидерланды).
Количество лейкоцитов в E 9 / л измеряли с использованием негемолизированной EDTA-антикоагулированной цельной крови с помощью флуоресцентной проточной цитометрии (Sysmex XN9000, Sysmex BV, Etten-Leur, Нидерланды).
Измерения саркопении
Скорость походки оценивалась с помощью теста ходьбы на 4 метра в обычном темпе [23] и выражалась в метрах в секунду (м / с).Тест на время и вперед (TUG) как показатель функциональной подвижности [24], и тест на стойку в кресле (CST) как индикатор силы нижних конечностей [25] были выражены в секундах (с).
Сила захвата (HGS) измерялась ручным динамометром в положении стоя с вытянутой рукой (угол 180 градусов) (ручной динамометр Jamar, Sammons Preston, Inc., Болингбрук, Иллинойс) и выражалась в килограммах (кг). Использовалась максимальная сила захвата из шести попыток (три левых и три правых) [26].
Мышечную массу измеряли в положении стоя с помощью прямого сегментарного многочастотного анализа биоэлектрического импеданса (DSM-BIA; InBody 720; Biospace Co., Ltd., Сеул, Корея), который является проверенным инструментом для оценки состава тела [27 ]. Пациенты с кардиостимулятором или дефибриллятором были исключены из этого измерения. Из измерений DSM-BIA были извлечены два параметра: относительная масса скелетных мышц (RMM) в процентах, рассчитанная как [масса скелетных мышц в кг / вес * 100], и мышечная масса аппендикуляра (ALM), деленная на рост 2 в кг / м. 2 рассчитывается как [ALM / высота 2 ].Измерения DSM-BIA были доступны у 68 пациентов, поскольку эти измерения были добавлены к комплексной гериатрической оценке на более позднем этапе периода включения.
Статистический анализ
Для нормально распределенных переменных были представлены средние значения и стандартные отклонения (SD), для искаженных переменных медианы и межквартильные диапазоны (IQR), а для категориальных переменных — число и процент. Связи между независимыми переменными (СОЭ, альбумин и количество лейкоцитов) и зависимыми переменными (показатели саркопении) были проанализированы с использованием многомерной линейной регрессии.Результаты были представлены как β с 95% доверительным интервалом (95% ДИ) и значениями p ; уровень значимости был установлен на уровне α = 0,05. Перекошенные переменные (тест TUG и CST) были преобразованы в логарифм с использованием натурального логарифма. Логарифмически преобразованный β можно интерпретировать следующим образом: [(e β — 1). 100] равняется проценту изменения зависимой переменной с увеличением каждой единицы независимой переменной. Возраст, пол и количество заболеваний были определены как возможные искажающие факторы. Был проведен дополнительный анализ чувствительности, за исключением пациентов, принимавших противовоспалительные препараты ( n = 36).Был проведен второй дополнительный анализ, сравнивающий СОЭ, уровни альбумина и количество лейкоцитов у пациентов с низкими или нормальными показателями саркопении на основе пороговых значений определения EWGSOP2, с использованием анализов логистической регрессии с поправкой на возраст, пол и количество сопутствующих заболеваний. Для статистического анализа использовалась статистика IBM SPSS 25 для Windows. Для визуального представления были рассчитаны тертили СОЭ и построены гистограммы с использованием GraphPad Prism версии 7.00 для Windows, GraphPad Software, La Jolla California USA.
Симптомы, причины, лечение и тесты
Диагностика и тесты
Как диагностируется артрит?
Чтобы диагностировать артрит, врач изучает историю болезни и задает вопросы о боли пациента. Врач проведет физическое обследование, чтобы определить причины боли и то, как эта боль влияет на способность пациента функционировать.
Пациенту могут быть сделаны рентгеновские снимки или другие процедуры визуализации, такие как компьютерная томография (компьютерная томография) или МРТ (магнитно-резонансная томография), чтобы увидеть, насколько сильно повреждены суставы. Пациент также может обратиться к разным специалистам.
Какие анализы крови делают для диагностики артрита?
Пациентам с артритом, вероятно, будут сданы анализы крови при первом обращении к врачу и в рамках последующего лечения. Это связано с тем, что кровь является наиболее легко и безопасно отбираемой тканью тела, и она содержит следы материала из всех остальных частей тела.Наиболее распространенные анализы крови, используемые для диагностики и лечения артрита, включают следующие:
Общий анализ крови: Полный анализ крови (CBC) — это серия анализов крови, которые предоставляют информацию о различных частях крови, включая эритроциты, лейкоциты и тромбоциты. Автоматические машины быстро подсчитывают типы клеток. Результаты теста CBC могут помочь диагностировать заболевания, а также сказать, насколько серьезно заболевание. В нормальных условиях количество лейкоцитов составляет от 4000 до 11000.Высокое количество лейкоцитов может означать воспаление (отек), которое может быть вызвано ревматоидным артритом (РА). Однако инфекции, стресс и физические упражнения также временно повышают количество лейкоцитов. Общий анализ крови также измеряет гемоглобин , компонент красных кровяных телец, содержащий железо и переносящий кислород. Гематокрит — это процент от общего объема крови, который состоит из эритроцитов. Нормальные значения гематокрита составляют от 39% до 51% для мужчин и от 36% до 46% для женщин.Более низкий гематокрит может быть вызван рядом факторов или условий, включая РА.
Скорость оседания эритроцитов: Скорость оседания эритроцитов (СОЭ) — это тест, при котором образец крови помещается в пробирку, чтобы увидеть, как далеко оседают эритроциты за один час. Воспаление в организме производит белки в крови, которые заставляют красные клетки слипаться вместе и заставляют их падать быстрее, чем здоровые клетки крови. Поскольку воспаление может быть вызвано другими состояниями, кроме артрита, только анализ СОЭ не позволяет диагностировать артрит.
Ревматоидный фактор: Ревматоидный фактор (РФ) — это антитело, обнаруживаемое у многих пациентов с РА. Это один из нескольких методов, используемых для диагностики РА (80% пациентов с РА имеют РФ в крови, хотя другие воспалительные или инфекционные заболевания также могут быть причиной).
Антинуклеарные антитела: Пациенты с некоторыми ревматическими заболеваниями, такими как волчанка, вырабатывают антитела, направленные на ядра клеток организма. Эти антитела, известные как антинуклеарные антитела (АНА), обнаруживаются при просмотре сыворотки крови пациента (прозрачная жидкость, отделенная от крови) под микроскопом.Более 95% пациентов с волчанкой имеют положительный результат теста на АНА. Однако пациенты с другими заболеваниями также могут иметь положительные результаты теста на АНА, и даже у совершенно здоровых людей могут быть положительные результаты теста на АНА, поэтому перед постановкой диагноза необходимо выполнить другие тесты.
Ведение и лечение
Как лечится артрит?
Лечение артрита зависит от типа артрита, силы боли и общего состояния здоровья пациента.Цель состоит в том, чтобы вылечить все аспекты боли при артрите, увеличить подвижность (движение) и силу суставов, а также помочь пациентам научиться справляться с болью.
Варианты лечения включают лекарства, упражнения, тепло / холод, использование средств защиты суставов и хирургическое вмешательство. Планы лечения могут включать более одного из этих видов лечения. В рамках комплексного плана лечения артрита ваш врач может также назначить профессиональную и физиотерапию, которые могут оказать дополнительную помощь в вашем выздоровлении.
Как эрготерапевты могут помочь вам вылечить артрит?Эрготерапевты научат вас, как уменьшить нагрузку на суставы во время повседневной деятельности.Они могут показать вам, как изменить обстановку дома и на рабочем месте, чтобы уменьшить количество движений, которые могут усугубить артрит. Эрготерапевты также могут наложить шины на ваши руки или запястья и порекомендовать вспомогательные устройства, которые помогут вам водить машину, купаться, одеваться, вести домашнее хозяйство и выполнять другие задачи.
Как физиотерапевты могут помочь вам вылечить артрит?Вас могут научить физиотерапевты:
- Упражнения, предназначенные для сохранения подвижности, силы и использования суставов
- Правильная механика тела для перехода из одного положения в другое
- Правильная механика при выполнении повседневных дел
- Правильная осанка для защиты целостности суставов
- Как пользоваться вспомогательными средствами для ходьбы, такими как костыли, ходунки или трость, при необходимости
Пациентам с артритом коленного или голеностопного сустава от легкой до умеренной степени тяжести терапевт может порекомендовать функциональный ортез на колено или голеностопный сустав, который будет поддерживать ваш сустав, обеспечивая большую свободу в повседневных занятиях, таких как ходьба, походы и игра в гольф.
Каковы цели лечения артрита с помощью физиотерапии?Ваш физиотерапевт разработает программу в соответствии с вашими конкретными потребностями, независимо от того, распространены ли ваши артритические проблемы широко или ограничены одним суставом или областью тела.
Цели лечения:
- Предотвратить потерю работоспособности шарниров
- Восстановить способности, которые могли быть утеряны
- Поможет адаптироваться к новым уровням активности
- Поддерживайте свою физическую форму
- Поддерживайте свою способность принимать участие в выбранных вами занятиях с минимальной помощью других
Терапию следует начинать рано, чтобы уменьшить болезненные симптомы воспаления, предотвратить деформацию и постоянную жесткость суставов, а также сохранить силу в окружающих мышцах.Когда боль и отек лучше контролируются, планы лечения могут включать упражнения для увеличения диапазона движений, а также для улучшения мышечной силы и выносливости.
Какие терапевтические методы использования трудотерапии или физиотерапии для лечения артрита?- Упражнение . Это важная часть лечения артрита, которая наиболее эффективна, если делать ее правильно каждый день. Ваш терапевт назначит вам программу, которая будет меняться по мере изменения ваших потребностей.
- Температурные режимы . Прикладывание пакетов со льдом или грелок может помочь локально облегчить боль. Тепло помогает расслабить мышечные спазмы. Принятие теплой ванны или душа перед тренировкой может облегчить вам занятие.
- Терапия для пациентов с операциями на суставах . Предоперационные программы обучения и упражнений, начатые перед операцией в амбулаторном терапевтическом отделении, продолжаются дома. Они могут быть изменены в больнице после операции, чтобы соответствовать новым потребностям в период реабилитации.Эти упражнения могут быть добавлены к вашему обычному режиму упражнений, и вы можете обнаружить, что ваша способность выполнять упражнения улучшилась после операции.
- Способы защиты суставов . Вы можете уменьшить нагрузку на суставы, пораженные артритом, занимаясь повседневными делами.
- Некоторые способы сделать это:
- Терапевт может показать вам, как выполнять повседневные задачи, не усиливая боль и не вызывая повреждения суставов. Вам могут помочь методы совместной защиты:
- Используйте надлежащую механику тела, чтобы садиться и выходить из машины, стула или ванны, а также для подъема предметов.
- Вспомогательные устройства . Многие вспомогательные устройства были разработаны, чтобы упростить деятельность и снизить нагрузку на суставы и мышцы. Психотерапевт порекомендует устройства, которые будут полезны при выполнении задач, которые вы могли решить дома или на работе. Несколько примеров полезных приспособлений: стул для ванны в душе или ванне; поручни вокруг унитаза или ванны; рожки для обуви и захваты для носков с длинной ручкой. Ваш терапевт может направить вас к каталогам, которые предлагают широкий выбор вспомогательных устройств, которые вы можете заказать.
- Функциональная фиксация : В некоторых случаях легкой и средней степени артрита коленного и голеностопного сустава фиксация может улучшить стабильность, разгрузить болезненный сустав и повысить комфорт при таких действиях, как ходьба, лестница и такие развлекательные мероприятия, как игра в гольф и походы.
Программы физиотерапии могут включать:
- Упражнения, направленные на восстановление нормальной подвижности или гибкости суставов
- Упражнения, направленные на восстановление нормальных сил
- Информация о том, безопасно ли вам ходить со вспомогательным устройством или без него
- Постуральное обучение и модификации активности для облегчения дискомфорта и улучшения работоспособности
- Оценка функциональной фиксации пораженного сустава
Жить с
Что я могу сделать, чтобы облегчить жизнь с артритом?
Одеваться, чистить зубы, есть — вы делаете это каждый день.Но люди с артритом часто борются с этой повседневной деятельностью.
Часто простые настройки упрощают управление этими задачами, и существует целый мир адаптивных продуктов, предназначенных для людей с артритом. Начните со следующих советов, чтобы упростить распорядок дня.
На кухне
Открыть: Если у вас артрит, открыть банку сложно. В легких случаях резиновое покрытие для открывания банки помогает улучшить сцепление. Если это не помогает, подумайте о покупке специального открывателя для банок, банок и других емкостей.
Держите под рукой: Если вы любите готовить, кастрюли и сковороды с мягкими ручками и более длинными ручками могут облегчить процесс. Точно так же, если у вас возникнут проблемы с использованием столового серебра, адаптивная посуда с более толстыми ручками облегчит приготовление домашних блюд.
В ванной
Поднимите сиденье: Для многих, особенно тех, у кого проблемы с коленями, бедрами и спиной, ходить в туалет и выходить из него — ежедневная задача. Решения варьируются от высоких сидений, которые увеличивают высоту унитаза, до подъемников с электроприводом, если вам нужна дополнительная помощь.
Go electric: Электрические зубные щетки имеют более толстые ручки, которыми легче пользоваться, чем у традиционных. Они также выполняют большую часть работы по чистке зубов, что полезно, если у вас проблемы с плечом. Точно так же электрические бритвы облегчают бритье и могут уменьшить порезы и порезы, которые вы получаете от бритья больными, неустойчивыми руками.
Shower smart: Если у вас проблемы с входом и выходом из душа или вы боитесь упасть, попробуйте установить перила или использовать регулируемое кресло для душа.Также могут помочь другие, более простые изменения. Например, с жидким мылом обращаться легче, чем с брусками. Вы даже можете добавить в свой душ автоматический дозатор.
Попробуйте альтернативные варианты протирки: Никто не хочет говорить о гигиене туалета, но это важно. Пациенты часто говорят мне, что артрит мешает им правильно вымыться, что приводит к раздражению. Одна альтернатива: купите свернутый хлопок и отломайте кусочки для протирания. Хлопок на ощупь более приятный на ощупь, чем туалетная бумага, и вы можете увлажнить его для лучшей очистки.Только помните: не смывайте его, иначе вам придется заняться водопроводом.
В гостиной
Укрепите свое сиденье: Это большое удобное кресло может выглядеть привлекательно, но оно может принести больше вреда, чем пользы. Например, слишком мягкий стул усугубляет симптомы со стороны спины. А когда вы опускаетесь в кресло, вставать труднее. Купите устойчивый стул, достаточно высокий, чтобы вы легко садились и вылезали из него. При необходимости кресла с электроприводом могут поднять вам настроение.
Добавьте дверные ручки: Если поворачивать традиционные закругленные дверные ручки сложно, подумайте о приобретении переходников.Они устанавливаются на дверные ручки и включают в себя рычажный механизм, который требует только нажатия, а не поворота.
В раздевалке
Наденьте обувь: Для многих моих пациентов надевание обуви — самая сложная часть при одевании. Крошечные традиционные рожки для обуви не годятся. Но, как и садовые и чистящие инструменты, вы можете купить рожки с длинными ручками (от двух до трех футов). Использование этих длинных ручек избавляет от необходимости сгибаться и бороться.
Застежка-молния: Поскольку застежки-молнии и пуговицы на одежде такие маленькие, с ними трудно маневрировать, если вы имеете дело с опухшими и воспаленными суставами.Подумайте о покупке универсального инструмента для перевязки, который поможет застегнуть молнии и даже застегнуть пуговицы на место.
Как мне справиться с болью в руках?
Поскольку боль в руках затрудняет выполнение повседневных задач и действий, вам нужны практические способы прожить день. Помимо лечения, вы можете принять меры самостоятельно — с помощью экспертов — чтобы контролировать свое состояние.
Воспользуйтесь таймингом
Боль в руке зависит от типа артрита.
Например, люди с остеоартритом, как правило, испытывают боль, которая усиливается с каждым днем. Если это относится к вам, постарайтесь быть более активными по утрам. Пораньше займитесь садоводством или работой в саду, а также другими делами, требующими тяжелого ручного труда. Запланируйте утреннюю игру в футбол или теннис. В результате вы почувствуете себя лучше и станете работать лучше.
Люди с ревматоидным артритом или другими воспалительными заболеваниями могут чувствовать противоположное. Они обычно просыпаются окоченевшими. По прошествии дня они расслабляются.Если это относится к вам, отложите свои занятия на послеобеденное время и вечером, когда будете чувствовать себя лучше.
В любом случае не переусердствуйте. Людям с артритом спортивное клише «игра через боль» предлагает рецепт от травм.
Получите совет специалиста по адаптации
Никогда не недооценивайте свою способность адаптироваться. Но также не стоит недооценивать способность эрготерапевта (ОТ) помочь вам адаптироваться.
Например, ОТ может предложить упражнения, предназначенные для усиления вашего захвата, снижения уровня боли и увеличения диапазона движений.Все три критичны.
OT также может помочь вам настроить то, как вы взаимодействуете с повседневными предметами в вашем доме или офисе, а также со спортивным снаряжением. Например, некоторые люди с серьезными проблемами с большим пальцем меняют способ хвата лыжных палок, чтобы уменьшить нагрузку на большие пальцы.
Ваше хобби может быть другим, но цель работы с ОТ остается той же: помочь вам быть максимально активным и независимым.
Обнимите лед и тепло
Во-первых, лед. Ледяной массаж творит чудеса при боли, вызванной физической нагрузкой.Возьмите кусок льда и круговыми движениями потрите им болезненный сустав. Только не делайте этого больше пяти минут за раз, чтобы не вызвать раздражение кожи. Вы также можете использовать пакет со льдом с крышкой.
Что касается жары, то купание в теплой воде приносит облегчение. Фактически, некоторым людям с ревматоидным артритом так нравится ощущение теплой воды, что они даже мыть посуду вручную в раковине, чтобы хорошо впитать. Просто помните, что тепло не всегда помогает при острой травме.
Ищите специализированные инструменты
С помощью ОТ или врача — или таких групп, как Arthritis Foundation, — вы можете найти адаптивные инструменты, облегчающие боль в руке.
Например, если у вас возникли проблемы с обычными инструментами, поищите кухонную утварь и садовые инструменты со специальными более толстыми ручками.
В офисе можно заказать специальные клавиатуры для компьютеров, удобные для рук, а также гарнитуры громкой связи для разговоров по телефону. Вы даже можете приобрести специальные адаптеры для пера, которые упрощают нанесение чернил на бумагу.
То же самое и с физической активностью. Для гольфа, тенниса или других видов спорта, в которых интенсивно используются руки, специальные ручки могут иметь большое значение.Перчатки также рекомендуются для всех видов деятельности. Они уменьшают трение, а обеспечиваемое ими сжатие может облегчить симптомы. Перчатка для гольфа может помочь, например, в игре в теннис, даже если к ней нужно привыкнуть. И хотя садоводы любят чувствовать землю, защита и дополнительные перчатки очень важны.
То, что работает для вас, может не сработать для кого-то другого, поэтому для поиска облегчения может потребоваться небольшое экспериментирование. Но не бойтесь просить помощи у ОТ или врача.Ваши руки слишком важны для вашей повседневной жизни.
Как мне бороться с артритом, влияющим на мою половую жизнь?
Есть способы преодолеть препятствия на пути к артриту. Они требуют терпения, готовности пробовать новое и честности с партнером. Но секс — важная и здоровая часть жизни. Обычно польза стоит дополнительных усилий.
Попробуйте новую позицию
Боль — главный симптом артрита. К сожалению, это также одно из основных препятствий для секса.
Иногда небольшое изменение в вашем распорядке дня — например, попытка новой позы — может иметь большое значение. Несколько примеров:
- Если артрит бедер делает пребывание внизу слишком болезненным, переключитесь на верх.
- Если ваша основная проблема — боль в пояснице, попробуйте использовать подушки, чтобы поддержать спину и уменьшить дискомфорт.
- Если колени — ваши болевые точки, попробуйте позы, которые снимут с них стресс. Например, это может означать, что вы находитесь внизу.
- Если другие позы создают нагрузку на ваши больные суставы, попробуйте позу «ложкой», когда вы и ваш партнер лежите на боку.
Для людей с артритом «смешивание вещей» — это больше, чем просто разнообразие. Это практично. Чтобы найти подходящую позу, потребуется время и эксперименты.
Выберите лучшее время для секса
Боль — один из факторов. Другое дело — усталость. Есть определенное время дня, когда вы можете чувствовать себя слишком истощенным для секса. И хотя большинство лекарств от артрита не влияют на половую функцию, такие препараты, как метотрексат (от ревматоидного артрита), могут усилить вашу усталость.
Планирование может помочь. Чувствуете ли вы себя наиболее отдохнувшим и бодрым утром или днем? У вас самый низкий уровень боли через несколько минут после приема противовоспалительного средства? Сделайте это своими окнами возможностей. Перед сном — не единственное время для секса, особенно если именно в это время вы чувствуете себя хуже всего.
«Но секс лучше, когда он спонтанный», — подумаете вы. Это романтическая идея, но не всегда правда. Парам часто приходится работать, чтобы поддерживать здоровую сексуальную жизнь в долгосрочной перспективе.Поиск творческих решений для боли и усталости — лишь часть этой работы.
Обсуди это со своим партнером
Если вы не говорите о сексе, вы не можете над этим работать.
Не все проблемы, связанные с артритом, являются физическими. У вас может быть депрессия. Вы можете чувствовать себя менее привлекательным, чем раньше. Не держите эти вопросы при себе.
Если вам сложно разговаривать, подумайте о том, чтобы пригласить вашего партнера на прием и позволить своему врачу начать разговор.В некоторых случаях консультирование пар может помочь вам справиться с проблемами в отношениях, которые сопровождаются хронической болью.
Открытость и честность могут привести к творческим решениям. Например, если половой акт слишком болезненен, использование игрушек для взрослых или другие формы близости, такие как массаж, предлагают альтернативу. Вы никогда не узнаете, если не начнете разговор.
Решение связанных проблем
Иногда ревматоидный артрит доставляет не только боль и усталость, но и физические проблемы.Примерно от 15% до 20% пациентов с ревматоидным артритом также страдают синдромом Шегрена, который приводит к сухости в некоторых частях тела, включая влагалище.
У женщин с синдромом Шегрена половой акт обычно вызывает боль. Личные смазки могут иметь огромное значение. Только не забудьте проверить этикетку на наличие пропиленгликоля. Этот ингредиент вызывает у некоторых людей раздражение.
Если усталость — ваша самая большая проблема, вам могут помочь изменения в образе жизни. Исключите продукты высокой степени очистки, так как они могут вызвать воспаление.Ешьте больше свежих фруктов и овощей, чтобы повысить уровень питательных веществ. Добавьте в свой еженедельный распорядок легкие упражнения. Не сжигайте свечу с обоих концов, потому что отдых очень важен.
Эти советы полезны для здоровья любого человека. Но людям с артритом они могут помочь повысить энергию, необходимую для всех жизненных занятий, включая секс.
% PDF-1.4 % 21 0 объект > эндобдж xref 21 74 0000000016 00000 н. 0000002174 00000 п. 0000002291 00000 н. 0000002851 00000 н. 0000002897 00000 н. 0000003032 00000 н. 0000003167 00000 н. 0000003301 00000 п. 0000003435 00000 п. 0000003962 00000 н. 0000004272 00000 н. 0000005010 00000 н. 0000005642 00000 н. 0000006354 00000 п. 0000006989 00000 н. 0000007035 00000 н. 0000007148 00000 н. 0000007259 00000 н. 0000007372 00000 н. 0000007877 00000 н. 0000008426 00000 н. 0000008528 00000 н. 0000008952 00000 н. 0000009458 00000 п. 0000010459 00000 п. 0000011390 00000 п. 0000012184 00000 п. 0000012322 00000 п. 0000012934 00000 п. 0000013615 00000 п. 0000014505 00000 п. 0000015295 00000 п. 0000016050 00000 п. 0000016481 00000 п. 0000016585 00000 п. 0000017013 00000 п. 0000017493 00000 п. 0000018308 00000 п. 0000018449 00000 п. 0000019287 00000 п. 0000019455 00000 п. 0000020160 00000 п. 0000024058 00000 п. 0000039147 00000 п. 0000042280 00000 п. 0000045270 00000 п. 0000045325 00000 п. 0000045394 00000 п. 0000045503 00000 п. 0000053050 00000 п. 0000053338 00000 п. 0000053685 00000 п. 0000053710 00000 п. 0000054208 00000 п. 0000054312 00000 п. 0000055431 00000 п. 0000055775 00000 п. 0000056136 00000 п. 0000056245 00000 п. 0000060437 00000 п. 0000060961 00000 п. 0000061531 00000 п. 0000061639 00000 п. 0000069763 00000 п. 0000070221 00000 п. 0000070736 00000 п. 0000073061 00000 п. 0000073418 00000 п. 0000073838 00000 п. 0000074567 00000 п. 0000074649 00000 п. 0000074731 00000 п. 0000074813 00000 п. 0000001776 00000 н. трейлер ] / Назад 260136 >> startxref 0 %% EOF 94 0 объект > поток hb«a`Oe`g` Ā
Острый миелоидный лейкоз — Консультант по терапии рака
ОБЗОР: Что нужно знать каждому практикующему врачу
Острый миелоидный лейкоз (ОМЛ) — это форма рака крови, характеризующаяся клональной экспансией злокачественных миелоидных бластов в костном мозге, крови или других тканях.Первоначальный диагноз и лечение ОМЛ должны рассматриваться как неотложная медицинская помощь, и лучше всего их проводить в специализированном лечебном центре детской онкологии.
Вы уверены, что у вашего пациента острый миелоидный лейкоз? Каковы типичные признаки этого заболевания?
У большинства детей с ОМЛ наблюдается целый ряд симптомов, связанных с инфильтрацией костного мозга лейкозными бластами. Дополнительные симптомы могут быть вызваны инфильтрацией других тканей.Многие симптомы носят общий и относительно неспецифический характер. Не у всех пациентов будут все симптомы, но типичными являются следующие:
У большинства пациентов наблюдаются лихорадка, усталость и / или боль в костях.
Боль в костях, артралгия и / или артрит могут проявляться снижением активности, общей суетливостью, раздражительностью или отказом от ходьбы. Длинные кости, в которых костные полости заменяются миелобластами, часто поражаются сильнее; однако общая боль в костях и дискомфорт являются обычным явлением.
Потеря веса, если она присутствует, обычно относительно легкая, но анорексия встречается часто.
Кровотечения из-за тромбоцитопении — обычное явление. Часто возникают синяки и петехии. Часто лица, осуществляющие уход, замечают «сыпь» или «красные пятна», которые на самом деле являются петехиями. Кровотечение центральной нервной системы (ЦНС), забрюшинное кровотечение, тяжелое желудочно-кишечное кровотечение или геморрагический инсульт — редкие, но опасные для жизни осложнения. Риск серьезных кровотечений особенно высок у пациентов с впервые диагностированным острым промиелоцитарным лейкозом (APL; M3 по французско-американско-британской классификации [FAB]), у которых тромбоцитопения часто сопровождается диссеминированной внутрисосудистой коагулопатией.
Анемия может проявляться бледностью, головной болью, утомляемостью, головокружением, снижением энергии или толерантности к физическим нагрузкам, а иногда и обмороком.
Гепатомегалия и / или спленомегалия, возникающие в результате лейкемической инфильтрации, присутствуют у многих пациентов при постановке диагноза, но часто игнорируются.
Лимфаденопатия чаще встречается при остром лимфобластном лейкозе (ОЛЛ), чем при ОМЛ, но может возникать при любом из них.
Редким, но важным проявлением ОМЛ является компрессия спинного мозга, которая возникает в результате хлоромы (солидной опухоли, возникающей в результате локальной пролиферации миелобластов) в параспинальной / эпидуральной области.Хлоромы встречаются примерно у 10% пациентов с ОМЛ. Они могут возникать в любом месте тела, но чаще всего в коже или костях. Они особенно распространены в случаях с транслокацией t (8; 21) с морфологическим подтипом FAB M2, но также распространены у пациентов с подтипами FAB M4 и M5.
Поражение ЦНС встречается примерно у 5% пациентов с ОМЛ, причем более высокая частота встречается у пациентов с ОМЛ с моноцитарной дифференцировкой (классификация FAB M4 или M5), особенно при высоком уровне лейкоцитов (WBC).В большинстве случаев поражение ЦНС протекает бессимптомно, но иногда у пациентов наблюдаются головные боли, менингизм или паралич черепных нервов.
Гиперлейкоцитоз становится потенциальной клинической проблемой, когда количество лейкоцитов превышает 100 000 / мкл. Циркулирующая кровь может стать гипервязкой с заметно повышенным содержанием лейкоцитов, что приводит к застою крови в головном мозге, легких, почках и других органах, что проявляется дыхательной недостаточностью / гипоксией, нарушением сознания / инсультом и почечной недостаточностью.
Не все пациенты с ОМЛ имеют высокое количество лейкоцитов. Даже незначительные отклонения в общем анализе крови могут указывать на лейкемию. Они могут включать небольшое увеличение или уменьшение количества лейкоцитов или некоторое подавление в любой или всех линиях эритроцитов, лейкоцитов и тромбоцитов. Панцитопения может быть тонкой или более глубокой. Практически все пациенты с ОМЛ имеют одно или несколько отклонений в общем анализе крови.
Лейкозные бласты могут отсутствовать в мазке периферической крови, и только аспират костного мозга и / или биопсия могут подтвердить диагноз в этой ситуации.Световой микроскопии недостаточно для получения конкретной диагностической информации, хотя в большинстве случаев она может отличить ОМЛ от ВСЕГО. Во многих случаях для подтверждения диагноза и фенотипа требуются специальные окрашивания и лабораторные методы. Дополнительные анализы с проточной цитометрией и цитогенетическими методами (как традиционными, так и молекулярными) необходимы для дальнейшей классификации различных подмножеств AML и надлежащего планирования лечения.
У некоторых детей с новым диагнозом ОМЛ наблюдается синдром лизиса опухоли, нарушение обмена веществ, вызванное высвобождением внутриклеточного содержимого перед лицом гибели клеток, вызванной быстрым обновлением клеток.Наиболее частые результаты можно увидеть на стандартных химических панелях, в том числе повышение уровней калия, фосфора и мочевой кислоты, что может привести к вторичной гипокальциемии и повреждению почек с повышенными уровнями азота мочевины в крови и креатинина. Также может быть повышен уровень трансаминаз.
Какое другое заболевание / состояние имеет некоторые из этих симптомов?
Многие дети, которым в конечном итоге был поставлен диагноз AML, были обследованы по другим причинам их симптомов. Обычно пациенты могут быть обследованы на предмет рецидивов лихорадки, утомляемости, аденопатии, спленомегалии, гепатомегалии, потери веса и боли в костях.
Чаще всего при дифференциальной диагностике учитываются инфекционные заболевания и ревматологические состояния.
Инфекции, особенно вирусные заболевания, не только имитируют физические симптомы и признаки, но также могут иметь повышенное количество лейкоцитов или какой-либо элемент панцитопении, а также повышенную скорость оседания эритроцитов (СОЭ) или уровень С-реактивного белка (СРБ), поскольку Что ж.
Боль в суставах, лихорадка, гепатоспленомегалия и бледность являются общими признаками как при системном ювенильном ревматоидном артрите (JRA), так и при лейкемии.Следует рассмотреть возможность проведения аспирации костного мозга для исключения лейкемии перед лечением стероидами при подозрении на системный JRA.
Меньший процент пациентов обращается к ортопедам из-за рецидивирующей лихорадки и боли в костях, а часть пациентов фактически лечится от остеомиелита из-за этих симптомов, когда рентгенологическое изображение показывает костные аномалии, которые ошибочно принимаются за инфекцию, но фактически представляют костный мозг или костный мозг. вовлечение лейкемической инфильтрации.
У пациентов могут быть и другие злокачественные новообразования. Подтип лейкемии не может быть диагностирован на основании признаков и симптомов, потому что симптомы ОМЛ очень похожи на симптомы ОЛЛ, а иногда и хронического миелоидного лейкоза. Иногда признаки и симптомы других «маленьких круглых голубых опухолей» детского возраста, включая саркому Юинга, лимфому, рабдомиосаркому или нейробластому, могут имитировать симптомы ОМЛ. Каждая из этих опухолей имеет схожий вид под микроскопом, и только дальнейшее тестирование в сочетании с визуализацией и клинической информацией может отличить их друг от друга.
Апластическая анемия или другие синдромы недостаточности костного мозга могут проявляться схожими симптомами, физическими данными и показателями крови, такими как панцитопения, анемия, головные боли, инфекции, петехии или проявления кровотечения.
Что послужило причиной развития этой болезни в это время?
Подавляющее большинство случаев ОМЛ у детей возникает у пациентов с неизвестной предрасположенностью, и их можно рассматривать как спорадические.
Наиболее распространенной наследственной предрасположенностью к развитию ОМЛ (или ОЛЛ) является синдром Дауна.У детей с синдромом Дауна риск лейкемии примерно в 10-20 раз выше, чем у других детей. В течение первых 3 лет жизни дети с синдромом Дауна имеют особенно высокий риск развития мегакариобластного подтипа AML (FAB M7).
В целом, пациенты с синдромом Дауна составляют примерно 10% педиатрических пациентов с ОМЛ. Кроме того, примерно у 10% новорожденных с синдромом Дауна проявляется преходящее миелопролиферативное расстройство (ВНЧС).Это заболевание имитирует врожденный ОМЛ, но обычно проходит спонтанно в течение 4-6 недель. Ретроспективные исследования показывают, что FAB M7 AML разовьется у 20-30% младенцев с синдромом Дауна, а TMD разовьется в возрасте до 3 лет.
Унаследованные синдромы недостаточности костного мозга предрасполагают к ОМЛ. Некоторые из этих синдромов приводят к трехлинейной недостаточности (например, анемия Фанкони, врожденный дискератоз), тогда как другие в первую очередь влияют на одну или две гемопоэтические линии (например, синдром Костмана, анемия Даймонда-Блэкфана, синдром Швахмана-Даймонда, врожденная амегакариоктическая тромбоцитопения).
Другие наследственные заболевания, связанные с повышенной частотой развития ОМЛ, но обычно не характеризующиеся недостаточностью костного мозга, включают синдром Ли-Фраумени, синдром Блума, семейное заболевание тромбоцитов со склонностью к развитию ОМЛ, нейрофиброматоз типа 1 и синдром Нунана.
Были редкие сообщения о родственниках с несколькими случаями ОМЛ, происходящими в течение нескольких поколений, в которых не был идентифицирован какой-либо известный предрасполагающий синдром или другое состояние, но в которых была обнаружена общая конституциональная хромосомная аномалия.Моносомия 7 была наиболее частой отмеченной аномалией.
Есть несколько приобретенных состояний, которые были связаны с повышенным риском ОМЛ. Было отмечено, что пациенты с тяжелой апластической анемией (SAA), получающие иммуносупрессивные схемы и рекомбинантный гранулоцитарный колониестимулирующий фактор человека, имеют значительный риск (до 20%) развития миелодиспластического синдрома (MDS) или AML.
Пароксизмальная ночная гемоглобинурия также связана с повышенным риском развития МДС и ОМЛ, но встречается реже, чем САА в детской возрастной группе.
МДС считается предрасполагающим к развитию ОМЛ в любой возрастной группе, но ОМЛ, возникающий в результате МДС, гораздо чаще встречается у взрослых, чем у детей.
Факторы риска ОМЛ, связанные с воздействием, включают ионизирующее излучение и различные химиотерапевтические препараты.
Существует несколько редких наследственных и приобретенных факторов риска, которые, как было показано, связаны с повышенным риском ОМЛ в детстве.
Какие лабораторные исследования следует запросить для подтверждения диагноза? Как следует интерпретировать результаты?
Общий анализ кровии разница в количестве лейкоцитов являются ненормальными у подавляющего большинства детей с ОМЛ и могут демонстрировать цитопении одной, двух или трех линий.
В мазке периферической крови могут быть обнаружены бласты и / или незначительные изменения, указывающие на инфильтративный процесс, включая наличие «каплевидных» красных кровяных телец, относительную тромбоцитопению (количество тромбоцитов <100000 / мкл) или отсутствие соответствующего количества ретикулоцитов для степени поражения анемия.
Уровни лактатдегидрогеназы часто повышены, поскольку она содержится в лейкоцитах и «выливается» наружу, когда эти клетки переворачиваются.
Уровень мочевой кислоты часто повышен из-за быстрого обмена клеток и разрушения внутриклеточного содержимого, включая ДНК.
Химические анализы сыворотки могут отражать почечную недостаточность от легкой до умеренной с повышенным уровнем креатинина, гиперфосфатемию, гипокальциемию и другие метаболические маркеры синдрома лизиса опухоли.
Уровни СОЭ и СРБ обычно повышены и не особенно полезны, поскольку не помогают отличить ОМЛ от других воспалительных или инфекционных процессов. Обратное также верно; нормальный уровень СОЭ или СРБ не исключает AML.
Панели коагуляции(протромбиновое время, международное нормализованное отношение, активированное частичное тромбопластиновое время) могут продемонстрировать клинически значимую коагулопатию, особенно при APL (FAB M3).
Могут ли быть полезны визуализирующие исследования? Если да, то какие?
В целом, визуализация для педиатрического AML довольно ограничена, за исключением случаев, когда результаты фокусного физикального обследования предполагают, что у пациента может быть хлорома или внутреннее кровотечение из-за коагулопатии.
Подтверждение диагноза
После подозрения на общий анализ крови, истории болезни и физикального обследования окончательный диагноз AML ставится путем аспирации костного мозга и биопсии. Когда количество лейкоцитов высокое и есть бластные клетки периферической крови, проточная цитометрия может быть выполнена на периферической крови.Хотя это может дать точную диагностическую картину, аспирация костного мозга и биопсия по-прежнему являются золотым стандартом и должны выполняться, если процедуры не противопоказаны с медицинской точки зрения.
Морфологическая оценка выполняется с помощью стандартной световой микроскопии мазков аспирата костного мозга, окрашенных красителями Райта-Гимзы или аналогичными.
Проточная цитометрическая оценка экспрессии поверхностного антигена является окончательным подходом к классификации лейкемии.
Хромосомные анализы с помощью стандартного кариотипирования и флуоресцентной гибридизации in situ (FISH) следует проводить у детей с ОМЛ, поскольку они обнаруживают наличие хромосомных аномалий (например,g., транслокации, делеции), которые являются диагностическими, прогностическими и во многих случаях определяют терапевтические решения. Исследования FISH должны, как минимум, включать пробы для оценки inv (16) / t (16; 16), t (8; 21), t (15; 17), 11q23, -7 и -5 / 5q- .
Молекулярное тестирование на основе полимеразной цепной реакции также должно выполняться для выявления наличия мутаций в определенных генах (например, FLT3, NPM1, CEBPA), которые являются прогностическими и могут определять лечение.
Люмбальная пункция выполняется для оценки наличия или отсутствия лейкемического поражения ЦНС.Цитологическое исследование — единственный способ оценить это должным образом. Это должен делать педиатр-гематолог / онколог, имеющий большой опыт лечения пациентов детской онкологии. Визуализация обычно не показана, если нет очаговых неврологических признаков.
Если вы можете подтвердить, что у пациента острый миелоидный лейкоз, какое лечение следует начать?
Пациенты с подозрением на ОМЛ должны быть стабилизированы и переведены на попечение обученных детских онкологов в условиях, которые могут поддержать реанимацию детей.Полезны знания в области детской хирургии и анестезии, равно как и сильная служба трансфузионной медицины.
Для снижения риска серьезного кровотечения следует рассмотреть возможность применения агрессивных продуктов крови с тромбоцитами и, при наличии коагулопатии, свежезамороженной плазмой. Было показано, что в случаях подозрения на APL раннее лечение препаратом, индуцирующим дифференцировку, полностью транс-ретиноевой кислотой (ATRA) снижает риск серьезного кровотечения.
Пациенты с впервые диагностированной лейкемией подвергаются значительному риску заражения инвазивными бактериальными и грибковыми инфекциями из-за длительной абсолютной и функциональной нейтропении.У пациентов с лихорадкой следует проводить посев из стерильных участков и настоятельно рекомендуется незамедлительно использовать эмпирические противомикробные препараты.
Пациенты с высоким количеством лейкоцитов (> 100 000 / мкл) подвержены риску осложнений гиперлейкоцитоза. Пациентам с симптомами следует незамедлительно пройти обменное переливание крови или лейкоферез. Данные подтверждают использование аналогичных процедур для бессимптомных пациентов с гиперлейкоцитозом, но существуют разногласия относительно оптимального уровня лейкоцитов, при котором следует выполнять эти процедуры.У пациента с гипдерлейкоцитозом как можно скорее следует начинать окончательную терапию, направленную на лейкоз.
Первоначально пациенты должны получать гидратацию с помощью поддерживающих внутривенных жидкостей (ЭКО), в 1,5–2 раза превышающих поддерживающие, которые подщелачивают, чтобы попытаться поддерживать рН мочи примерно на уровне 6,5–7. Типичным ЭКО будет D5W1 / 4NS с 25-50 мэкв NaHCO 3 при двукратном обслуживании. Это делается для поддержания хорошего кровотока через почки и предотвращения повреждения почек в результате лизиса опухоли и повышения растворимости мочевой кислоты, которая выводится с мочой.
Пациентам не следует назначать стероидные препараты при подозрении на лейкоз, так как стероиды могут скрыть полный диагноз, временно уменьшая лейкемию.
В экстренных случаях любой продукт крови, который переливается, следует подвергать лейкофильтрации (для предотвращения передачи цитомегаловируса (ЦМВ)) и облучать. Предпочтительно сначала использовать ЦМВ-отрицательные продукты, пока не будут получены окончательные серологические результаты. Целесообразно обсудить любые возможные переливания с принимающим детским онкологом, чтобы заранее определить лучший план переливания и выбор продукта.
Пациентам следует давать лекарства для профилактики и / или лечения синдрома острого лизиса опухоли. В большинстве случаев используется аллопуринол, ингибитор ксантиноксидазы, который снижает выработку мочевой кислоты. Типичная доза аллопуринола составляет 100 мг / м 2 / доза каждые 8 часов. Для пациентов со значительной гиперфосфатемией используется фосфатное связующее, такое как гидроксид алюминия.
Расбуриказа, рекомбинантная форма уратоксидазы, которая непосредственно расщепляет и расщепляет мочевую кислоту, показана пациентам с клиническими проявлениями лизиса опухоли или людям с высоким риском из-за очень повышенного количества лейкоцитов (> 50 000-100 000 / мкл) или значительного экстрамедуллярная опухолевая нагрузка.Поскольку расбуриказа довольно дорога, ее обычно не назначают пациентам с низким риском лизиса опухоли, поскольку соотношение затрат и результатов не является благоприятным. И наоборот, у пациентов с высоким риском лизиса опухоли стоимость иногда однократной дозы расбуриказы и проявленная клиническая польза намного перевешивают риск и стоимость почечного диализа, которые могут потребоваться у этих пациентов.
После постановки окончательного диагноза можно начинать лечение лейкемии.
Какие стандартные подходы к лечению острого миелоидного лейкоза у детей?
Лечение ОМЛ относительно стандартизировано, и большинство детей получают лечение по схеме, разработанной в ходе текущего или недавно завершившегося клинического исследования.
Пациенты с ОМЛ, связанные с синдромом Дауна, и пациенты с ОПЛ лечатся по протоколам, отличным от тех, которые получают другие дети с ОМЛ.
Для вновь диагностированных пациентов стандарт лечения включает попытку вызвать ремиссию с помощью интенсивной комбинированной химиотерапии. Индукционная терапия ОМЛ обычно включает комбинацию двух наиболее активных агентов, цитарабина (обычно вводимого в «низких» дозах путем непрерывной инфузии или два раза в день в течение 7-10 дней, и антрациклина.Дополнительные агенты, используемые во время первого курса индукционной терапии, включают этопозид и / или 6-тиогуанин.
При современной терапии 80–85% детей с ОМЛ войдут в ремиссию после одного цикла химиотерапии с неудачами из-за рефрактерной лейкемии и / или смертью от токсичности или осложнений, таких как смертельная инфекция.
После завершения индукционной терапии генетические факторы риска лейкемии интегрируются с показателями раннего ответа на лечение для определения постиндукционной терапии.Чувствительные меры конечной индукции минимальной остаточной болезни (MRD), которые могут выявить 0,1% или меньше бремени оставшихся лейкозных клеток, используются для измерения ответа на лечение и, как было показано, позволяют предсказать окончательный прогноз.
Пациентам, у которых на основании этих факторов прогнозируется высокий риск рецидива, обычно предлагается аллогенная трансплантация гемопоэтических стволовых клеток (ТГСК) в первой ремиссии, если можно определить подходящего донора (родственного или неродственного). Пациенты, у которых на основании этих факторов прогнозируется относительно низкий риск рецидива, обычно лечатся тремя-четырьмя дополнительными курсами химиотерапии, большинство из которых включают высокие дозы цитарабина в качестве основы.
Каждый цикл терапии ОМЛ обычно связан с 2–4 неделями глубокой паницитопении и значительным риском инвазивной бактериальной и / или грибковой инфекции. По этой причине поддерживающая терапия является важным компонентом терапии ОМЛ. Пациенты часто госпитализируются в этот период панцитопении с очень низким порогом для начала эмпирической антибактериальной терапии. Обычно применяется профилактическое лечение для предотвращения дрожжевых / грибковых инфекций, но существуют разногласия относительно выбора агентов.
В отличие от ОЛЛ терапия ОМЛ не включает длительную низкоинтенсивную «поддерживающую» фазу, поскольку рандомизированные исследования показали, что поддерживающая терапия не улучшает исходы при ОМЛ.
Таргетная терапия, направленная на генетические поражения, вызывающие лейкемию, в настоящее время разрабатываются и тестируются; при AML лучшим примером являются ингибиторы рецепторной тирозинкиназы FLT3 для пациентов с определенным типом мутации в гене FLT3.
ОМЛ-терапия обычно включает профилактическое пресимптоматическое лечение, направленное на ЦНС, с интратекально вводимой химиотерапией.
Какие побочные эффекты связаны с каждым вариантом лечения?
Наиболее частым серьезным острым побочным эффектом химиотерапии является миелосупрессия, приводящая к анемии, нейтропении и тромбоцитопении. К другим частым острым побочным эффектам химиотерапии относятся тошнота, рвота, мукозит, алопеция и усталость. Редкие, но серьезные поздние эффекты химиотерапии включают бесплодие и второй рак (чаще всего связанный с лечением ОМЛ).
Отдельные химиотерапевтические препараты имеют свой собственный уникальный профиль побочных эффектов.
Антрациклины и родственные препараты (доксорубицин, даунорубицин, митоксантрон): риск острой и долгосрочной кардиотоксичности
Цитарабин: острая лихорадка, синдром ладони-стопы, синдром утечки капилляров
Этопозид: Острая анафилаксия / аллергические реакции
HSCT связан с множеством побочных эффектов, связанных как с интенсивной химиотерапией перед инфузией стволовых клеток (например, инфекция, тяжелая гепатотоксичность), так и с возникающими аллогенными иммунологическими эффектами (болезнь трансплантат против хозяина).
Каковы возможные исходы острого миелолейкоза у детей?
При правильном лечении большинство детей, у которых сегодня диагностирован ОМЛ, будут излечены. В целом, примерно 60% детей с диагнозом AML будут выживать в течение длительного времени, при этом некоторые подгруппы (APL, AML, связанный с синдромом Дауна, AML с основным связывающим фактором) имеют примерно 80% шанс на излечение. У других подгрупп пациентов прогноз гораздо хуже. Недавняя работа была сосредоточена на выявлении новых агентов с новыми механизмами действия и улучшении эффективности и переносимости ТГСК.
Без лечения ОМЛ приводит к летальному исходу. Семьям следует мягко сказать, что при современном лечении излечение возможно, но не у значительной части пациентов.
Большинство людей, успешно пролеченных от ОМЛ в детстве, могут рассчитывать на отличное качество жизни после лечения, достижение академического, рабочего и социального статуса во взрослом возрасте, аналогичного их братьям и сестрам или сверстникам, сопоставимым по возрасту и социально-экономическому положению. Однако вполне возможны отдаленные побочные эффекты и поздние осложнения.
Что вызывает острый миелолейкоз у детей и как часто это встречается?
В Соединенных Штатах заболеваемость ОМЛ среди детей младше 20 лет составляет примерно 7 случаев на миллион в год, или примерно 600 новых случаев в год. Это составляет 19% лейкозов в детском возрасте, остальную часть составляют ОЛЛ (76%) и редкие хронические лейкозы детского возраста (5%). Заболеваемость ОМЛ у детей в возрасте от 0 до 19 лет в США увеличивалась со скоростью 1,3% в год с 1975 по 2004 год.
В отличие от ОЛЛ заболеваемость ОМЛ у детей не имеет явного возрастного пика, хотя наблюдается небольшое увеличение заболеваемости в периоды неонатального и подросткового возраста. После 20 лет заболеваемость ОМЛ неуклонно возрастает с возрастом, так что у взрослых ОМЛ примерно в четыре раза чаще, чем ОЛЛ. Заболеваемость ОМЛ у мальчиков и девочек существенно не различается.
Имеются данные о том, что заболеваемость ОМЛ у детей зависит от расы, этнической принадлежности и географии.В США дети латиноамериканского происхождения имеют значительно более высокую заболеваемость ОМЛ (9 случаев на миллион), что в первую очередь связано с увеличением заболеваемости подтипом APL.
Частота вторичного ОМЛ после лечения других злокачественных новообразований увеличивается у педиатрических пациентов, вероятно, в результате увеличения выживаемости и увеличения использования эпиподофиллотоксинов (таких как этопозид) для лечения многих твердых опухолей у детей. Риск вторичного ОМЛ был связан не только с эпиподофиллотоксинами, но и с антрациклинами (которые, как и эпиподофиллотоксины, ингибируют топоизомеразу II), алкилирующими химиотерапевтическими агентами и облучением.
Как эти патогены / гены / воздействия вызывают болезнь?
Несколько линий доказательств предполагают, что ОМЛ у детей является заболеванием, которое возникает в результате накопления двух или более нарушений функции определенных онкогенов и / или генов-супрессоров опухолей.
Наиболее частой рецидивирующей цитогенетической аномалией у детей и взрослых с ОМЛ является транслокация t (8; 21), которая приводит к экспрессии слитого белка AML1-ETO. Гривз с соавторами исследовали ДНК, выделенную из архивных карт пятен крови новорожденных (карты Гатри) детей, у которых t (8; 21) / AML1-ETO AML развился до 10 лет спустя, и обнаружили, что t (8; 21) / AML1-ETO был обнаружен при рождении у большинства этих детей.
Это исследование предоставило доказательства того, что значительная часть случаев ОМЛ у детей возникает внутриутробно, с появлением миелоидного предшественника, который становится «прелейкемическим» в результате первой «разрешающей» мутации. Только спустя годы, иногда годы, один из этих предлейкозных предшественников приобретает вторую, «промо-мутацию», которая приводит к полномасштабному случаю лейкемии.
Подобный феномен был продемонстрирован у детей с ОЛЛ с цитогенетическими аномалиями t (12; 21) / TEL-AML1 и t (4; 11) / MLL-AF4.Появилась модель миелоидного лейкемогенеза, в которой мутации, которые в первую очередь вызывают нарушение дифференцировки, такие как AML1-ETO и PML-рецептор ретиноевой кислоты-альфа (RAR-a), взаимодействуют с мутациями, которые обеспечивают преимущество пролиферации / выживаемости, такими как FLT3 или Мутации RAS, вызывающие ОМЛ.
Специфические повторяющиеся цитогенетические и молекулярные аномалии, которые были связаны с ОМЛ, можно в широком смысле классифицировать как химерные факторы транскрипции, мутационно активированные онкогены или другие различные аномалии.
Химерные факторы транскрипции обычно образуются в результате хромосомных транслокаций, которые сливают ДНК-связывающий домен активатора транскрипции с репрессором транскрипции. Таким образом, репрессор транскрипции перенаправляется на гены-мишени активатора транскрипции, многие из которых, как было показано, играют важную роль в дифференцировке миелоида. Функционально считается, что это вызывает блок дифференцировки, который характеризует острый лейкоз. Наличие одной из этих транслокаций в отдельном случае ОМЛ может иметь важное прогностическое и терапевтическое значение.
AML со слиянием t (8; 21) и AML1-ETO: транслокация t (8; 21) связана с характерными клиническими, морфологическими и иммунофенотипическими особенностями. Хлоромы (экстрамедуллярные скопления лейкозных клеток, также известные как гранулоцитарная саркома) встречаются примерно в 20% случаев. Более 80% из t (8; 21) случаев классифицируются как FAB типа M2; и наоборот, из всех случаев, классифицируемых как FAB M2, примерно 40% будут иметь t (8; 21). Иммунофенотип случаев с t (8; 21) часто включает экспрессию В-клеточного антигена CD19 и антигена природных киллеров CD56.И у взрослых, и у детей t (8; 21) ассоциируется с благоприятным прогнозом.
AML со слиянием inv (16) или t (16; 16) и CBFB-MYh21: аномалии inv (16) и t (16; 16) по существу патогномоничны для подтипа FAB M4Eo, и оба дают благоприятный прогноз для обоих взрослые и дети с ОМЛ.
AML с (15; 17) и слияние PML-RARA (и варианты): AML с t (15; 17) неизменно ассоциируется с APL, отдельным подтипом AML, который лечится иначе, чем другие типы AML из-за его отмеченного чувствительность к дифференцирующим эффектам ATRA и триоксида мышьяка.Транслокация t (15; 17) приводит к продукции гибридного белка, включающего
RAR-α и PML. Другие гораздо менее распространенные транслокации с участием RAR-α также могут приводить к APL [например, t (11; 17) с участием гена PLZF]. Идентификация пациентов с t (11; 17) важна из-за их пониженной чувствительности к ATRA.
AML с перестройками гена MLL: транслокации хромосомной полосы 11q23 с участием гена MLL, включая большинство случаев AML, вторичного по отношению к эпиподофиллотоксину, связаны с моноцитарной дифференцировкой (FAB M4 и M5).Прогноз для de novo AML с перестройкой MLL является промежуточным, но для случаев, связанных с лечением, неблагоприятный.
AML со слиянием t (1; 22) и OTT-MAL: транслокация t (1; 22) (p13; q13) ограничена острым мегакариобластным лейкозом (AMKL) и встречается в одной трети случаев AMKL у детей. . У небольшого числа детей, о которых сообщалось, наличие t (1; 22), по-видимому, связано с плохим прогнозом, хотя после интенсивной терапии были отмечены долгосрочные выжившие.
Мутационно активированные онкогены
AML с мутациями FLT3: Мутации FLT3 с внутренней тандемной дупликацией (ITD) встречаются примерно у 15% детей с AML и связаны с плохим прогнозом, особенно когда оба аллеля мутированы или имеется высокое отношение мутантного аллеля к нормальному аллель.Мутации в киназном домене (KD)
FLT3 также были выявлены примерно у 7% детей с AML. Мутации FLT3-KD не имеют такого же отрицательного прогностического значения, как мутации FLT3-ITD. Мутации FLT3 встречаются у 30-40% детей и взрослых с APL, а мутации FLT3-ITD прочно связаны с микрогранулярным вариантом (M3v) и гиперлейкоцитозом. Прогностическое влияние FLT3-ITD на APL неясно.
AML с мутациями RAS или c-KIT: мутации RAS (N-RAS или
KRAS) встречаются примерно в 20%, а мутации c-KIT — примерно в 5% случаев AML у детей.Однако активирующие мутации c-KIT встречаются в 20-40% случаев AML с t (8; 21) и inv (16) и связаны с относительно плохим прогнозом по сравнению с аналогичными пациентами без мутаций c-KIT.
Прочие отклонения
Хромосомные аномалии, связанные с худшим прогнозом у взрослых с ОМЛ, включают хромосому 7 [моносомию 7 и del (7q)], хромосому 5 [моносомию 5 и del (5q)] и длинное плечо хромосомы 3 или t (3; 3) ) (q21; q26)). Эти цитогенетические подгруппы также связаны с плохим прогнозом у детей с ОМЛ.
GATA-1: Мутации GATA-1 присутствуют у большинства, если не у всех, детей с синдромом Дауна либо с преходящим миелопролиферативным заболеванием (TMD), либо с AMKL. Мутации
GATA-1 не наблюдаются у детей с AMKL, у которых нет синдрома Дауна, а также у детей с синдромом Дауна и другими типами лейкемии. GATA-1 — это фактор транскрипции, необходимый для нормального развития эритроидных клеток, мегакариоцитов, эозинофилов и тучных клеток. Мутации GATA-1 придают повышенную чувствительность к цитарабину, возможно, за счет снижения экспрессии цитидиндезаминазы и, таким образом, объясняют лучшие результаты у детей с синдромом Дауна и AML M7 при лечении схемами, содержащими цитарабин.
CEBPA и NPM1: мутации в генах CEBPA и
NPM1 встречаются примерно в 5-10% случаев AML у детей и обычно коррелируют с благоприятным исходом у пациентов с нормальным кариотипом без FLT3 / ITD.
Как можно предотвратить ОМЛ в детстве?
На сегодняшний день нет данных, позволяющих предположить, что детский AML является предотвратимым заболеванием.
Какие доказательства?
Creutzig, U, Zimmermann, M, Ritter, J. «Стратегии лечения и долгосрочные результаты у педиатрических пациентов, получавших лечение в четырех последовательных испытаниях AML-BFM». Лейкемия. т. 19. 2005. С. 2030–2042. (Немецкий опыт борьбы с отмыванием денег в детстве)
Касперс, GJ, Цваан, CM. «Острый миелоидный лейкоз у детей: к качественному излечению всех пациентов». Haematologica. т. 92. 2007. С. 1519-32. (Хороший обзор лечения и прогноза AML у детей)
Malinge, S, Израэли, S, Crispino, JD. «Понимание проявлений, исходов и механизмов лейкемогенеза при синдроме Дауна». Кровь. т.113. 2009. С. 2619–28. (Клинико-биологический обзор преходящего миелопролиферативного заболевания, связанного с синдромом Дауна, и острого лейкоза.)
Малруни, Д.А., Довер, округ Колумбия, Ли, С. «Двадцатилетнее наблюдение за выжившими в детском возрасте и молодыми взрослыми острым миелоидным лейкозом: отчет исследования выживших после рака в детстве». Рак. т. 112. 2008. С. 2071-9. (Поздние эффекты и выживаемость в детском AML)
Niewerth, D, Creutzig, U, Bierings, MB. «Обзор трансплантации аллогенных стволовых клеток при впервые диагностированном остром миелоидном лейкозе у детей». Кровь. т. 116. 2010. С. 2205-14. (Всестороннее обсуждение роли аллогенных ТГСК в ОМЛ у детей)
Радхи, М., Мешинчи, С., Гамис, А. «Прогностические факторы при остром миелоидном лейкозе у детей». Curr Hematol Malig Rep. vol. 5. 2010. С. 200-6. (Обзор прогностических факторов и оснований для стратификации риска при ОМЛ у детей)
Sanz, MA, Grimwade, D, Tallman, MS. «Ведение острого промиелоцитарного лейкоза: рекомендации экспертной группы от имени European LeukemiaNet». Кровь. т. 113. 2009. С. 1875–91. (Полное руководство по лечению острого промиелоцитарного лейкоза)
Смит, Ф.О., Алонзо, Т.А., Гербинг, РБ. «Отдаленные результаты у детей с острым миелоидным лейкозом: отчет о трех последовательных испытаниях фазы III, проведенных Детской онкологической группой: CCG 251, CCG 213 и CCG 2891». Лейкемия. т. 19. 2005. С. 2054–62. (Североамериканский опыт лечения ОМЛ у детей)
Vardiman, JW, Thiele, J, Arber, DA.«Пересмотр в 2008 г. классификации миелоидных новообразований и острого лейкоза Всемирной организации здравоохранения (ВОЗ): обоснование и важные изменения». Кровь. т. 114. 2009. С. 937-51. (Текущий диагностический подход и схема классификации AML)
Продолжающиеся споры относительно этиологии, диагностики и лечения
Наиболее важным спором в отношении ОМЛ у детей является наиболее целесообразное использование аллогенных ТГСК при первой ремиссии. В последнем завершенном протоколе детской онкологической группы (COG) пациенты с промежуточным цитогенетическим риском были распределены на ТГСК на основании доступности HLA-идентичного семейного донора.Пациенты с низким цитогенетическим риском и пациенты с неудачной первичной индукцией были распределены на ТГСК от лучшего доступного донора. Пациенты с благоприятным цитогенетическим риском не были отнесены к ТГСК.
В текущем текущем протоколе COG пациенты с промежуточным цитогенетическим риском распределяются на HSCT с лучшим доступным донором на основании наличия выявляемого MRD в конце первого индукционного курса. Всем пациентам с высоким аллельным соотношением FLT3 – ITD-положительных также назначают ТГСК с лучшим доступным донором.
Между различными группами существуют значительные разногласия относительно того, является ли подход COG к HSCT в AML оптимальным. Рандомизированные испытания, посвященные этому противоречию, отсутствуют, поэтому противоречие, вероятно, сохранится в обозримом будущем.
Схемы цитотоксической химиотерапии, используемые для лечения ОМЛ, обладают значительной токсичностью, и маловероятно, что значительное улучшение лечения будет достигнуто за счет дальнейшей интенсификации химиотерапии. Таким образом, существует большой интерес к разработке «молекулярно-целевых» методов лечения, направленных на основные мутации, вызывающие ОМЛ.Существенные улучшения результатов были достигнуты при использовании этого подхода в APML с ATRA и триоксидом мышьяка, но на сегодняшний день в области таргетной терапии для других подтипов AML был достигнут незначительный прогресс.
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
анализов крови | Ассоциация миозитов
Доктор может выбрать несколько анализов крови. Ниже приводится список некоторых из них. Если не указано иное, все эти тесты требуют взятия пробы крови с помощью иглы. Некоторые анализы крови требуют, чтобы вы не ели и не пили, за исключением воды, примерно за восемь часов до анализа. Поскольку упражнения могут повлиять на результаты некоторых тестов, вам может потребоваться ограничить их за несколько дней до теста, чтобы избежать ложно завышенных результатов.Некоторые лекарства также могут повлиять на результаты этих тестов, поэтому обязательно проконсультируйтесь с врачом, если вы вообще принимаете какие-либо лекарства, включая аспирин или другие лекарства, отпускаемые без рецепта.
Альдолаза — это фермент, особенно в печени и скелетных мышцах. Когда печень или мышцы повреждены, клетки выпускают свое содержимое (включая альдолазу) в кровоток. Поскольку мышечная слабость может быть вызвана проблемами либо нервов, либо мышц, этот тест определяет слабость, вызванную мышечными проблемами.Альдолаза не изменится, если слабость вызвана неврологическими проблемами.
Нормальные диапазоны могут незначительно отличаться в зависимости от калибровок конкретной лаборатории. Также существуют небольшие различия в нормальных диапазонах в зависимости от возраста и пола. Однако, как правило, нормальные показатели у взрослых составляют от 1,0 до 7,5 единиц на литр.
Антинуклеарные антитела (также известные как ANA) — это скрининговый анализ крови, позволяющий определить, есть ли у вас аутоиммунное заболевание. Антитела — важная часть иммунной системы.Они борются с инфекциями, вирусами и другими чужеродными веществами, которые могут вызывать болезни. Когда эта защитная система направлена на борьбу с собственными тканями организма, возникает аутоиммунное заболевание, и тест на ANA будет положительным. Однако положительный результат ANA не позволяет идентифицировать конкретное заболевание. Тем более, что отрицательный результат теста не исключает миозит.
Креатинкиназа (также известная как CK или креатинфосфокиназа [CPK]) — важный диагностический анализ крови при миопатиях. CK — это тип белка, называемого ферментом, который особенно активен в скелетных мышцах, сердечной ткани и головном мозге.Когда мышечная ткань повреждена, клетки выпускают свое содержимое в кровоток, вызывая повышенный уровень КФК в крови.
УровниCK в крови могут варьироваться в зависимости от ряда факторов, включая пол, расу, возраст, активность, состояние здоровья, метод тестирования и многое другое. Более высокие уровни CK в сыворотке могут указывать на повреждение мышц в результате хронического заболевания или острого мышечного повреждения. При миозите нередко уровни КФК намного превышают верхний предел нормы. Если тест CK указывает на повреждение мышц, потребуется больше тестов, чтобы точно определить, где произошло повреждение мышцы.
УровниКК часто используются для оценки развития болезни после лечения. Однако это ненадежный показатель активности заболевания, и нормальный уровень ферментов не исключает полностью возможность воспаления мышц. Пациенты с миозитом иногда задаются вопросом, почему они чувствуют себя лучше или хуже, чем показывают их уровни КФК. Уровни могут отставать от улучшения или обострения болезни, и на них может влиять активность или другие факторы. Кроме того, на запущенной стадии заболевания уровни мышечных ферментов в сыворотке могут быть устойчиво низкими на фоне сильной мышечной слабости.
Скорость оседания (также называемая скоростью оседания эритроцитов [СОЭ] или скоростью оседания) измеряет отек и воспаление мышц. Врачи используют скорость седативного эффекта, чтобы наблюдать за развитием воспаления мышц. Этот тест не специфичен для конкретного заболевания, а просто определяет наличие и тяжесть воспаления. Его можно использовать для контроля эффекта от лечения.
Результаты измерения уровня седиментации выражаются в миллиметрах (мм), на которые красные кровяные тельца попадают в пробирку за один час (час).Нормальный диапазон варьируется в зависимости от лабораторного оборудования, возраста, пола, беременности, инфекции и других факторов. Скорость седации будет выше при более сильном воспалении.